Резюме
Введение. Ювенильный идиопатический артрит – наиболее частое ревматическое заболевание в детском возрасте. Адалимумаб – препарат выбора при полиартрите, HLA-B27-ассоциированном артрите, псориатическом артрите, а также при ассоциации артрита с энтезитами и увеитами. Представляет интерес оценка эффективности и безопасности генно-инженерного биологического препарата адалимумаб у пациентов с полиартикулярным серонегативным по ревматоидному фактору ювенильным идиопатическим артритом, проживающих в Самарском регионе.
Цель работы. Цель исследования состояла в оценке эффективности и безопасности генно-инженерного биологического препарата адалимумаб у пациентов с полиартикулярным серонегативным по ревматоидному фактору ювенильным идиопатическим артритом, проживающих в Самарском регионе.
Материалы и методы. Проведено ретро- и проспективное исследование 32 (8 мальчиков, 24 девочки) пациентов с полиартикулярным ювенильным идиопатическим артритом, серонегативным по ревматоидному фактору. Диагностика заболевания осуществлялась с использованием диагностических критериев Международной лиги ревматологических ассоциаций. Исследование проводилось с 2018 по 2022 г. на базе Самарского областного клинического кардиологического диспансера им. В. П. Полякова. Анализ эффективности терапии проводился в течение 6 визитов с интервалом в 70 дней и включал оценку функциональной способности с использованием опросника CHAQ. К показателям эффективности терапии относилось достижение улучшения на 50-90% при лекарственной ремиссии заболевания.
Результаты. Доказаны эффективность, безопасность, хорошая переносимость антицитокинового генно-инженерного биологического препарата адалимумаб при лечении детей с полиартикулярным серонегативным по ревматоидному фактору ювенильным идиопатическим артритом.
Заключение. Полученные результаты позволяют сделать вывод о целесообразности применения препарата адалимумаб у больных с рефрактерностью к иммуносупрессивной терапии, принятой для лечения юношеского артрита, и считать такой подход перспективным в детской ревматологии.
Конфликт интересов. Авторы статьи подтвердили отсутствие конфликта интересов, о котором необходимо сообщить.
Ювенильный идиопатический артрит (ЮИА) – наиболее частое ревматическое заболевание в детском возрасте. Так, в 2007 г. на территории Российской Федерации среди детей до 14 лет регистрировалось 45,8 случая ЮИА на 100 тыс. детского населения, а в возрасте 15-17 лет – 116,4 на 100 тыс. подростков. В 2020 г. число случаев ЮИА среди детей до 14 лет составило 49,57 на 100 тыс. детского населения, 15-17 лет – 121,53 на 100 тыс. подростков [1].
Заболевание подразделяют на различные подтипы в зависимости от основных клинических признаков и течения. Диагноз ЮИА основывается на следующих критериях – начало заболевания в возрасте до 16 лет и артрит, длящийся более шести недель: полиартикулярный ЮИА (пЮИА), серонегативный пЮИА, ЮИА с системным началом (сЮИА), олигоартикулярный ЮИА, артрит, связанный с энтезитом, ювенильный псориатический артрит и недифференцированный ЮИА [2, 3].
Медикаментозное лечение ЮИА состоит из двух частей – небиологическое и биологическое. Первое включает нестероидные противовоспалительные препараты (например, ибупрофен, индометацин, напроксен), глюкокортикостероиды (ГКС) и противоревматические препараты, модифицирующие заболевание (например, метотрексат, сульфасалазин, лефлуномид, циклоспорин А). Эффективность и безопасность небиологического медикаментозного лечения была показана ранее во многих исследованиях [4, 5].
Несмотря на принципиально безопасное и эффективное использование указанных препаратов при лечении ЮИА, у части пациентов сохраняется активность заболевания, неконтролируемое воспаление и серьезные осложнения, что, вероятнее всего, обусловлено сложным патогенетическим механизмом развития ЮИА (активация клеточного, гуморального и врожденного иммунитета). Появление биологических агентов, нацеленных на специфические провоспалительные цитокины – интерлейкин-1 (ИЛ-1), ИЛ-6 и фактор некроза опухоли (ФНО-α, он же TNF-α), ответственные за патогенез заболевания, значительно изменило его течение [5]. Генно-инженерные препараты (ГИБП) способны селективно блокировать отдельные звенья иммунопатологического процесса [6], давая возможность улучшения качества жизни пациентов, достижения более длительной ремиссии и уменьшения последствий заболевания [7].
К ГИБП относится адалимумаб (Хумира), представляющий собой полностью гуманизированное моноклональное антитело, нацеленное на ФНО-α и ингибирующее его взаимодействие с соответствующим рецептором (TNFR) на клеточной поверхности p55 и p75. Адалимумаб связывается с растворимым ФНО-α, нейтрализуя его биологические эффекты [8]. По данным немецкого реестра биологических препаратов, адалимумаб высокоэффективен у детей и подростков с воспалительными заболеваниями. Более того, лечение адалимумабом безопасно и эффективно у пациентов с ЮИА [9, 10]. По данным голландского реестра биологических препаратов The Dutch Register, по результатам рандомизированных двойных слепых плацебо-контролируемых и открытых пилотных исследований адалимумаб эффективен в качестве терапии второй линии у пациентов с ЮИА (кроме подтипа системного заболевания), не ответивших на базисные препараты в адекватных дозах, что является показанием для назначения ГИБП. Адалимумаб – препарат выбора при полиартрите, HLA-B27-ассоциированном и псориатическом артрите, а также при ассоциации артрита с энтезитами, увеитами [11-13].
В настоящее время известны результаты многих клинических испытаний ГИБП адалимумаб, свидетельствующие о его эффективности и безопасности. Доза адалимумаба составляет 24 мг/м2 в течение 15 дней (максимум 40 мг). Адалимумаб вводят подкожно (п/к) при лечении ювенильного ревматоидного артрита [8, 11].
Целью данной работы было оценить эффективность и безопасность ГИБП адалимумаб у пациентов с ЮИА, проживающих в Самарском регионе, в сопоставлении с данными многоцентровых исследований.
Материалы и методы исследования
Проведено ретро- и проспективное исследование у детей с полиартикулярным ЮИА, серонегативным по ревматичскому фактору (РФ), с использованием клинико-анамнестических, лабораторных и инструментальных методов обследования. Перед началом лечения от родителей детей и пациентов в возрасте 14 лет и старше было получено письменное информированное согласие. Адалимумаб назначался на основании заключения комиссии по назначению ГИБП в Самарском областном клиническом кардиологическом диспансере (СОККД) им. В. П. Полякова.
Исследование проводилось с 2018 по 2022 г. на базе СОККД им. В. П. Полякова. В исследование вошли 32 пациента (8 мальчиков, 24 девочки) с полиартикулярным серонегативным юношеским артритом, проживающие в Самарском регионе. Диагностика заболевания осуществлялась с использованием диагностических критериев Международной лиги ревматологических ассоциаций (International League of Associations for Rheumatology, ILAR) [11, 12]. Средний возраст пациентов составил 10,75 ± 3,08 года (n = 32, Ме = 10,75, m = 0,79). В качестве противоревматической терапии до начала лечения адалимумабом дети получали нестероидные противовоспалительные препараты, метотрексат, Метипред, преднизолон (табл. 1).
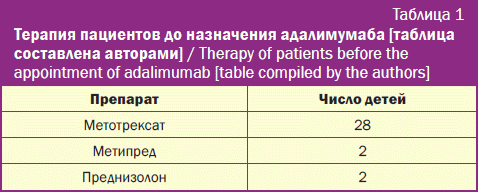
После проведения курсов терапии до назначения адалимумаба улучшения состояния пациентов не отмечалось. Учитывая отсутствие эффекта от проводимой терапии иммунодепрессантами в течение 3 месяцев, прогрессирование процесса (активный суставной синдром, высокие лабораторные показатели активности заболевания, включая ФНО-α), комиссией принималось решение о назначении ГИБП адалимумаб на фоне продолжающейся терапии метатрексатом. Адалимумаб в дозе 40 мг вводился подкожно 1 раз в 2 недели; метотрексат – в дозе 15-25 мг/м2 стандартной поверхности тела – 1 раз в неделю внутримышечно. При первом назначении препарата адалимумаб у всех больных отмечался активный суставной синдром. Отсутствие показателей, свидетельствующих о почечной и печеночной недостаточности, а также данных за острую и хроническую инфекцию являлось критерием включения больных в данное исследование. Кроме этого, был исключен туберкулез на основании отрицательных результатов туберкулиновых тестов (реакция Манту, Диаскин-тест). Критериями исключения были также другие формы ЮИА и возраст пациентов 18 и более лет. Группы контроля не было.
Анализ эффективности терапии проводился в течение 6 визитов с интервалом в 70 дней и включал оценку функциональной способности с использованием опросника под названием «Анкета оценки здоровья детей» (Childhood Health Assesment Questionnaire, CHAQ):
0 баллов – ребенок выполняет действие без всяких сложностей;
1 балл – с некоторыми сложностями;
2 балла – со значительными сложностями;
3 балла – не способен выполнить действие из-за тяжести заболевания.
Нами рассчитывался индекс функциональной недостаточности с минимальным значением 0 и максимальным – 3. Индекс CHAQ < 1,5 соответствовал минимальным и умеренным, ≥ 1,5 – выраженным нарушениям. Оценка выраженности болевого синдрома и общего самочувствия проводилась по 100 мм Visual Analogue Scale Pain Intensity Assessment – Визуальной аналоговой шкале (ВАШ), где 0 соответствовал отсутствию симптома, а 100 – его максимальной выраженности. Оценивались количество суставов с активным артритом и ограниченным диапазоном движения; значение скорости оседания эритроцитов (СОЭ). Эффективность лечения определялась по педиатрическим критериям Американской коллегии ревматологов (АКР-педи) в течение 6 визитов с интервалом в 70 дней, шестой визит осуществлялся путем телефонного контакта через 70 дней после пятого визита, во время которого собиралась информация о серьезных нежелательных явлениях (НЯ).
Показателем исследования являлась оценка общего числа событий или распределение количественных признаков в выборке исследования в определенный момент времени. Целевые показатели устанавливали на основании данных, полученных из вторичных источников информации (эффективность лечения определялась по педиатрическим критериям АКР-педи) [11]. Коррекцию результатов исследования осуществляли путем стратификации по критериям АКР-педи в зависимости от сроков применения ГИБП адалимумаб. Размер выборки предварительно не рассчитывался.
Последовательность формирования выборки исследования представлена на рис. 1.
Не включались в исследование пациенты с вариантом течения ЮИА, отличным от полиартикулярного; с серопозитивной формой; не получающие лечение ГИБП; получающие лечение любым ГИБП, кроме адалимумаба; получающие адалимумаб в составе комплексной терапии.
В процессе исследования соблюдались условия его остановки после шестого визита пациента.
Статистическая обработка данных проводилась с помощью лицензированного программного обеспечения SPSS Statistics, версия 21 (лицензия № 20130626-3). Значения медианы [25; 75] процентиля использовались в ходе лечения для оценки количественных признаков. Для независимых выборок статистические различия рассчитывались с учетом критерия Стьюдента, в случае отклонения от нормального распределения проводилось вычисление медианы (Ме). Различия при р < 0,05 считались статистически значимыми.
Перед началом оценки результатов лечения, проводимой по протоколу ведения детей с ЮИА, от каждого пациента было получено информированное согласие.
Результаты
В исследование вошли 32 пациента (8 мальчиков, 24 девочки) с полиартикулярным ЮИА, серонегативным по РФ. У всех пациентов на момент начала исследования выявлен артрит с выраженными нарушениями (рис. 2). При проведении корреляционного анализа значений показателей CHAQ первого и пятого визитов получен достоверный результат, доказывающий положительное влияние адалимумаба на течение болезни (р < 0,001). Таким образом, анализ функциональной способности пациентов с использованием опросника CHAQ позволил отметить улучшение качества жизни в разных ее сферах (рис. 2).
Среднее значение СОЭ на момент начала исследования составило 30,375 ± 10,770. На фоне терапии показатель СОЭ нормализовался. Доказано статистически значимое снижение (р = 0,001) данного показателя (рис. 3).
Среднее значение уровня боли при первом визите достоверно снизилось к пятому визиту (рис. 4) (р < 0,001), что доказывает положительное влияние исследуемого препарата на течение заболевания.
Полученные показатели оценки влияния болезни на самочувствие ребенка также отражали улучшение его состояния на фоне проводимой терапии (р = 0,001) (рис. 5).
При первом визите среднее количество суставов с активным артритом составило 10,500 ± 6,512, при пятом – 1,688 ± 3,511 (p = 0,001) (рис. 6).
В ходе шестого визита НЯ не выявлены.
В процессе оценки эффективности лечения по педиатрическим критериям АКР-педи получены следующие результаты: ко второму визиту улучшения на 30% были зарегистрированы у 100% пациентов; на 50% – у 91% (29 человек), на 70% – у 75% (24 человека); на 90% – у 63% (20 человек). К третьему визиту улучшения на 30% фиксировались у 100% пациентов; на 50% – также у 100%, на 70% – у 88% (28 человек); на 90% – у 66% (21 человек). К четвертому визиту улучшения на 30% отмечались у 100% пациентов; на 50% – у 100%, на 70% – у 88% (28 человек); на 90% – у 66% (21 человек); к пятому визиту улучшения на 30% были у 100% пациентов; на 50% – у 100%, на 70% – также у 100%; на 90% – у 97% пациентов (31 человек).
Обсуждение
В целом лечение адалимумабом оказалось эффективным у подавляющего большинства больных с полиартикулярным серонегативным по РФ ЮИА. Эффективность терапии подтверждена статистически достоверными результатами. По критериям AКР-педи положительная динамика отмечалась у всех пациентов уже ко второму визиту. Проведенное исследование свидетельствует об эффективности и безопасности лечения данной категории больных препаратом адалимумаб.
Среди обстоятельств, которые могли повлиять на конечный результат исследования, можно выделить следующие: размер выборки, при увеличении которой полученные результаты были бы более достоверными; отсутствие группы сравнения (получающие другие ГИБП; получающие адалимумаб и метотрексат и др.), ограниченное количество лабораторных показателей активности воспаления, не позволяющее провести глубокий математический анализ [14].
C начала XXI века отмечается значительное улучшение диагностики аутоиммунных заболеваний, внедрение инновационных методов лечения ревматических заболеваний с помощью ГИБП [15, 16]. Применение последних обес-печивает выраженный противовоспалительный эффект и в значительной степени предотвращает деструкцию суставов [16]. ГИБП способны избирательно воздействовать на ключевые патогенетические звенья аутоиммунного процесса, предотвращая инвалидизацию больного и тем самым улучшая качество жизни [17].
Стратегическая цель лечения ЮИА базируется на принципах контролируемого лечения ревматоидного артрита, а именно лечения до достижения цели (от англ. treatment to target – T2T). В наше исследование были включены дети, у которых отмечалась неэффективность базисных препаратов в адекватных дозах, что является показанием для назначения ГИБП. При выборе препарата адалимумаб мы руководствовались доказательствами его эффективности и безопасности при лечении различных вариантов ЮИА, представленными в целом ряде исследований [18], и его способностью блокировать синтез ФНО-α, подавляя образование не только ИЛ-1, но ИЛ-6 и ИЛ-8, простагландинов, оксида азота и др.
Результаты нашего исследования подтвердили, что терапия адалимумабом полиартикулярного серонегативного варианта ЮИА у детей Самарского региона значительно улучшила качество жизни пациентов, была эффективной и безопасной (по критериям АКР-педи), что соответствует данным научной литературы и расширяет их.
Заключение
Полученные данные об эффективности и безопасности препарата адалимумаб у детей с ЮИА позволяют сделать вывод об их соответствии результатам многоцентровых исследований, а также о целесообразности применения препарата адалимумаб у больных с рефрактерностью к иммуносупрессивной терапии и считать такой подход перспективным в детской ревматологии.
Благодарности.
Коллектив авторов выражает благодарность коллективу детского кардиохирургического и кардиоревматологического отделения СОККД им. В. П. Полякова за помощь в проведении исследования и оценки результатов.
Вклад авторов:
Авторы внесли равный вклад на всех этапах работы и написания статьи.
Contribution of authors:
All authors contributed equally to this work and writing of the article at all stages.
Литература/References
- Санталова Г. В., Плахотникова С. В., Шорохов С. Е.; ФГБОУ ВО СамГМУ Минздрава России. Современные аспекты диагностики и терапии ювенильного идиопатического артрита: учебное пособие. Самара: ООО «Порто-принт», 2021. 61 с. [Santalova G. V., Plakhotnikova S. V., Shorokhov S. E.; FSBEI IN SamSMU of the Ministry of Health of Russia. Modern aspects of diagnosis and therapy of juvenile idiopathic arthritis: a textbook. Samara: Porto-print LLC, 2021. 61 p. (In Russ.)]
- Алексеева Е. И. Ювенильный идиопатический артрит: клиническая картина, диагностика, лечение. Вопросы современной педиатрии. 2015; 14 (1): 78-94. [Alekseeva E. I. Juvenile idiopathic arthritis: clinical picture, diagnosis, treatment. Voprosy sovremennoi pediatrii. 2015; 14 (1): 78-94. (In Russ.)]
- Игишева Л. Н., Притчина С. С., Быкова Ю. А. и др. Ювенильные артриты: диагностика и лечение. МиД. 2017; 1: 48-61. [Igisheva L. N., Pritchina S. S., Bykova Yu. A., et al. Juvenile arthritis: diagnosis and treatment. MiD. 2017; 1: 48-61. (In Russ.)]
- Zhou J., Ding Y., Zhang Y., et al. CD3+CD56+ natural killer T cell activity in children with different forms of juvenile idiopathic arthritis and the influence of etanercept treatment on polyarticular subgroup. Clin Immunol. 2017; 176: 1-11. DOI: 10.1016/j.clim.2016.12.001.
- Ayaz N. A., Karadağ Ş. G., Çakmak F., et al. Leflunomide treatment in juvenile idiopathic arthritis. Rheumatol Int. 2019; 39 (9): 1615-1619. DOI: 10.1007/s00296-019-04385-7.
- Adrovic A., Yildiz M., Haslak F., et al. Tocilizumab therapy in juvenile systemic sclerosis: a retrospective single centre pilot study. Rheumatol Int. 2021; 41 (1): 121-128. DOI: 10.1007/s00296-020-04732-z.
- Баранов А. А., Алексеева Е. И., Валиева С. И. и др. Терапия генно-инженерными биологическими препаратами: эффективность и безопасность переключения. ВСП. 2014; 1. [Baranov A. A., Alekseeva E. I., Valieva S. I., et al. Therapy with genetically engineered biological drugs: efficiency and safety of switching. VSP. 2014; 1. (In Russ.)]
- Vanoni F., Minoia F., Malattia C. Biologics in juvenile idiopathic arthritis: a narrative review. Eur J Pediatr. 2017; 176 (9): 1147-1153. DOI: 10.1007/s00431-017-2960-6.
- Barut K., Adrovic A., Şahin S., et al. Juvenile Idiopathic Arthritis. Balkan Medical Journal. 2017; 34 (90). DOI: org/10.4274/balkanmedj.2017.0111.
- Brunner H. I., Nanda K., Toth M., et al. Safety and Effectiveness of Adalimumab in Patients With Polyarticular Course of Juvenile Idiopathic Arthritis: STRIVE Registry Seven-Year Interim Results. Arthritis Care Res (Hoboken). 2020; 72 (10): 1420-1430. DOI: 10.1002/acr.24044.
- Алексеева Е. И., Митенко Е. В., Валиева С. И. и др. Эффективность и безопасность терапии адалимумабом у детей с ювенильным идиопатическим артритом и увеитом. ВСП. 2012; 1. [Alekseeva E. I., Mitenko E. V., Valieva S. I., et al. Efficacy and safety of adalimumab therapy in children with juvenile idiopathic arthritis and uveitis. VSP. 2012; 1. (In Russ.)]
- Гайдар Е. В., Костик М. М., Дубко М. Ф. и др. Эффективность адалимумаба при хроническом переднем увеите, ассоциированном с ювенильным идиопатическим артритом и резистентным к терапии метотрексатом: ретроспективное исследование серии случаев. ПФ. 2016; 4: 340-344. [Gaidar E. V., Kostik M. M., Dubko M. F., et al. The effectiveness of adalimumab in chronic anterior uveitis associated with juvenile idiopathic arthritis and methotrexate resistant to therapy: a retrospective study of a series of cases. PF. 2016; 4: 340-344. (In Russ.)]
- Галстян Л. А., Жолобова Е. С., Старикова А. В. и др. Эффективность терапии абатацептом у пациентки с ювенильным идиопатическим артритом и двухсторонним увеитом. ВСП. 2016; 3: 307-310. [Galstyan L. A., Zholobova E. S., Starikova A. V., et al. The effectiveness of abatacept therapy in a patient with juvenile idiopathic arthritis and bilateral uveitis. VSP. 2016; 3: 307-310. (In Russ.)]
- Петри А., Сэбин К. Наглядная статистика в медицине. М.: ГЭОТАР-МЕД, 2020. 232 с. [Petri A., Sabin K. Visual statistics in medicine. Moscow: GEOTAR-MED, 2020. 232 p. (In Russ.)]
- Аксенов М. В., Пятых Е. А. Возможности использования генно-инженерных биологических препаратов в лечении ревматоидного артрита. Международный студенческий научный вестник. 2015; 2-3: 396-398. [Aksenov M. V., Pyatykh E. A. Possibilities of using genetically engineered biological preparations in the treatment of rheumatoid arthriti. Mezhdunarodnyi studencheskii nauchnyi vestnik. 2015; 2-3: 396-398. (In Russ.)]
- Давыдова М. А. Развитие и прогноз деструктивных изменений суставов у детей с ювенильным идиопатическим артритом. Вопросы практической педиатрии. 2017; 12 (3): 46-53. [Davydova M. A. Development and prognosis of destructive changes in the joints in children with juvenile idiopathic arthritis. Voprosy prakticheskoi pediatrii. 2017; 12 (3): 46-53. (In Russ.)]
- Давыдова М. А., Санталова Г. В., Стадлер Е. Р. и др. Динамика деструктивных изменений суставов при ювенильном идиопатическом артрите у детей, получавших метотрексат или комбинацию метотрексата и тоцилизумаба: результаты когортного исследования. Вопросы современной педиатрии. 2017; 16 (6): 502-508. [Davydova M. A., Santalova G. V., Stadler E. R., et al. Dynamics of destructive changes in the joints in juvenile idiopathic arthritis in children treated with methotrexate or a combination of methotrexate and tocilizumab: results of a cohort study. Voprosy prakticheskoi pediatrii. 2017; 16 (6): 502-508. (In Russ.)]
- Малиевский В. А., Нижевич А. А., Первушина Е. П. и др. Опыт применения адалимумаба у больной ювенильным артритом с увеитом на фоне болезни Крона. Вопросы современной педиатрии. 2013; 4 (12): 181-184. [Malievsky V. A., Nizhevich A. A., Pervushina E. P., et al. Experience with the use of adalimumab in a patient with juvenile arthritis with uveitis associated with Crohn's disease. Voprosy prakticheskoi pediatrii. 2013; 4 (12): 181-184. (In Russ.)]
Г. В. Санталова, https://orcid.org/0000-0002-6078-2361, g.v.santalova@samsmu.ru
Ю. В. Серёжкина, https://orcid.org/0000-0002-6505-999X, yuliana300800@gmail.com
О. В. Служаева, https://orcid.org/0000-0002-0193-6172, oks-samsmu@yandex.ru
Федеральное государственное бюджетное образовательное учреждение высшего образования Самарский государственный медицинский университет Министерства здравоохранения Российской Федерации; 443099, Россия, Самара, ул. Чапаевская, 89
Сведения об авторах:
Плахотникова Светлана Валентиновна, к.м.н., доцент, заведующая учебной частью кафедры факультетской педиатрии Федерального государственного бюджетного образовательного учреждения высшего образования Самарский государственный медицинский университет Министерства здравоохранения Российской Федерации; 443099, Россия, Самара, ул. Чапаевская, 89; s.v.plahotnikova@samsmu.ru
Санталова Галина Владимировна, д.м.н., профессор кафедры факультетской педиатрии Федерального государственного бюджетного образовательного учреждения высшего образования Самарский государственный медицинский университет Министерства здравоохранения Российской Федерации; 443099, Россия, Самара, ул. Чапаевская, 89; g.v.santalova@samsmu.ru
Сережкина Юлиана Васильевна, старший лаборант кафедры факультетской педиатрии Федерального государственного бюджетного образовательного учреждения высшего образования Самарский государственный медицинский университет Министерства здравоохранения Российской Федерации; 443099, Россия, Самара, ул. Чапаевская, 89;
Служаева Оксана Вячеславовна, старший лаборант кафедры факультетской педиатрии Федерального государственного бюджетного образовательного учреждения высшего образования Самарский государственный медицинский университет Министерства здравоохранения Российской Федерации; 443099, Россия, Самара, ул. Чапаевская, 89; oks-samsmu@yandex.ru
Information about the authors:
Svetlana V. Plakhotnikova, MD, Associate Professor, Head of Education of the Department of Faculty Pediatrics at the Federal State Budgetary Educational Institution of Higher Education Samara State Medical University of the Ministry of Health of the Russian Federation; 89 Chapaevskaya str., Samara, 443099, Russia; s.v.plahotnikova@samsmu.ru
Galina V. Santalova, Dr. of Sci. (Med.), Professor of the Department of Faculty Pediatrics at the Federal State Budgetary Educational Institution of Higher Education Samara State Medical University of the Ministry of Health of the Russian Federation; 89 Chapaevskaya str., Samara, 443099, Russia; g.v.santalova@samsmu.ru
Yuliana V. Serezhkina, Senior Laboratory Assistant, Department of Faculty Pediatrics at the Federal State Budgetary Educational Institution of Higher Education Samara State Medical University of the Ministry of Health of the Russian Federation; 89 Chapaevskaya str., Samara, 443099, Russia; yuliana300800@gmail.com
Oksana V. Sluzhaeva, Senior Laboratory Assistant, Department of Faculty Pediatrics at the Federal State Budgetary Educational Institution of Higher Education Samara State Medical University of the Ministry of Health of the Russian Federation; 89 Chapaevskaya str., Samara, 443099, Russia; oks-samsmu@yandex.ru
Опыт применения антицитокинового препарата адалимумаб у детей с полиартикулярным серонегативным юношеским артритом, проживающих в Самарском регионе/ С. В. Плахотникова, Г. В. Санталова, Ю. В. Серёжкина, О. В. Служаева
Для цитирования: Плахотникова С. В., Санталова Г. В., Серёжкина Ю. В., Служаева О. В. Опыт применения антицитокинового препарата адалимумаб у детей с полиартикулярным серонегативным юношеским артритом, проживающих в Самарском регионе. Лечащий Врач. 2023; 9 (26): 76-81. https://doi.org/10.51793/OS.2023.26.9.010
Теги: дети, ревматическое заболевание, увеит, артрит, энтезит
Купить номер с этой статьей в pdf