Микоплазменная инфекция является распространенным инфекционным заболеванием в человеческой популяции, характеризуется высокой частотой заболеваемости и особенностями течения в детском возрасте. Последнее требует привлечения внимания и углубления представлений об этой инфекции у педиатров, инфекционистов и врачей семейной медицины.
Несмотря на то, что объективных сведений об удельном весе микоплазмозов в России нет, любой практикующий врач амбулаторного или стационарного звена здравоохранения, особенно среди детского населения, с расширением диагностических лабораторных возможностей на этапе скринингового обследования больного, довольно часто сталкивается с микоплазменной инфекцией.
Основной вопрос, возникающий при интерпретации результатов обследования, — как расценивать инфекционный процесс с позиций его активности, необходимости выбора этиотропного препарата и оптимизации терапии.
Микоплазменная инфекция — острое зооантропонозное заболевание, вызываемое грамотрицательными бактериями, сопровождающееся различными воспалительными поражениями респираторного, урогенитального трактов, суставов, кроветворной и нервной систем, а при генерализации процесса — развитием ДВС-синдрома с поражением жизненно важных органов.
Первые сообщения о микоплазмах появились в конце XIX века, когда был выделен патогенный представитель семейства — возбудитель гнойной бычьей плевропневмонии Pleuropneumoniae organism. В отдельную группу микроорганизмов микоплазмы были выделены в 1898 г. и назывались плевропневмония-подобные организмы (ППО). В 1929 г. Е. Новаком предложено название этих патогенов — микоплазмы. Длительное время их относили к вирусам. В 1942 г. М. Д. Итон описал возбудителя «атипичной пневмонии», считая его вирусом, размером 180–250 нм, который пассировался при инокуляции на куриных эмбрионах. В 1961 г. B. Marmion и G. Goodborn высказали предположение о том, что агент Итона является микоплазмой. R. Chenock с соавт. в 1962 г. доказали микоплазменную природу агента Итона, выделив чистую культуру микоплазм на бесклеточной среде, и дали ей название
Микоплазмы лишены компонентов клеточной стенки Х-Е диаминопимелиновой кислоты и мукопептидного комплекса, что обусловливает их полиморфизм (кольца, гранулы, сферическая форма). Они способны к автономному росту и репродукции. Размеры их колеблются от 0,1 до 10 мк.
Колонии микоплазм разнообразны по своей форме и могут быть представлены многочисленными элементами: мелкими палочками, коккоподобными клетками, шаровидными телами, нитевидными и ветвистыми структурами разной длины. Благодаря разнообразию форм микоплазмы могут адсорбироваться на любых клетках эукариот (эритроцитах, реснитчатом эпителии бронхов, сперматозоидах и др.), размножаться на их поверхности и в межклеточных пространствах.
Микоплазмы покрыты трехслойной цитоплазматической мембраной. В их цитоплазме диффузно распределены нуклеиновые кислоты в виде нитей ДНК, РНК и рибосомы. С помощью актиноподобного белка микоплазмы прикрепляются к мембранам клеток. Эти патогены являются факультативными мембранными паразитами. Разнообразие микоплазм делает их схожими с вирусами (но в отличие от последних они способны к размножению на искусственных питательных средах), а по морфологии и клеточной организации микоплазмы сходны с L-формами бактерий. Возбудители выделяют экзотоксин, а в некоторых случаях и нейротоксин, оказывающие первичное токсическое действие на нервную и сердечно-сосудистую системы, повышая проницаемость гематоэнцефалического барьера. Микоплазмы окрашиваются по Романовскому нейтральным красным, акридином оранжевым, а также при ШИК-реакции [1].
В 1980 г. H. Brunnеr с соавт. воспроизведен был экспериментально респираторный микоплазмоз. Выделение микоплазм из половых путей человека послужило первым свидетельством того, что микроорганизмы данной группы способны паразитировать в организме человека, что повлекло за собой широкомасштабные исследования, в ходе которых было показано, что микоплазмы паразитируют в слизистых дыхательного тракта и мочеполовых путей. Еще в 1965 г. сообщалось о способности микоплазм вызывать в клетках хромосомные изменения, затрагивающие процессы размножения, иммуносупрессию и онкогенную трансформацию клеток при смешанных микоплазма-вирусных инфекциях [2].
Инфицированность населения микоплазмами колеблется от 9% до 70%. Доля микоплазменной инфекции среди заболеваний респираторного тракта по данным различных авторов колеблется от 4,9% до 67%. Отмечаются ежегодные сезонные подъемы заболеваемости в холодное время года, эпидемии повторяются каждые 3–5 лет. При эпидемических подъемах увеличивается число заболевших микоплазмозом до 20–40% к общему числу в структуре других респираторных инфекций. Обследование групп недоношенных и доношенных новорожденных свидетельствует о том, что в 53% проб сыворотки недоношенных и в 42% — доношенных новорожденных имеются антитела к микоплазме, что указывает на возможность трансплацентарной передачи антител, а также на то, что около 50% женщин к периоду беременности или во время таковой инфицированы микоплазмами. Широкое распространение урогенитальных микоплазм и их частое выявление у практически здоровых людей затрудняет решение вопроса о роли этих микроорганизмов в патогенезе заболеваний урогенитального тракта. С точки зрения одних исследователей они относятся к абсолютным патогенам, а других — к условно-патогенным микроорганизмам. С наибольшей частотой урогенитальный микоплазмоз регистрируется среди лиц с повышенной половой активностью, гонорее, трихомониазе, кандидамикозе, герпесе и, что немаловажно при беременности, — у 50% женщин с нарушениями репродуктивной функции.
О возможности внутриутробного инфицирования плода свидетельствуют данные о выделении микоплазм из амниотической жидкости, плаценты и крови плода при целостности плодных оболочек, а также о выделении уреаплазм у новорожденных, матерям которых родовспоможение осуществлялось путем кесарева сечения.
Внутриутробные микоплазмозы развиваются более чем у 20% детей. При этом варианте инфицирования развивается генерализованный патологический процесс с поражением органов дыхания и зрения плода, центральной нервной системы (ЦНС) и кожных покровов.
Недоношенные дети инфицированы микоплазмами в 3 раза чаще, чем доношенные. У них с высокой частотой развиваются легочные поражения — воспаление, сопровождающееся гиперреактивностью бронхов и инактивацией сурфактанта, перестройкой сосудов легких, способствуя развитию легочной гипертензии и гиперактивного воспалительного ответа на повреждение, вследствие хронической гипоксии, пневмонии или внутриутробной активации синтеза цитокинов. Частота врожденных пороков (чаще со стороны ЦНС) в группе мертворожденных детей и умерших новорожденных, инфицированных микоплазмами, составляет до 50%, что в 3 раза выше в сравнении с неинфицированными детьми. M. fermentans, M. hominis, M. pneumoniae, M. orale, M. salivarium способны вызывать у эмбриона хромосомные аберрации [3, 4].
По мнению ряда авторов распространенность микоплазмоза, половой путь передачи, неадекватность диагностических подходов и проводимой терапии могут привести к преобладанию последнего над классическими венерическими инфекциями.
Наиболее изученной в настоящее время является M. pneumoniaе, которая отличается от других представителей семейства микоплазм: 1) по гомологии нуклеиновых кислот; 2) в отличие от индигенной микоплазменной флоры человека, обладает способностью к гемадсорбции и гемолизу, вырабатывая гемолизин С2О2 — важнейший фактор патогенности; 3) продуцирует термостабильный митогенный фактор, являющийся мембранным белком — эндотоксической субстанцией. Повреждающее действие микоплазм на клетки обусловлено еще и слаботоксичными продуктами обмена — ионами аммония или перекисью водорода.
Микоплазмы растут на агаре с добавлением дрожжевого экстракта лошадиной сыворотки; способны размножаться в эпителиальных клетках куриного эмбриона, культурах клеток человека и животных; образуют очень мелкие колонии, размером до 1 мм, напоминающие «яичницу-глазунью». Микоплазмы размером от 100–600 нм, изменчивой формы, чувствительны к температурному воздействию, ультрафиолетовому облучению и действию дезинфицирующих средств.
M. pneumoniaе являются возбудителями респираторного микоплазмоза. В работах последних лет имеются сообщения о том, что они могут также обнаруживаться у женщин в содержимом цервикального канала и у их половых партнеров, что свидетельствует о половом или оральном пути передачи инфекции.
M. incognitis являются причиной малоизученного генерализованного инфекционного процесса.
M. fermentans и M. penetrans — по данным исследований последних лет играют роль в развитии СПИДа.
M. hominis, M. genitalium, M. urealiticum — являются возбудителями урогенитального микоплазмоза; обнаруживаются у женщин при спонтанных абортах, вызывая аномалии развития плода.
M. orale, M. salivarium, выделяемые из полости рта, вызывают периодонтиты, пульпиты, стоматиты, хронические остеомиелиты, а M. fermentans, M. artritidis — заболевания суставов.
В основе патогенетического действия микоплазм лежат уникальные свойства мембранных паразитов. Фактором патогенности микоплазм является способность их мембран к тесному слиянию с мембраной клеток хозяина с помощью особых концевых структур липопротеиновой природы, взаимодействующих с клетками макроорганизма. Липидные компоненты мембран микоплазм диффундируют в мембрану клетки, а холестерин клетки макроорганизма поступает в мембрану микоплазм. При этом нарушается движение ресничек мерцательного эпителия, изменяется физиология клеток и архитектоника их мембран. В клетках хозяина они могут длительно персистировать, размножаться не только внеклеточно, но и внутриклеточно, нарушать нормальные регуляторные механизмы стволовых, иммунокомпетентных и других клеток. Биологические свойства микоплазм препятствуют либо фагоцитозу, либо перевариванию их в фагоцитах. В тех случаях, когда микоплазмы не перевариваются фагоцитами, последние становятся разносчиками инфекции, содействуя ее генерализации.
Прикрепляясь к эритроцитам, микоплазмы вызывают их гемолиз, что может сопровождаться нарушением микроциркуляции, васкулитом и образованием тромбов. Закупорка кровеносных и лимфатических сосудов приводит к усилению экссудации пораженных органов, образованию очагов некроза, развитию местного иммунного воспаления.
Микоплазмы вначале проявляют цитотоксический эффект, что активизирует систему комплемента, за этим следует иммунокомплексный процесс, а через 5–6 недель развиваются аутоиммунные механизмы.
Адсорбция их на лимфоцитах приводит к неспецифической поликлональной активации Т- и В-клеток с последующим развитием аутоиммунных реакций или к подавлению пролиферации этих клеток с развитием иммуносупрессии. Все 3 механизма: цитотоксический, иммунокомплексный и антителообразования действуют параллельно в острой фазе заболевания. Ярким проявлением аутоиммунных реакций при этой инфекции является развитие бронхиальной астмы, микоплазменного слизисто-кожного синдрома Стивенса–Джонсона [5, 6].
При хронизации процесса на фоне персистенции микоплазм доминирующим является антительный механизм на фоне сохраняющегося иммунокомплексного процесса и угнетения клеточного звена иммунитета.
При респираторном микоплазмозе общепризнанным является капельно-аспирационный путь заражения. Инкубационный период в среднем длится 7–14 дней, но может составлять от 4 до 25 дней. Микоплазмоз у детей проявляется в виде поражения бронхолегочного тракта, при котором воспалительным процессом охвачены носоглотка и бронхи. У детей с астмой количество приступов на фоне микоплазмоза значительно увеличивается и протекает в более тяжелой форме. Основным симптомом микоплазмоза, по которому можно заподозрить данную этиологию у ребенка, является длительный кашель (более 2 недель), не поддающийся традиционным методам терапии.
У детей старшего возраста респираторное заболевание начинается остро, с быстрым развитием интоксикации, лихорадки до 38–40 °С. Состояние улучшается к 5–8 дню заболевания, но в дальнейшем может отмечаться вялая динамика симптомов с длительным субфебрилитетом, как правило, до 3–4 недель [7].
При поражении верхних дыхательных путей слабо или умеренно выражены явления назофарингита, сухой навязчивый кашель, боль в горле, неловкость при глотании. Могут развиться симптомы стенозирующего ларинготрахеита.
Часто бронхи вовлекаются в воспалительный процесс, в легких выслушиваются сухие хрипы. При рентгенологическом исследовании определяется интерстициальный характер легочных изменений с усилением сосудистого и бронхиального рисунка. Бронхит нередко имеет тенденцию к затяжному течению [8].
Для микоплазменной пневмонии характерен более длительный инкубационный период (15–40 дней), выраженность симптомов интоксикации: анорексия, повторная рвота, головная боль, гипертермия. В отличие от взрослых, у которых нередко наблюдаются «немые пневмонии», у детей перкуторно и аускультативно выявляются характерные для пневмонии укорочение перкуторного звука и ослабление дыхания в локусе поражения легочной ткани. Выслушиваются сухие и разнокалиберные влажные хрипы. Кашель сухой, упорный, носит коклюшеподобный характер. Физикальные изменения носят затяжной и по интенсивности волнообразный характер на фоне сохраняющегося стабильно субфебрилитета. Явления кислородной недостаточности при этой пневмонии слабо выражены.
Рентгенологическая картина по распространенности очагов поражения разнообразна. Чаще на фоне изменений в прикорневых зонах отмечается понижение прозрачности, смазанность структуры с усилением сосудистого компонента легочного рисунка. При этом на всем протяжении легочных полей определяются немногочисленные очаговые тени. Реже наблюдаются массивные сегментарные и полисегментарные пневмонии, сопровождающиеся значительными проявлениями токсикоза и болями в боку [9].
Интерстициальная пневмония при микоплазмозе встречается чаще у детей старшего возраста.
На фоне поражения органов дыхания при микоплазменной инфекции имеют место внереспираторные симптомы, проявляющиеся артралгиями в области крупных суставов, мелкопятнистой сыпью, полиморфной эритемой, лимфаденопатией, гепатоспленомегалией. В показателях периферической крови характерными являются умеренно выраженный лейкоцитоз, нейтрофилез со сдвигом лейкоцитарной формулы влево, ускорение СОЭ, которые могут сохраняться до 3–4 недель болезни.
При M. pneumoniae может развиться серозный менингит или поражение вещества головного мозга одновременно с поражением респираторного тракта или предшествовать пневмонии [10, 11].
Поражение почек при микоплазмозе характеризуется изменениями в эпителии почечных канальцев и в клубочковом аппарате по типу умеренно выраженного мембранозно-пролиферативного гломерулонефрита, что клинически выражается умеренной гематурией и протеинурией с относительно легким течением.
Возможна манифестация M. pneumoniae с развития гепатита с синдромом холестаза.
При развитии врожденного микоплазмоза у новорожденных выделяют детей, инфицированных антенатально или интранатально, в том числе заразившихся в первые дни жизни.
При анте- или интранатальном заражении микоплазмоз имеет все признаки генерализованного процесса с поражением различных систем и органов: печени, почек, легких и ЦНС.
Ведущими клиническими синдромами врожденного микоплазмоза являются: прогрессирующая гидроцефалия на первой неделе жизни; нарастающие симптомы дыхательной и сердечно-сосудистой недостаточности по правожелудочковому типу, геморрагический синдром с пенисто-кровянистыми выделениями изо рта, кровотечениями и кровоизлияниями во внутренние органы.
При инфицировании новорожденных в первые дни жизни наиболее выраженные изменения имеют место в респираторном тракте, особенно у недоношенных детей. Кроме того, характерны конъюнктивиты, поражения кожи в виде абсцессов и некрозов, вульвиты, кардиопатии, тяжелые поражения ЦНС с последующим развитием гидроцефалии.
При хроническом течении уреаплазменной инфекции нередко имеет место летальный исход у недоношенных детей с малой массой тела при рождении, что является следствием слабой воспалительной и иммунной реакций.
При подозрении на респираторный микоплазмоз используют мазки из носоглотки, мокроту, лаважную жидкость, бронхиальные смывы, а при патологоанатомическом исследовании — мазки-отпечатки тканей и органов.
В педиатрии культуральные методы применяются редко. Недостатком их является низкая чувствительность, из-за неадекватности питательных сред, неспособности некоторых штаммов микоплазм расти в отсутствие живых клеток, а также длительности культивирования.
В настоящее время практически утратили свою актуальность широко использовавшиеся в прежние годы для верификации микоплазмоза такие реакции, как реакция иммунофлюоресценции (РИФ), реакция связывания комплимента (РСК) и реакция непрямой гемагглютинации (РНГА).
Лабораторная диагностика респираторного микоплазмоза считается оптимальной, если используется комбинация методов, направленных на выявление в исследуемых материалах антигенов возбудителя методами иммуноферментного анализа (ИФА) и реакция агрегатгемагглютинации (РАГА) или его генома при помощи полимеразной цепной реакции (ПЦР) [12, 13].
Определение специфического антигена проводят в РАГА — диагностический титр 1:8 или 0,001–0,0001 мкг/мл по белку.
К наиболее чувствительным методам обнаружения антител к микоплазмам относят реакцию пассивной гемагглютинации (РПГА) (диагностический титр 1:32), ИФА и реакцию непрямой иммунофлюоресценции (РНИФ), в которых обнаруживают антитела классов IgM и IgG [1].
В современных условиях для диагностики этой инфекции используется ПЦР, чувствительность и специфичность которой оценивается в пределах 92–98%. Применение ПЦР возможно для определения антигена микоплазмы в мазках при местном воспалительном процессе. Полимеразная цепная реакция имеет ряд преимуществ перед серодиагностикой, однако высокая стоимость этого теста не позволяет широко использовать его в практическом здравоохранении.
При остром начале и выраженной интоксикации микоплазмоз дифференцируют с гриппом. В отличие от него, интоксикация при микоплазменной инфекции носит затяжной характер с максимумом ее нарастания после 4–5 дня болезни. При распространении процесса на нижние дыхательные пути дифференцируют микоплазмоз с РС-инфекцией, коклюшем, пневмонической формой орнитоза и с острыми пневмониями другой этиологии.
Диагностика микоплазменной инфекции сложна из-за полиморфизма клинических симптомов, поэтому большое значение в первую очередь придается результатам лабораторной диагностики.
Терапии подлежат все пациенты, у которых микоплазменная инфекция была диагностирована одним из перечисленных ранее чувствительных методов. Лечение заболевания должно быть комплексным, с учетом другой патологии, помимо поражения респираторной системы, сопутствующей микрофлоры, а также дисфункции иммунной системы со стойкой депрессией клеточного звена иммунитета.
Основной задачей применения этиотропной терапии является не только ликвидация клинической симптоматики, а вероятность эрадикации возбудителя из очага инфекции и ликвидация персистенции. Если не достигается эрадикация, то возможна хронизация инфекции и рецидивы, вызываемые уже резистентными штаммами микроорганизмов [14, 15].
Этиотропная терапия микоплазмоза включает наиболее эффективные на современном этапе антибактериальные препараты из группы макролидов и азалидов, к которым наиболее чувствительны микоплазмы, при применении в оптимальных дозах: азитромицин (внутрь 10 мг/кг однократно в сутки), джозамицин (внутрь 30–50 мг/кг в 3 приема в сутки), кларитромицин (внутрь 7,5–15 мг/кг в 2 приема в сутки), рокситромицин (внутрь 5–8 мг/кг в 2 приема в сутки), клиндамицин (внутрь 10–25 мг/кг в 3 приема в сутки или в/в, в/м 20–40 мг/кг в сутки, не более 3 г/сутки), мидекамицин (внутрь 30–50 мг/кг в 2–3 приема в сутки). Продолжительность антибиотикотерапии зависит от тяжести и остроты болезни и составляет от 7 до 21 дня [16].
В патогенетической терапии важное значение придается коррекции функциональных нарушений со стороны бронхолегочной и сердечно-сосудистой систем. С целью дезинтоксикации при среднетяжелых формах назначают обильное питье; при тяжелых формах — в/в капельные инфузии коллоидных и глюкозосолевых растворов.
Применяются поливитамины, витаминно-минеральные комплексы, препараты метаболической терапии и гепатопротекторы, в том числе Актовегин, Рибоксин, Кокарбоксилаза, Хофитол, Лив.52 и др. По показаниям — глюкокортикоиды (преднизолон 2–3 мг/кг), ингибиторы протеаз (Контрикал, Гордокс), антиагреганты (циннаризин, кавинтон и др.), нестероидные противовоспалительные препараты (ибупрофен, индометацин, диклофенак и др.).
В симптоматической терапии назначают жаропонижающие, сердечные гликозиды и др., муколитики, отхаркивающие препараты (амброксол, бромгексин, Мукалтин, корень солодки и др.). При развитии бронхообструкции назначаются β-агонисты и ингаляционные кортикостероиды.
С целью иммунокоррекции назначаются иммуномодуляторы в зависимости от изменений в показателях иммунограммы (Тималин, Т-активин, Тимоген, Имунофан, Полиоксидоний, Ликопид, Деринат и др.), а также препараты интерферона (Виферон, Кипферон, Реаферон и др.) или его индукторы (Циклоферон, Амиксин, Арбидол, Анаферон и др.) [17].
В течение 4 лет (2013–2016 гг.) под нашим наблюдением находилось 52 больных в возрасте от 5 мес до 17 лет, из них 22 больных — в инфекционных боксированных отделениях, а амбулаторно обследовано 20 больных в условиях консультативно-диагностического центра Морозовской детской клинической больницы г. Москвы, а также 10 детей — амбулаторно в многопрофильной клинике Vessel Clinic, у которых диагностировали различные клинические формы микоплазмоза.
В составе больных преобладали девочки — 33 и 19 мальчиков, среди которых в возрасте до 3 лет было — 8; от 4 до 7 лет — 14; от 8 до 14 лет — 24 и старше 14 лет — 6 детей.
В этиологической структуре микоплазмоза у обследованных больных методами ИФА и РАГА верифицировались: 1) у 33 детей моноинфекция: M. pneumoniae — у 26 (из них антигенемия регистрировалась у 8 и IgM — у всех 26 детей); у всех детей с пневмонией методом ПЦР в назофарингеальных мазках и индуцированной мокроте была выделена M. pneumoniae, а серологическим методом — регистрировалось повышение титра антител класса IgM; у 6 из 17 детей с микоплазменной пневмонией в индуцированной мокроте были обнаружены: Streptococcus viridans + Candida albicans (у 2), Candida albicans (у 2), Staphylococcus epidermidis (у 1), Staphylococcus epidermidis + Streptococcus viridans (у 1). M. hominis верифицировалась у 7 детей (антигенемия — у 5; IgM — у 2 детей); 2) микст-инфекция диагностирована у 19 больных: IgM к M. pneumoniae + C. pneumoniae — у 3; антигены у 8 и IgM — у 2 к M. pneumoniae + M. hominis; антигены у 4 и IgM — у 2 к M. pneumoniae + M. hominis + M. urealytica + M. arthritis + M. fermentans.
У 27 детей микоплазмоз протекал на фоне активно персистирующей герпесвирусной инфекции, в спектре которой ЭБВ-инфекция регистрировалась у 8 детей (у всех больных обнаруживалась антигенемия на фоне диагностически значимого титра антител); ЦМВИ диагностирована у 5 детей (у 2 — с антигенемией и у всех — выявлялся диагностически значимый титр антител); ВГЧ 6-го типа был выявлен у 11 детей (у всех обнаруживались антигены в мононуклеарных клетках крови + антитела в диагностическом титре) и у 3 детей регистрировалась инфекция простого герпеса (при диагностически значимом титре антител).
У 11 детей диагностировали риносинусит, из них у 8 больных сочетавшийся с аденоидитом и тонзиллофарингитом и у 3 детей — с острым гнойным средним отитом.
У 19 детей диагностировали бронхит, среди которых преобладали дети до 5 лет жизни, из них у 5 выражены были признаки бронхообструкции с рентгенологическими признаками эмфизематозного изменения легких.
Среди 17 детей с микоплазменной пневмонией преобладали дети школьного возраста (82,35%), чаще болели девочки. Все дети поступали в стационар в конце второй недели заболевания. Заболевание развивалось остро, температура тела в первые двое суток повышалась до 38–39 °С у 11 детей (64,7%). У 2 из них на фоне фебрильной температуры отмечалась рвота. У 6 из 17 детей с первых дней отмечалась субфебрильная температура тела, которая держалась в течение недели. У всех детей был коклюшеподобный сухой, мучительный малопродуктивный кашель. До поступления в стационар дети наблюдались амбулаторно, где получали антибиотики пенициллинового ряда на 3–4 день от начала заболевания. На момент поступления в стационар состояние этих детей оценивалось как среднетяжелое, у 9 из 17 больных наблюдалась вторая волна повышения температуры до фебрильных цифр (38–39 °С), сменившаяся длительным субфебрилитетом. У остальных детей температура при поступлении была 37–37,8 °С. Из симптомов интоксикации отмечались головная боль у 10 из 17 и слабость у 13 из 17 детей. Носовое дыхание было затруднено у 12 из 17 детей. К концу второй недели кашель оставался малопродуктивным. При перкуссии легких у всех обследованных детей наблюдалось укорочение перкуторного звука. При аускультации в половине случаев (у 9 детей) выслушивались влажные мелкопузырчатые хрипы, в остальных случаях — сухие и влажные (у 3), сухие (у 1) и крепитирующие (у 2 детей); хрипы не выслушивались у только у 2 детей. Течение заболевания у всех детей было затяжным, с длительно сохранявшимся субфебрилитетом и мучительным сухим кашлем.
В клиническом анализе крови только у 3 из 17 детей отмечался лейкоцитоз с лейкоцитарным сдвигом влево и ускорение СОЭ, у остальных детей показатели анализа крови были в пределах нормы.
Особенностью рентгенологической картины легких были инфильтративные очаги с тенденцией к слиянию, локализация очагов выявлялась как в верхних, так и в нижних долях (рис.). Очаговые тени имели нечеткие края и размытость. Наблюдалось усиление легочного рисунка. Рентгенологические изменения сохранялись в течение 8–9 суток с момента поступления. При повторной рентгенограмме очагов воспаления не наблюдалось, но сохранялось усиление легочного рисунка.
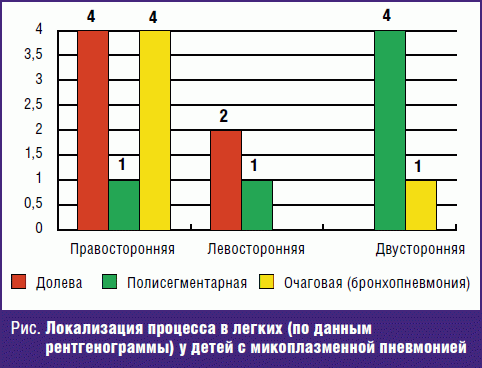
Осложненное течение заболевания отмечалось у 4 детей в виде острого катарального отита, бронхообструктивного синдрома и реактивного панкреатита.
Исход заболевания у всех детей с подтвержденной микоплазменной пневмонией был благоприятный: выздоровление наступало через 8–18 суток с момента поступления в стационар.
Экстрареспираторные проявления микоплазмоза отмечены у 8 детей, у которых сопутствовала смешанная активно персистирующая герпесвирусная инфекция, из них у 2 была инфекция мочевыводящих путей (пиелонефрит), у 2 — синдром Стивенса–Джонсона; у 1 ребенка имел место мезоаденит, сопровождавшийся артралгиями; у 1 был иммунный тиреоидит, у 1 — иммунная нейтропения и у 1 — иммунная тромбоцитопения.
Явления васкулита при моноинфекции M. hominis регистрировались у 4 детей в виде папулезной сыпи с геморрагическим пропитыванием на фоне тонзиллофарингита. Длительный субфебрилитет регистрировался у 14 детей, из них — у 9 отмечались жалобы на головную боль, астению, снижение качества успеваемости; у остальных 5 больных раннего возраста в акушерском анамнезе жизни имелись указания на микоплазмоз у матерей, перинатальную энцефалопатию, у которых при дуплексном сканировании сосудов головы и шеи выявлялись ЭХО-признаки затруднения венозного оттока или ангиоспазма артерий Виллизиева круга, при явном уплотнении комплекса интима-медиа (КИМ) сосудов, что косвенно указывало на эндотелиальную дисфункцию, развившуюся, вероятнее всего, в результате воздействия на сосудистый эндотелий непосредственно микоплазм, ответных цитотоксических реакций и вследствие этого на клинически выраженную внутречерепную гипертензию.
У детей с микоплазмозом, протекавшим с сопутствующей активно персистирующей герпесвирусной инфекцией, применяли терапию, в составе которой использовали противогерпетические препараты — ацикловир, НеоЦитотект и другие в сочетании с препаратами интерферона α-2β и индукторами интерферона.
У больных с синдромом Стивенса–Джонсона и васкулитом на фоне этиотропной терапии применялись короткие курсы глюкокортикоидной терапии и препараты, улучшающие микроциркуляцию в сосудистом русле. Всем больным с тяжелой формой микоплазмоза проводилась посиндромная инфузионная и дезинтоксикационная терапия.
В заключение можно утверждать, что микоплазменная инфекция сопровождается у детей длительной антигенемией, обусловливающей рецидивы заболевания и аутоиммунизацию.
Микоплазмоз более чем у 50% больных детей протекает на фоне иммуносупрессирующей активно персистирующей герпесвирусной инфекции, о чем свидетельствуют наши исследования, согласующиеся с данными литературы.
Вышеуказанное является обоснованием для оптимизации этиотропной и патогенетической терапии микоплазмоза, направленной на коррекцию существенных нарушений в иммунной резистентности организма и эндотелиальной дисфункции у детей, страдающих микоплазмозом.
Литература
- Прозоровский С. В., Раковская И. В., Вульфович Ю. В. Медицинская микоплазмология. М., 1995. 287, с. 9.
- Покровский В. И., Прозоровский С. В. Новые аспекты инфекционной пульмонологии. В кн.: Эпидемиология и инфекционная патология. М., 1989. С. 12–13.
- Цинзерлинг А. В., Вуду Г. А. Внутриутробный микоплазмоз. Кишинев, 1986.
- Мальцева Л. И., Капелюшник Н. Л., Зефирова Т. П. и др. Механизмы развития осложнений беременности и перинатальных повреждений плода при микоплазменной инфекции // Журн. акушерства и женских болезней. 1998. Спец. вып. С. 138.
- Esposito S., Principi N. Asthma in children: are Chlamydia or Mycoplasma involved. Pediatr. Drugs., 2001, 3: 159–168.
- Nicolson G. L., Marwan Ph. D., Nasralla Y. et al. Mycoplasmal Infections in Chronic Illnesses // Med. Sent. 1999, № 5. Vol. 4: 172–175.
- Цинзерлинг А. В. Заболевания, вызываемые микроорганизмами семейства Mycoplasmatiaceae. В кн.: Современные инфекции. Патологическая анатомия и вопросы патогенеза. СПб: Сотис, 1993. С. 222–228.
- Чешик С. Г., Линкова С. А., Афанасьева В. А. и др. Клинико-рентгенологическая характеристика бронхолегочного микоплазмоза у детей // Педиатрия. 1987. № 1. С. 34–39.
- Клембовский А. И. Микоплазменная пневмония. Морфологическая характеристика и особенности патогенеза острого воспаления легких у детей. В кн.: Пневмонии у детей / Под ред. С. Ю. Каганова, Ю. Е. Вельтищева. М.: Медицина, 1985. С. 83–85.
- Bruch L. A., Jefferson R. J., Pike M. G. et al. Mycoplasma pneumoniae infection, menin goencephalitis, and hemophagocytosis // Pediatr. Neurol. 2001. V. 25. № 1. P. 67–70.
- Denny F. W., Clyde W. A., Glezen W. P. Mycoplasma pneumoniae disease: Clinical spectrum, pathophysiology, epidemiology and control // J. Infect. Dis., 1971, 123: 74.
- Медицинская микробиология / Под ред. В. И. Покровского, О. К. Поздеева. М.: Гэотар Медицина, 1999.
- Раковская И. В. Микоплазмы и микоплазмозы человека. Рук-во для врачей. М., 1999.
- Чемоданов В. В. Новая эра — новые стандарты назначения антибиотиков // Практика педиатра. 2004, декабрь, с. 18–21.
- Таточенко В. К. Антибиотики при острых респираторных заболеваниях у детей // Consilium medicum. 2004, приложение № 1. С. 3–6.
- Страчунский Л. С., Козлов С. Н. Макролиды в современной клинической практике. Смоленск: Русич, 1998. 304 с.
- Таточенко В. К. Практическая пульмонология детского возраста. М., 2001. 268 с. 13.
Ф. С. Харламова*, 1, доктор медицинских наук, профессор
О. В. Шамшева*, доктор медицинских наук, профессор
Д. А. Воробьева*
Ю. В. Романова**
Н. Л. Вальтц**
А. В. Денисова***
* ГБОУ ВПО РНИМУ им. Н. И. Пирогова МЗ РФ, Москва
** ГБУЗ Морозовская ДГКБ ДЗМ, Москва
*** Многопрофильная клиника Vessel Clinic, Москва
1 Контактная информация: kharlamova47@bk.ru
Купить номер с этой статьей в pdf