Артериальная гипертензия (АГ), являясь одним из основных факторов риска (ФР) развития сердечно-сосудистых заболеваний, вносит наибольший вклад в сердечно-сосудистую заболеваемость и смертность, поскольку является весьма распространенным заболеванием (в России АГ страдает около 40% взрослого населения).
При длительно существующей и плохо леченной АГ высок риск развития инфаркта миокарда (ИМ), мозгового инсульта, хронической сердечной недостаточности, нарушений ритма, внезапной сердечной смерти. Эффективная антигипертензивная терапия способна в значительной степени снизить частоту развития сердечно-сосудистых осложнений и сердечно-сосудистую смертность, что и является основной целью лечения больных АГ. Для достижения этой цели требуется не только снижение артериального давления (АД) до целевого уровня, но и коррекция всех модифицируемых факторов риска (курения, дислипидемии и пр.), предупреждение и/или регресс поражения органов-мишеней (сердце, почки, сосуды), а также лечение ассоциированных с АГ и сопутствующих заболеваний (рис. 1) [1].
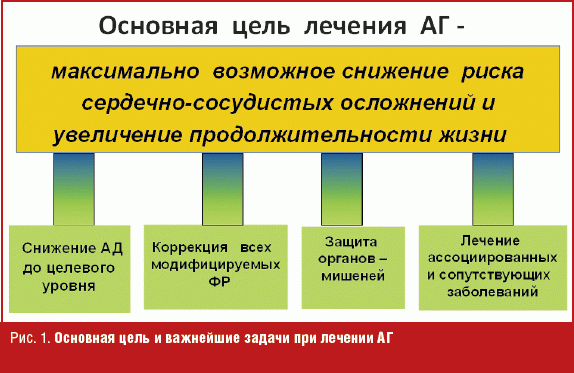
Ингибиторы ангиотензинпревращающего фермента (ИАПФ) на протяжении многих лет занимают место среди пяти основных классов антигипертензивных препаратов, назначение которых четко регламентировано в Российских рекомендациях по диагностике и лечению АГ в зависимости от сопутствующих заболеваний и состояний.
Наиболее широк перечень показаний к применению ИАПФ и блокаторов рецепторов ангиотензина II (БРА), снижающих активность ренин-ангиотензиновой системы (РАС). ИАПФ, снижая активность ключевого фермента, ответственного за образование ангиотензина II, являющегося мощным вазоконстриктором, стимулирующего секрецию альдостерона и пролиферацию гладкомышечных клеток, приводят к вазодилатации, мягкому диуретическому эффекту, оказывают калийсберегающее действие.
При длительном применении ИАПФ уменьшают выраженность гипертрофии миокарда левого желудочка (ЛЖ) и сосудистой стенки, уменьшают внутриклубочковую гипертензию, оказывают антипротеинурическое действие, снижают риск развития почечной недостаточности. К достоинствам ИАПФ помимо высокой антигипертензивной эффективности относятся метаболическая нейтральность, мощное органопротективное действие (кардио-, нефро- и ангипротективное), хорошая переносимость.
ИАПФ не только являются высокоэффективными, хорошо переносимыми антигипертензивными препаратами с доказанным органопротективным эффектом, они способны снизить частоту сердечно-сосудистых осложнений и увеличить продолжительность жизни больных АГ (исследования CAPPP, HOPE, INVEST, ANBP 2).
Именно ИАПФ следует отдавать предпочтение у больных АГ с дисфункцией ЛЖ (не говоря уже о наличии клинически выраженных проявлений недостаточности кровообращения). Выбор в пользу ИАПФ должен быть сделан при наличии гипертрофии левого желудочка (ГЛЖ), поскольку данные препараты наряду с сартанами являются наиболее эффективными в отношении регресса ГЛЖ.
У больных сахарным диабетом (СД) и АГ ИАПФ являются препаратами выбора, предотвращая развитие диабетической нефропатии либо замедляя ее прогрессирование. Еще более важным представляется их способность предотвращать сердечно-сосудистые осложнения и улучшать прогноз у этих больных.
И еще один важный аспект: нередко ИАПФ могут быть назначены в ситуациях, когда противопоказаны другие антигипертензивные препараты. ИАПФ можно назначать при обструктивных заболеваниях легких (хроническая обструктивная болезнь легких (ХОБЛ)), перемежающейся хромоте, СД 1-го типа, подагре, тяжелой хронической сердечной недостаточности (ХСН), нарушениях атрио-вентрикулярной проводимости. К применению же ИАПФ существует очень небольшое количество абсолютных противопоказаний (беременность, стеноз почечных артерий, тяжелая почечная недостаточность, ангионевротический отек в анамнезе, вызванный ИАПФ).
В настоящее время в России зарегистрировано около полутора десятков ИАПФ, отличающихся друг от друга по химическому строению, прочности связывания АПФ, действующих непосредственно или путем образования активного метаболита (большинство ИАПФ являются пролекарствами), длительности действия, путям экскреции.
В отличие от большинства других ИАПФ, являющихся пролекарствами, лизиноприл не подвергается биотрансформации в печени, то есть является активным лекарством и действует без образования активного метаболита. После приема внутрь лизиноприл быстро всасывается, прием пищи не влияет на абсорбцию лизиноприла. Пик концентрации в крови достигается через 6 ч после приема препарата. Лизиноприл практически не связывается с белками плазмы, что означает отсутствие лекарственного взаимодействия с препаратами, способными вытеснять лекарства из связи с белком (нестероидные противовоспалительные препараты, амиодарон и др.). Лизиноприл экскретируется в неизмененном виде с мочой. Клиренс лизиноприла коррелирует с клиренсом креатинина, поэтому параллельно с возрастными изменениями выделительной функции почек изменяется и скорость выведения препарата из организма, как правило, у больных пожилого возраста коррекция дозы не требуется [2], но при тяжелой хронической почечной недостаточности (клиренс креатинина менее 30 мл/мин) может потребоваться уменьшение дозы лизиноприла.
Лизиноприл не оказывает негативного влияния на содержание глюкозы, мочевой кислоты крови, липидный спектр. Существуют сведения о благоприятном влиянии лизиноприла в отношении чувствительности тканей к инсулину, уровня глюкозы натощак и постпрандиально (рис. 2) [3, 4].
Артериальная гипертензия
Исследования суточного профиля АД подтвердили сохранение антигипертензивного эффекта лизиноприла в ранние утренние часы. Поскольку максимальный эффект развивается через 6 ч после приема лизиноприла, для предотвращения утреннего подъема АД (время сердечно-сосудистых катастроф), препарат следует назначать вечером перед сном [5].
При монотерапии хороший клинический эффект наблюдается у 50–80% больных с АГ 1–2 степени. В многочисленных исследованиях (ALLHAT, TROPHY, STOP-2, HOT и др.) было показано, что лизиноприл не уступает по эффективности другим ингибиторам АПФ, в том числе эналаприлу [6], тиазидным диуретикам (гидрохлоротиазид), бета-адреноблокаторам (метопролол, небиволол) [7], антагонистам кальция (амлодипин, верапамил ретард, нифедипин ретард, фелодипин ретард), БРА (телмисартан [8], вальсартан [9]).
В исследовании ALLHAT [10] оценивалась смертность от ИБС и частота инфарктов миокарда у пациентов старше 55 лет, страдающих АГ и получавших хлорталидон в дозе 12,5–25 мг (15255 больных), амлодипин в дозе 2,5–10 мг (9048 больных), доксазозин (9061 больной) и лизиноприл в дозе 10–40 мг в сутки (9054 пациента). Если целевого уровня АД достигнуть не удавалось, добавляли второй препарат (атенолол — 25–100 мг, резерпин — 0,05–0,2 мг однократно в сутки или клонидин — 0,1–0,3 мг два раза в сутки). Третьим препаратом был гидралазин (25–100 мг два раза в сутки). Исследование в группе доксазозина было остановлено уже через 3,2 года после начала лечения в связи с достоверным повышением риска сердечно-сосудистых осложнений. По способности предотвращать наступление первичной комбинированной конечной точки (инфаркт миокарда и сердечно-сосудистая смерть) не было показано преимуществ ни одного из этих трех лекарственных препаратов. Лизиноприл оказался значительно эффективнее амлодипина в отношении профилактики развития сердечной недостаточности. Следует также отметить, что лизиноприл эффективно предотвращал возникновение новых случаев СД 2-го типа [11]. Частота новых случаев СД через 2 года терапии оказалась почти в 2 раза выше в группе хлорталидона.
Гипертрофия левого желудочка
ГЛЖ является независимым фактором риска у больных АГ. В исследовании SAMPLE была подтверждена способность лизиноприла вызывать регресс ГЛЖ: индекс массы миокарда ЛЖ уменьшался на 15,8% при лечении лизиноприлом в дозе 20 мг/сутки [12]. Наряду с регрессией ГЛЖ лизиноприл приводил к улучшению систолической и диастолической функции ЛЖ. Rizzoni и соавт. уже через год лечения лизиноприлом обнаружили достоверную регрессию гипертрофии миокарда ЛЖ. Через три года лечения уменьшение ГЛЖ стало еще более выраженным (рис. 3), уменьшилось соотношение толщины медии артерии к диаметру ее просвета, улучшилась эндотелийзависимая релаксация сосудов [13].
Позднее в исследовании ELVERA было также отмечено достоверное уменьшение индекса массы миокарда при назначении лизиноприла у пожилых больных АГ [14].
В клинической практике все чаще встречаются пациенты с АГ и коморбидными состояниями (ожирение, сахарный диабет, ХОБЛ, подагра, заболевания печени); эти заболевания и состояния могут как ограничивать, так и диктовать выбор конкретного противогипертензивного препарата.
Заболевания почек
Подобно другим ИАПФ, лизиноприл уменьшает альбуминурию, почечно-сосудистое сопротивление, увеличивает почечный кровоток и скорость клубочковой фильтрации, причем нефропротективное действие лизиноприла не связано с его антигипертензивным эффектом.
Лизиноприл относится к числу немногих ИАПФ, эффективность которых хорошо изучена у больных с СД 1-го и 2-го типа. В многоцентровом плацебо-контролируемом исследовании EUCLID было изучено влияние лизиноприла на развитие и прогрессирование диабетической нефропатии и ретинопатии у 530 больных СД 2-го типа без АГ [15]. Через 2 года уровень микроальбуминурии в группе лизиноприла оказался на 18,8% ниже по сравнению с группой плацебо. Особенно выраженным был эффект лизиноприла у больных с микроальбуминурией в начале исследования: у них снижение экскреции альбумина с мочой составило 49,7%, в то время как у пациентов с исходной нормоальбуминурией снижение экскреции альбумина с мочой по сравнению с плацебо составило 12,7%. Кроме того в группе лизиноприла было выявлено снижение риска прогрессирования диабетической ретинопатии на 50% по сравнению с группой плацебо, при этом максимальный протективный эффект лизиноприла в отношении развития и прогрессирования диабетической ретинопатии был отмечен у пациентов с компенсированным СД (при уровне гликированного гемоглобина < 7%).
Еще в одном крупном исследовании (3463 больных СД 2-го типа с диабетической нефропатией и АГ) через 3 мес после назначения лизиноприла помимо снижения АД было отмечено улучшение азотвыделительной функции (почти у 50% больных с исходно повышенным уровнем креатинина этот показатель достоверно снизился). В исследовании также было отмечено положительное влияние лизиноприла на уровень гликированного гемоглобина и липиды крови. Лизиноприл очень хорошо переносился: побочные эффекты были выявлены всего у 2,2% пациентов [16].
В настоящее время проводятся еще несколько исследований, результаты которых могут расширить показания к применению лизиноприла при хронических заболеваниях почек. Изучается эффективность лизиноприла у больных с поликистозом почек (HALT Progression of Polycystic Kidney Disease) и у больных с хронической почечной недостаточностью (VA NEPHRON-D: Diabetes iN Nephropathy Study) [17]. В данном исследовании предполагается изучить влияние на прогрессирование диабетической нефропатии и риск сердечно-сосудистых осложнений ИАПФ лизиноприла (10–40 мг/сутки) и блокатора рецепторов ангиотензина лозартана (50–100 мг/сутки). Кроме того, лизиноприл продемонстрировал отчетливый антигипертензивный и выраженный антипротеинурический эффект у детей как с диабетической нефропатией на фоне СД 1-го типа [18], так и с хроническим заболеванием почек, не связанным с СД [19].
В настоящее время в исследовании PTN_LISINO изучается эффективность и безопасность лизиноприла у 28 детей в возрасте от 2 до 17 лет, перенесших трансплантацию почек. Предполагается, что лизиноприл окажется способен не только оказать антипротеинурическое действие, но и предотвращать реакции отторжения трансплантанта. В данном исследовании у всех пациентов будет определяться концентрация лизиноприла в плазме крови для определения оптимальной дозы препарата для маленьких пациентов, поскольку в настоящее время Управление по контролю качества пищевых продуктов и лекарственных препаратов США (Food and Drug Administration, FDA) разрешает применение лизиноприла для лечения АГ и ХСН у детей старше 6 лет и подростков.
Хроническая обструктивная болезнь легких
С. А. Иванов и соавт. изучили антигипертензивный эффект лизиноприла, а также его влияние на функцию внешнего дыхания и частоту побочных эффектов у страдающих АГ (1–2 степени) курильщиков с большим стажем курения и диагнозом «ХОБЛ» в сравнении с эналаприлом и амлодипином [20]. Через 4 недели терапии антигипертензивная эффективность изучаемых препаратов оказалась сопоставимой, но при назначении эналаприла чаще развивалась гипотензия и такие побочные эффекты, как кашель и бронхообструкция, приведшие к отмене препарата у 8% больных. Лучшая переносимость лизиноприла по сравнению с эналаприлом у больных ХОБЛ, по мнению авторов, связана с меньшим воздействием на брадикининовый механизм регуляции тонуса сосудов и бронхов. При лечении эналаприлом риск отрицательного влияния на бронхиальную проходимость был выше и требовал более тщательного контроля за показателями функции внешнего дыхания.
Заболевания печени
По данным разных авторов от 10 до 30% больных АГ имеют те или иные проблемы с печенью. Это и пациенты с вирусными гепатитами, и лица, злоупотребляющие алкоголем либо принимающие препараты, оказывающие гепатотоксическое действие. Но самым распространенным (до 20–30% общей популяции) заболеванием печени, несомненно, является неалкогольная жировая болезнь печени (стеатоз, стеатогепатит) [21]. Назначаемый при заболеваниях печени противогипертензивный препарат не должен оказывать гепатотоксическое действие, взаимодействовать с другими лекарствами типа индукторов или ингибиторов микросомальных ферментов печени, его активность не должна зависеть от функционального состояния печени. Этим требованиям полностью соответствует ингибитор АПФ лизиноприл, не нуждающийся в биотрансформации для обретения фармакологической активности. В эксперименте лизиноприл даже улучшал регенерацию печени после удаления ее доли [22, 23].
Н. Ф. Шустваль и соавт. [24] изучали сравнительную эффективность и переносимость лизиноприла (Диротона) и эналаприла у больных АГ 1-й и 2-й степени и сопутствующим хроническим вирусным гепатитом. Оба препарата примерно одинаково снижали АД, снижали периферическое сосудистое сопротивление, улучшали эластичность сосудов, однако лизиноприл достоверно чаще снижал уровень трансаминаз и билирубина по сравнению с эналаприлом, на основании чего авторы сделали вывод о более выраженном гепатопротективном действии лизиноприла.
В России также есть опыт применения лизиноприла (Диротона) у больных с АГ и сопутствующим заболеванием печени [25, 26]. Л. Б. Лазебник с соавт. после изучения эффективности Диротона у больных АГ с различной патологией органов пищеварения (стеатозом, циррозом печени, язвенной болезнью 12-перстной кишки) сделали вывод, что эффективность Диротона не зависит от выраженности изменений печени у больных АГ [27].
Острый инфаркт миокарда
Лизиноприл является одним из немногих ингибиторов АПФ, которые можно применять с первых часов развития острого инфаркта миокарда (ОИМ). В исследовании GISSI-3, включавшем более 19000 больных, было показано, что прием лизиноприла (5–10 мг), начинавшийся с первых суток ОИМ (при стабильной гемодинамике) и продолжавшийся в течение 6 недель, привел к достоверному снижению общей смертности и существенному улучшению функции левого желудочка [28]. Наиболее эффективным применение лизиноприла было у больных с сопутствующим СД, у которых смертность снизилась в среднем на 32%. Снижение 6-недельной смертности при лечении лизиноприлом составило в среднем 27% у больных СД 1-го типа и 44% у больных СД 2-го типа.
В данном исследовании было показано, что лизиноприл не взаимодействует с ацетилсалициловой кислотой, обычно назначаемой больным с ИМ в анамнезе для профилактики развития повторного ИМ: выживаемость пациентов, получавших лизиноприл, не изменялась в случае одновременного применения больными ацетилсалициловой кислоты.
Ишемическая болезнь сердца
Что касается стабильных форм ишемической болезни сердца (ИБС), хочется напомнить, что в исследовании COURAGE, впервые продемонстрировавшем преимущества консервативной стратегии лечения перед чрескожным коронарным вмешательством, так называемая оптимальная медикаментозная терапия в числе прочих включала ИАПФ лизиноприл [29].
Хроническая сердечная недостаточность
В ранних испытаниях, проведенных в основном в 1980-е гг. и первой половине 1990-х гг., установлено, что в когорте пациентов с асимптомной и манифестной сердечной недостаточностью лизиноприл проявляет благоприятный гемодинамический потенциал, способствуя снижению периферического сосудистого сопротивления, давления заклинивания в легочной артерии, потенцированию суточного диуреза и повышению контрактильной способности ЛЖ [30]. Позднее эффективность лизиноприла при ХСН была изучена в двойном слепом рандомизированном исследовании ATLAS [31]. В это исследование были включены 3164 больных сердечной недостаточностью II–IV функционального класса по классификации Нью-Йоркской ассоциации кардиологов (New York Heart Association, NYHA) с фракцией выброса ниже 30%. Больные получали лизиноприл — в низких (2,5–5 мг/сут) и высоких дозах (32,5–35 мг/сут). Длительность наблюдения составила 39–58 мес. В этом исследовании было показано, что даже при назначении в небольших дозах (а из-за склонности к гипотонии далеко не всегда удается применять рекомендованные дозы ИАПФ) ИАПФ позволяют добиться улучшения прогноза при этом тяжелом заболевании. Достоверных различий в общей смертности между группами больных, получавших высокие или низкие дозы лизиноприла, отмечено не было.
Клиническое улучшение также было примерно одинаковым. Однако в группе больных, получавших лизиноприл в высоких дозах, достоверно ниже оказался риск смерти и госпитализации из-за сердечно-сосудистой причины (на 9%, р = 0,027), риск госпитализации в связи с декомпенсацией ХСН снизился на 24%, что означает необходимость достижения по возможности более высоких доз ИАПФ. Важно подчеркнуть, что частота побочных эффектов в группе низких и высоких доз лизиноприла оказалась сопоставимой. В дальнейшем результаты исследования ATLAS явились основанием для рекомендаций применения наиболее высокой из возможных доз ИАПФ (40 мг/сутки для лизиноприла) с целью улучшения клинических исходов пациентов с ХСН.
Таким образом, лизиноприл является высокоэффективным ИАПФ длительного действия, который благоприятно влияет на течение и исходы АГ, ХСН, ОИМ, а также риск развития таких осложнений СД, как диабетическая нефропатия и диабетическая ретинопатия.
Диротон — самый назначаемый в России препарат лизиноприла с большим опытом применения у врачей и доказательной базой эффективного лечения больных с сердечно-сосудистыми заболеваниями и профилактики их осложнений. Диротон выпускается в таблетках по 2,5, 5, 10 и 20 мг, что облегчает подбор оптимальной дозы в зависимости возраста, наличия сердечной недостаточности и функции почек. Основными показаниями к применению Диротона являются АГ (в том числе реноваскулярная), ХСН и бессимптомная дисфункция ЛЖ, ОИМ (с первых часов заболевания при условии стабильности гемодинамики), диабетическая нефропатия.
При АГ 1-й и 2-й степени достаточными бывают дозы в 10–20 мг/сут, при АГ 3-й степени, особенно в сочетании с СД, может потребоваться увеличение дозы до 30–40 мг/сут. При необходимости проведения комбинированной антигипертензивной терапии можно прибегнуть к назначению фиксированной комбинации Диротона с гидрохлоротиазидом (Ко-Диротон).
Благодаря уникальным фармакокинетическим особенностям Диротон занимает особое место среди прочих ИАПФ, имеет хорошую доказательную базу и большой терапевтический потенциал, хорошо переносится, отвечает современным требованиям безопасности и должен шире применяться в клинической практике.
Литература
- Рекомендации РМОАГ/ВНОК по диагностике и лечению артериальной гипертонии (IV пересмотр), 2010.
- Laher M. S., Donohoe J. F., Kelly J. G., Doyle G. D. Antihypertensive and renal effects of lisinopril in older patients with hypertension // Am. J. Med. 1988, 85 (3 B): 38–43.
- Falkner B., Canessa M., Anzalone D. Effect of angiotensin converting enzyme inhibitor (lisinopril) on insulin sensitivity and sodium transport in mild hypertension. Am. J. Hypertens. 1995, 8 (5 Pt. 1): 454–460.
- Zehetgruber M., Beckmann R., Gabriel H. et al. The ACE-inhibitor lisinopril affects plasma insulin levels but not fibrinolytic parameters // Thromb. Res. 1996, 83 (2): 143–152.
- Macchiarulo C., Pieri R., Mitolo D. C. et al. Management of antihypertensive treatment with Lisinopril: a chronotherapeutic approach // Eur Rev Med Pharmacol Sci. 1999; 3 (6): 269–275.
- Diamant M., Vincent H. H. Lisinopril versus enalapril: evaluation of trough: peak ratio by ambulatory blood pressure monitoring // J Hum Hypertens. 1999; 13 (6): 405–412.
- Rosei E. A., Rizzoni D., Comini S. et al. Evaluation of the efficacy and tolerability of nebivolol versus lisinopril in the treatment of essential arterial hypertension: a randomized, multicentre, double–blind study // Blood Press Suppl. 2003, May; 1: 30–35.
- Stergiou G. S., Efstathiou S. P., Roussias L. G. et. Al. Blood pressure- and pulse pressure-lowering effects, trough: peak ratio and smoothness index of telmisartan compared with lisinopril // J Cardiovasc Pharmacol. 2003, Oct; 42 (4): 491–496.
- Malacco E., Santonastaso M., Vari N. A. et al. Comparison of valsartan 160 mg with lisinopril 20 mg, given as monotherapy or in combination with a diuretic, for the treatment of hypertension: the Blood Pressure Reduction and Tolerability of Valsartan in Comparison with Lisinopril (PREVAIL) study // Clin Ther. 2004. Jun; 26 (6): 855–865.
- Davis B. R., Culter J. A., Gordon D. J. Antihypertensive and lipid-lowering treatment to prevent heart attack trial // Am. J. Hypertens. 1996. Vol. 9. P. 342–360.
- Black H., Davis B. ALLHAT Collaborative Research Group Clinical outcomes in participants with cardiovascular dysmetabolic syndrome in the antihypertensive and lipid-lowering treatment to prevent heart attack trial (ALLHAT) // J. Hypertens. 2005, 23 (Suppl. 2): S146.
- Mancia G., Zanchetti A., Agabiti-Rosei E. et al. Ambulatory blood pressure is superior to clinic blood pressure in predicting treatment-induced regression of left ventricular hypertrophy. SAMPLE Study Group. Study on Ambulatory Monitoring of Blood Pressure and Lisinopril Evaluation // Circulation. 1997; 95 (6); 1464–1470.
- Rizzoni D., Muiesan M. L., Porteri E. et al. Effects of long-term antihypertensive treatment with lisinopril on resistance arteries in hypertensive patients with left ventricular hypertrophy // J. Hypertension. 1997; 15: 197–204.
- Terpstra W. F., May J. F., Smit A. J. et al. Long-term effects of amlodipine and lisinopril on left ventricular mass and diastolic function in elderly, previously untreated hypertensive patients: the ELVERA trial // J Hypertens. 2001; 19 (2): 303–309.
- EUCLID Study Group. Effect of lisinopril on progression of retinopathy in normotensive people with type 1 diabetes // Lancet. 1998; 351: 28–31.
- Parving H. H. Effects of ACE inhibitors on renal function in incipient and overt diabetic nephropathy // J Diabetes Complications. 1996; 10 (3): 133–135.
- Fried L. F., Duckworth W., Zhang J. H. VA NEPHRON-D Investigators. Design of combination angiotensin receptor blocker and angiotensin-converting enzyme inhibitor for treatment of diabetic nephropathy (VA NEPHRON-D) // Clin J Am Soc Nephrol. 2009, Feb; 4 (2): 361–368.
- Raes A., Van Aken S., Vande Walle J. et al. Are renal hypertrophy and renal functional abnormalities reversible in children with IDDM? // Pediat. Nephr. 1997, 11: C38.
- Raes A., Malfait F., Van Aken S. et al. Lisinopril in paediatric medicine: a retrospective chart review of long-term treatment in children // J. Renin Angiotensin Aldosterone Syst. 2007, 8 (1): 3–12).
- Савенков М. П., Иванов С. А., Окунева И. Н. с соавт. Применение лизиноприла у больных с артериальной гипертонией и хронической обструктивной болезнью легких // Росс. мед. журнал. 2009. № 2, 102–105.
- Bedogni G., Miglioli L., Masutti F. et al Prevalence of and risk factors for nonalcoholic fatty liver disease: the Dionysos nutrition and liver study // Hepatology. 2005; 42: 44–52.
- Ramalho F. S., Ramalho L. N., Castro-e-Silva O. et al. Effect of angiotensin–converting enzyme inhibitors on liver regeneration in rats // Hepatogastroenterology. 2002; 49 (47): 1347–1351.
- Yayama K., Sugiyama K., Miyagi R. et al. Angiotensin-converting enzyme inhibitor enhances liver regeneration following partial hepatectomy: involvement of bradykinin B2 and angiotensin AT1 receptors // Biol Pharm Bull. 2007; 30 (3): 591–594.
- Шустваль Н. Ф., Малый В. П., Пеньков Д. Б. Опыт применения диротона (лизиноприла) и эналаприла для лечения мягкой и умеренной артериальной гипертензии у больных с хроническим гепатитом // Укр. мед. журнал. 2004, I/II, № 1 (39), 45–50.
- Михеева О. М., Комиссаренко И. А., Дроздов В. Н. и др. () Применение ингибиторов ангиотензинпревращающего фермента у больных артериальной гипертонией на фоне патологии печени // Consilium medicum. 2007, 9 (11): 72–76.
- Драпкина О. М., Тутнов Д. А. Особенности лечения артериальной гипертензии у больных с заболеваниями печени // Рос. мед. вести. 2008, XIII (3): 43–48.
- Лазебник Л. Б., Михеева О. М., Комиссаренко И. А. Лизиноприл при лечении артериальной гипертонии у больных с патологией органов пищеварения // Лечащий Врач. 2012, № 7.
- GISSI-3: effects of lisinopril and transdermal glyceryl trinitrate singly and together on 6-week mortality and ventricularfunction after acute myocardial infarction. Gruppo Italiano per lo Studio della Sopravvivenza nel-l’Infarto Miocardico // Lancet. 1994; 343: 1115–1122.
- Kereiakes D. J., Teirstein P. S., Sarembock I. J. et al. The truth and consequences of the COURAGE trial // J. Am. Coll. Cardiol. 2007, 50 (16): 1598–1603.
- Dickstein K., Aarsland T., Woie L. et al. Acute hemodynamic and hormonal effects of lisinopril (MK-521) in congestive heart failure // Am. Heart J. 1986, 112 (1): 121–129.
- Packer M., Poole-Wilson P. A., Armstrong P. W. et al. Comparative effects of low and high doses of angiotensin-converting enzyme inhibitor, lisinopril, on morbidity and mortality in chronic heart failure. ATLAS Study Group // Circulation. 1999; 100 (23): 2312–2318.
Г. А. Барышникова, доктор медицинских наук, профессор
И. И. Степанова, кандидат медицинских наук
Н. В. Чупрова
ФГБУ «Учебно-научный медицинский центр» УД Президента РФ, Москва
Контактная информация об авторах для переписки: bargalan@mail.ru
Купить номер с этой статьей в pdf