В современной клинике внутренних болезней артериальная гипертензия (АГ) и хроническая обструктивная болезнь легких (ХОБЛ) занимают значимое место в структуре общей заболеваемости, а их сочетание представляет одно из самых частых коморбидных состояний [1–3]. ХОБЛ осложняет течение АГ, нередко приводя к более агрессивному поражению органов-мишеней. Доказано, что не только высокое артериальное давление (АД), но и повышенная вариабельность артериального давления (ВАД) ассоциируются с поражением органов-мишеней [4, 5] и признаются фактором риска сердечно-сосудистых осложнений [6, 7]. У больных АГ и ХОБЛ имеются общие факторы риска и схожие патогенетические механизмы, такие как системное воспаление, эндотелиальная дисфункция, оксидативный стресс, гипоксия [8, 9], что ведет к более ранней и выраженной активации симпатоадреналовой (САС) и ренин-ангиотензин-альдостероновой системы (РААС), способствуя прогрессированию заболеваний. Избыточная активность РААС у больных данной сочетанной патологией подтверждает необходимость специфического терапевтического воздействия с учетом положительного влияния антигипертензивных препаратов (АГП) на эту систему. Такими свойствами обладают прежде всего ингибиторы ангиотензинпревращающего фермента (иАПФ) и блокаторы рецепторов ангиотензина II (БРА), комбинация которых во всем мире признана нерациональной [10]. В связи с этим остается актуальным решение вопроса о выборе блокатора РААС для больных АГ в сочетании с ХОБЛ с учетом не только их антигипертензивного эффекта, но и влияния на патогенетические механизмы прогрессирования заболеваний, таких как эндотелиальная дисфункция, ВАД, давление в легочной артерии.
Целью данного исследования было изучить у больных АГ в сочетании с ХОБЛ краткосрочную, суточную и долгосрочную вариабельность артериального давления на фоне лечения ингибитором ангиотензинпревращающего фермента и блокатором рецепторов ангиотензина II исходно, через 4 недели и 6 месяцев лечения.
Материал и методы исследования
В исследование включено 60 человек с сочетанной патологией АГ и ХОБЛ, разделенных на две группы по 30 человек каждая. В первой группе больных в качестве основного АГП был назначен БРА (азилсартана медоксомил (Эдарби)) в дозе 40 мг/сутки, во второй группе — иАПФ (фозиноприл (Моноприл)) в дозе 20 мг/сутки. Больные, по необходимости, продолжали прием назначенных ранее статинов, бета-адреноблокаторов, диуретика гидрохлортиазида в дозе 12,5 мг в сутки, а также бронхолитическую терапию M-холинолитиком Атровентом или комбинированными препаратами Беродуал и Ультибро Бризхалер. Дозы препаратов в течение периода наблюдения за больными не менялись. Включались больные в возрасте от 40 до 65 лет, имеющие АГ 1–2 степени и сопутствующую ХОБЛ 1–2 степени тяжести вне обострения. Не включались больные резистентной, в том числе стойкой АГ тяжелой степени (систолическое АД (САД) > 180 мм рт. ст. и/или диастолическое АД (ДАД) > 110 мм рт. ст.), вторичной АГ, имеющие хроническую сердечную недостаточность со сниженной фракцией выброса и выше III ФК, бронхиальной астмой.
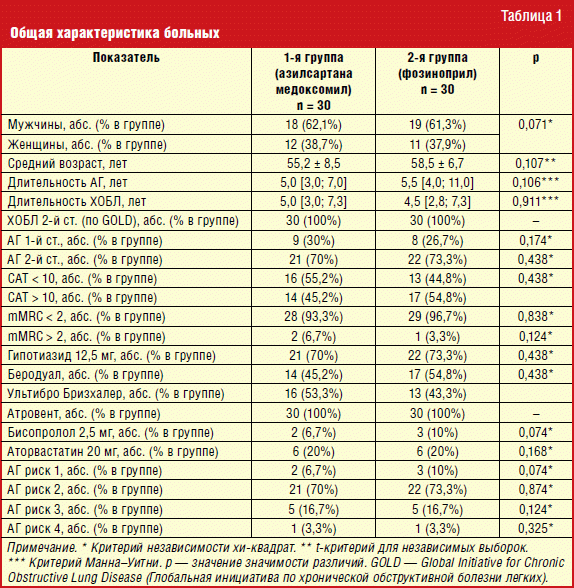
Пациенты обеих групп исследования оказались сопоставимы по полу, возрасту, тяжести основной и сопутствующей патологии (табл. 1).
Обследование всех больных проводили по классической схеме. Клиническое обследование включало: сбор жалоб, изучение анамнеза заболевания, осмотр, перкуссию и аускультацию, измерение АД по методу Короткова с помощью электронного сфигмоманометра AND UA-787, измерение частоты сердечных сокращений (ЧСС) за 1 минуту, расчет индекса курящего человека (ИКЧ, пачка/лет). Также всем больным проведено полное клинико-инструментальное обследование, а именно: офисное измерение АД и ЧСС исходно на 7-е, 14-е, 28-е сутки; исходно, через 4 недели и через 6 месяцев лечения — суточное мониторирование АД (СМАД) и исследование функции внешнего дыхания (ФВД). За краткосрочную ВАД (внутривизитную) мы принимали абсолютную разницу между тремя последовательными измерениями и рассчитывали ее, как для САД, так и для ДАД, на 28-й день исследования на фоне лечения; за межвизитную ВАД мы принимали абсолютную разницу между максимальным САД через 14 дней и 28 дней и максимальным ДАД, которая рассчитывалась нами между визитами больного также через 14 дней и 28 дней; долгосрочную ВАД — разницу между максимальным и минимальным значением уровня АД (MMD) мы рассчитывали как разницу между максимальным и минимальным значением САД через 2 и через 4 недели исследования при самоконтроле АД. Исходные характеристики больных представлены в табл. 2.
Диагноз АГ был установлен на основании общепринятых критериев (ESH/ESC2018). Диагноз ХОБЛ определялся в соответствии с признаками, изложенными в отечественных рекомендациях и в Международной программе «Глобальная стратегия диагностики, лечения и профилактики ХОБЛ» [11, 12]. Показателем, позволяющим достоверно судить о наличии ХОБЛ, служило постбронходилатационное значение ОФВ1/ФЖЕЛ < 0,70, подтверждающее наличие ограничения воздушного потока. Необходимым условием выполнения алгоритма постановки диагноза является оценка одышки по шкале mMRC (Medical Research Council Dyspnea Scale — mMRС) и симптомов по шкале CAT (COPD Assessment Test — CAT).
Следует отметить, что всем больным в ходе исследования предлагалось отмечать в дневниках самоконтроля нежелательные реакции, которые они могли бы связать с приемом назначенных им АГП, обязательными из которых считались кашель (его усиление и связь с приемом препарата), качество ночного сна, отеки, одышка, гипотония. В дальнейшем для объективной оценки характеристики респираторных нарушений всем больным проводилось исследование ФВД в динамике через 4 недели и 6 месяцев исследования, при сопоставлении с исходными данными.
Важно отметить, что на фоне назначенных АГП у 2 больных 1-й группы отмечалась «гипотония первой дозы» (снижение АД до 115/65 мм рт. ст. и 110/60 мм рт. ст. соответственно), не потребовавшая отмены препарата в последующем.
Также при сопоставлении дневников самоконтроля пациентов с показателями СМАД не установлено связи с повышением АД и усилением кашля, а также ухудшением качества ночного сна, приступами одышки, что может свидетельствовать об отсутствии нежелательных респираторных реакций на фоне назначенных блокаторов РААС.
Важно подчеркнуть, что на фоне применения как азилсартана медоксомила, так и фозиноприла у больных обеих групп не отмечалось отрицательного влияния на показатели ФВД, а выявлялось некоторое улучшение исследуемых параметров, что предположительно может быть связано с улучшением легочной гемодинамики и перфузии на фоне эффективной АГП-терапии.
Статистическая обработка данных проводилась с применением пакетов прикладных компьютерных программ IBM SPSS Statistics 24 (IBM), Statistica 6.0 для Windows (StatSoft) и Microsoft Office Excel 2016 (Microsoft). Различия считались достоверными при уровне значимости р ≤ 0,05.
Результаты и обсуждение
У всех пациентов, включенных в исследование, проводилось исследование АД и ЧСС исходно, на 7-й, 14-й и 28-й день при явке в стационар.
В динамике на фоне лечения обеими группами лекарственных препаратов к концу первого месяца лечения в 1-й группе больных САД снизилось до 128,0 ± 6,4 мм рт. ст., во 2-й группе больных САД снизилось до 134,2 ± 7,0 мм рт. ст. (р < 0,001). При межгрупповом сравнении выявлено, что лучше САД снижалось в 1-й группе пациентов, получающих лечение азилсартана медоксомилом, и к концу 1-го месяца лечения среднее САД в этой группе снизилось на 29,4 ± 6,3 мм рт. ст., а во 2-й группе — на 20,8 ± 7,4 мм рт. ст. (гипотеза об отсутствии взаимодействия фактора времени и типа лечения отвергается, р < 0,001) (рис. 1). На рисунке видно, что исходные средние значения по группам были статистически незначимые, а затем наблюдалось большее снижение САД в группе лечения азилсартана медоксомилом.
Что касается среднего ДАД в динамике, то на фоне лечения обеими группами лекарственных препаратов также к концу первого месяца лечения было выявлено достоверное снижение этого показателя (р < 0,001), так, в 1-й группе больных ДАД составило 78,7 ± 4,5 мм рт. ст., во 2-й группе больных ДАД снизилось до 81,1 ± 6,8 мм рт. ст. При межгрупповом сравнении достоверной разницы не получилось (р = 0,22). Однако в 1-й группе пациентов, принимающих азилсартана медоксомил, к концу 1-го месяца лечения среднее ДАД снизилось в большей степени, а именно на 8,9 ± 4,3 мм рт. ст., а во 2-й группе, получающей фозиноприл, — на 6,7 ± 5,1 мм рт. ст. (р < 0,001) (рис. 2).
При оценке средней ЧСС в динамике выявлено достоверное снижение этого показателя в обеих группах (р < 0,001). В 1-й группе больных ЧСС составила 71,1 ± 4,7 уд./мин., во 2-й группе больных — 71,3 ± 5,9 уд./мин. При межгрупповом сравнении на фоне фактора времени средних значений ЧСС достоверной разницы не получилось (р = 0,676 и р = 0,787 соответственно), в обеих группах ЧСС снижалась одинаково хорошо, так, в 1-й группе пациентов, принимающих азилсартана медоксомил, к концу 1-го месяца лечения ЧСС снизилась на 5,4 уд./мин, а во 2-й группе больных, принимающих фозиноприл, — на 5,0 уд./мин.
Следует отметить, что целевые цифры АД (меньше 140/90 мм рт. ст.) к четвертой неделе исследования были достигнуты у 29 (97%) больных в 1-й группе и у 19 больных (63%) во 2-й группе.
По результатам СМАД, средние значения САД за день (САДд) и САД за ночь (САДн), ДАД за день (ДАДд) и ДАД за ночь (ДАДн) в 1-й группе (азилсартана медоксомил) и во 2-й группе (фозиноприл) достоверно не отличались (р = 0,06 и р = 0,6, р = 0,1 и р = 0,6 соответственно). На момент включения в исследование по СМАД было 19 (63,3%) больных с суточным профилем АД «non-dipper» и 11 (36,7%) «night-peaker» в 1-й группе, и с недостаточным снижением ночного АД «non-dipper» было 20 человек (66,7%) и с повышенным профилем АД «night-peaker» — 9 (30%) во 2-й группе.
Через 6 месяцев исследования всем пациентам 1-й группы удалось достичь целевых цифр АД без повышения дозы препарата. САДд составило 126,5 ± 4,2 мм рт. ст., САДн составило 120,6 ± 4,1 мм рт. ст. (р < 0,001), ДАДд — 77,3 ± 2,3 мм рт. ст., ДАДн — 72,7 ± 3,5 мм рт. ст. (р < 0,001), среднее пульсовое давление (ПД) стало 53,4 ± 6,2 уд./мин (р < 0,001); во 2-й группе АД нормализовалось также у всех больных, однако 5 больным пришлось увеличить дозу фозиноприла до 40 мг/сутки. САДд составило 132,6 ± 7,4 мм рт. ст., САДн составило 123 ± 5,6 мм рт. ст. (р < 0,001), ДАДд — 79,4 ± 3,7 мм рт. ст., ДАДн — 72,7 ± 3,5 мм рт. ст. (р < 0,001), среднее ПД стало 57,5 ± 6,8 уд./мин (р < 0,001) (рис. 3, 4).
У 19 больных в 1-й группе, имевших утреннюю гипертонию, отмечено уменьшение величины утреннего подъема САД в среднем на 14,7 ± 6,8 мм рт. ст. (р < 0,001) и ДАД на 8,1 ± 5,3 мм рт. ст. (р < 0,001). Также в 1-й группе отмечается увеличение количества больных с нормальным профилем АД до 22 (73,3%) (р = 0,002), уменьшение количества больных с недостаточным ночным снижением АД до 8 (26,7%) (р < 0,001) (рис. 5).
Из 22 больных, имевших утреннюю гипертонию, у 17 отмечено уменьшение величины утреннего подъема САД в среднем на 11,7 ± 7,1 мм рт. ст. (р < 0,001) и ДАД на 7,6 ± 5,9 мм рт. ст. (р < 0,001) во 2-й группе, а также в результате лечения количество больных с суточным типом АД «dipper» увеличилось на 9 человек и составило 33,3% (р = 0,02) (рис. 6).
Что касается варибельности АД по результатам СМАД, то в 1-й группе вариабельность САДд (ВарСАДд) исходно 17,0 ± 4,3 мм рт. ст. и на фоне лечения через 6 месяцев достоверно снизилась до 12,9 ± 1,8 мм рт. ст. (р < 0,001). Вариабельность САДн (ВарСАДн): исходно 17,7 ± 11,6 мм рт. ст., через 6 месяцев — 13,6 ± 5,4 мм рт. ст. (р < 0,001). Вариабельность ДАДд (ВарДАДд): исходно 13,0 ± 4,5 мм рт. ст. и 9,8 ± 1,3 мм рт. ст. через 6 месяцев исследования (р < 0,001). Вариабельность ДАДн (ВарДАДн): исходно 11,8 ± 6,9 мм рт. ст. и 11,2 ± 7,2 мм рт. ст. через 6 месяцев исследования (р = 0,3).
Во 2-й группе также отмечалось снижение вариабельности АД. ВарСАДд при лечении фозиноприлом: исходно 16,3 ± 4,3 мм рт. ст., на фоне лечения через 6 месяцев достоверно снизилась до 13,5 ± 2,9 мм. рт. ст. (р < 0,001). ВарСАДн: исходно 17,0 ± 10,7 мм рт. ст., через 6 месяцев — 15,0 ± 8,7 мм рт. ст. (р < 0,001). ВарДАДд: исходно 12,6 ± 4,3 мм рт. ст. и 9,9 ± 1,6 мм рт. ст. через 6 месяцев исследования (р < 0,001). ВарДАДн: исходно 11,7 ± 6,7 мм рт. ст. и 10,9 ± 7,9 мм рт. ст. через 6 месяцев исследования (р = 0,2). Таким образом, в обеих группах на фоне лечения вариабельность АД как дневного, так и ночного достоверно снижалась (р < 0,001), за исключением ночной вариабельности ДАД, при межгрупповом сравнении которой достоверной разницы получено не было.
При изучении краткосрочной ВАД на 28-й день лечения выяснилось, что в первой группе внутривизитная вариабельность ДАД (ВарДАД) между вторым и третьим измерениями была достоверно ниже (р = 0,04), а при исследовании гендерных различий данный вид вариабельности был достоверно ниже у мужчин 1-й группы между вторым и третьим измерениями (р = 0,04) по сравнению со 2-й группой. У женщин как в 1-й, так и во 2-й группе больных достоверной разницы получено не было (табл. 3).
При исследовании долгосрочной вариабельности АД при внутригрупповом сравнении достоверно значимое снижение показателей выявлено у больных 1-й группы, получающих БРА азилсаратана медоксомил, по сравнению с больными 2-й группы, получающими иАПФ фозиноприл, как по межвизитной вариабельности САД (ВарСАД) (р = 0,004), так и ВарДАД (р = 0,003). При межгрупповом сравнении этих показателей достоверных различий не получилось.
Что же касается гендерных различий, то у мужчин в 1-й группе на фоне лечения отмечалось достоверное снижение межвизитной ВарСАД (р = 0,005) и межвизитной ВарДАД (р = 0,02) через 4 недели по сравнению со 2-й группой, где достоверной разницы не было (р = 0,49). У женщин 1-й группы показатели межвизитной ВарСАД достоверно не отличались от показателей 2-й группы между 2-й и 4-й неделями лечения (р = 0,42), а показатели межвизитной ВарДАД достоверно снижались у женщин 1-й группы по сравнению с женщинами 2-й группы (р = 0,04) (рис. 7).
Также нами был проанализирован такой вариант ВАД, как разница между максимальным и минимальным значением САД (MMD). Данная ВАД рассчитывалась через 2 недели и через 4 недели исследования для оценки эффективности назначенных доз лекарственных препаратов. В 1-й группе пациентов, которым был назначен БРА азилсартана медоксомил, средние значения MMD через 2 недели составили 55,0 [47,0; 60,0] мм рт. ст. и через 4 недели лечения показатели стали 40,0 [35,0; 45,0] мм рт. ст. (р < 0,001).
Во 2-й группе больных, получающих фозиноприл, средние значения MMD через 2 недели составили 50,0 [45,0; 58,0] мм рт. ст. и через 4 недели лечения показатели стали 40,0 [38,0; 46,0] мм рт. ст. (р < 0,001), что подтверждает эффективность обеих групп лекарственных препаратов на фоне лечения в течение первого месяца.
При изучении гендерных различий повышенные цифры ВАД MMD были в обеих группах больных и достоверно снижались в ходе лечения как в 1-й, так и во 2-й группе (р < 0,001), и достоверных различий между группами не выявлено.
Таким образом, в нашем исследовании ВАД снижалась на фоне как терапией иАПФ, так и БРА, однако вторыми в большей степени.
Что касается исследования ФВД, то в динамике получено статистически значимое улучшение показателя ОФВ1 в обеих группах больных (р < 0,001), но клинически оно было незначимым (прирост меньше 100 мл), больные соответствовали критериям отбора и находились вне обострения.
Важным является и то, что на фоне приема фозиноприла у больных с АГ и ХОБЛ (по данным дневников самоконтроля) не отмечалось ни одного случая приступов удушья, усиления одышки, ухудшения сна ночью, а также не было выявлено усиления сухого кашля или его развития на фоне приема данного препарата, что может подтверждать его эффективность и безопасность у данной группы больных. Достоверных изменений показателей ФВД также не было выявлено.
Выводы
- При краткосрочной терапии в течение 4 недель на фоне терапии азилсартана медоксомилом зарегистрирован больший процент пациентов, достигших целевого АД, по сравнению с фозиноприлом: 97% и 63% пациентов соответственно. При дальнейшем наблюдении в течение 6 месяцев все пациенты, принимавшие азилсартана медоксомил, достигли целевого уровня АД без увеличения дозы препарата, в то время как на фоне терапии фозиноприлом 5 пациентам для этого потребовалось увеличение дозы.
- У больных АГ и ХОБЛ в течение 6 месяцев терапии АГ фозиноприл и азилсартана медоксомил оказывают разное влияние на показатели суточного мониторирования АД и вариабельность АД, что выражается при лечении БРА, в отличие от иАПФ, в более быстрой нормализации суточного профиля АД (р = 0,002), уменьшении величины утреннего подъема систолического и диастолического АД (р < 0,001), снижении дневной и ночной вариабельности систолического АД (р < 0,001) и дневной вариабельности диастолического АД (р < 0,001), достоверно большего снижения межвизитной вариабельности систолического АД (р = 0,004) и диастолического АД (p = 0,003), что позволяет судить о более выраженной блокаде РААС блокатором рецепторов ангиотензина II.
Заключение
Таким образом, больным с коморбидной патологией АГ и ХОБЛ, помимо исследования показателей суточного мониторирования АД, в качестве дополнительных критериев эффективности проводимой антигипертензивной терапии, рекомендуется проводить исследование краткосрочной и долгосрочной вариабельности АД как одного из прогностически значимых факторов риска сердечно-сосудистых осложнений. Больным ХОБЛ для лечения сопутствующей АГ рекомендуется назначение блокаторов РААС, с предпочтительным назначением БРА — азилсартана медоксомила, обладающего более выраженной эффективностью в отношении снижения АД и вариабельности АД.
Литература
- Кароли Н. А., Ребров А. П. Хроническая обструктивная болезнь легких и артериальная гипертензия: сосудистая стенка как орган-мишень у коморбидных больных // Рациональная фармакотерапия в кардиологии. 2017. Т. 13, № 4. С. 513–518.
- Задиоченко В. С., Ли В. В., Адашева Т. В. Артериальная гипертензия у больных хронической обструктивной болезнью легких (20-летний опыт изучения) // Медицинский совет. 2012. № 10. С. 10–17.
- Dal Negro R. W., Bonadiman L., Turco P. Prevalence of different comorbidities in COPD patients by gender and GOLD stage // Multidiscip. Respir. Med. 2015. Vol. 10, № 1. P. 24.
- Höcht C. Blood Pressure Variability: Prognostic Value and Therapeutic Implications // Hypertension. 2013. Vol. 2013. ID398485.
- Vidal-Petiot E., Stebbins A., Chiswell K. et al. Visit-to-visit variability of blood pressure and cardiovascular outcomes in patients with stable coronary heart disease. Insights from the STABILITY trial // Eur. Heart J. 2017. Vol. 38, № 37. Р. 2813–2822.
- Остроумова О. Д., Борисова Е. В., Павлеева Е. Е. Вариабельность артериального давления. Межвизитная вариабельность артериального давления // Кардиология. 2017. Т. 57, № 11. С. 68–75.
- Parati G., Ochoa J. E., Lombardi C., Bilo G. Blood pressure variability: assessment, predictive value, and potential as a therapeutic target // Curr. Hypertens. Rep. 2015. Vol. 17, № 4. Р. 537.
- Münzel T. et al. Impact of oxidative stress on the heart and vasculature: part 2 of a 3-partseries // J. Amer. Coll. Cardiol. 2017. Vol. 70, №. 2. Р. 212–229.
- Tomiyamа H., Ishizu T., Kohro R. Longitudinal association among endothelial function, arterial stiffness and subclinical organ damage in hypertension // Int. J. Cardiol. 2018. Vol. 253. Р. 161–166.
- Williams B., Mancia G., Spiering W. et al. ESC/ESH Guidelines for the management of arterial hypertension // Eur. Heart J. 2018. Vol. 39, Is. 33. P. 3021–3104.
- Национальные рекомендации по ХОБЛ [Электронный ресурс]. Минздрав РФ; РНМОТ, 2018. С. 7–19. Режим доступа: http://spulmo.ru/obrazovatelnye-resursy/federalnye-klinicheskie-rekomendatsii/. Дата обращения: 09.03.2018.
- Global Initiative for Chronic Obstructive Lung Diseases (GOLD). Global strategy for the Diagnosis, Management, and Prevention of Chronic Obstructive Lung Disease. NHLBI/WHO workshop report. Updated 2019 [Electronic resource]. Mode of access: http://www.who.int/respiratory/copd/burden/en. Date of access: 15.02.2019.
М. Е. Королёва
ФГБОУ ВО ПИМУ Минздрава России, Нижний Новгород
1 Контактная информация: grigoreva28@mail.ru
DOI: 10.26295/OS.2019.40.83.003
Влияние азилсартана медоксомила на вариабельность артериального давления у больных артериальной гипертензией и хронической обструктивной болезнью легких/ Н. Ю. Григорьева, М. Е. Королёва
Для цитирования: Лечащий врач № 7/2019; Номера страниц в выпуске: 17-23
Теги: коморбидность, антигипертензивные препараты, одышка, легочная гемодинамика
Купить номер с этой статьей в pdf