Повреждение органов-мишеней в результате длительного повышения артериального давления (АД) является самостоятельным и независимым от степени артериальной гипертензии (АГ) фактором, который способствует развитию заболеваний, сопутствующих ей, а также их кумулятивных неблагоприятных исходов.
Сценарий течения АГ (влияние заболевания на качество жизни и прогноз больного; наличие осложнений и т. д.) зависит от многих факторов, в том числе от своевременно начатой фармакологической органопротекции, которая способна комплексно влиять на основные звенья патогенеза АГ (ренин-ангиотензин-альдостероновую, симпатоадреналовую, калликреин-кининовую системы, а также на натрий-зависимый механизм повышения АД).
На ранних стадиях АГ у пациентов с высоким риском развития ее осложнений для длительной терапии логично выбирать гипотензивные препараты, обладающие достаточным гипотензивным эффектом уже при назначении низких доз (профилактика гипотонии и минимизация нежелательных явлений лечения), а также максимально выраженными органопротективными свойствами. При этом предпочтение следует отдавать низкодозовым фиксированным комбинациям, которые, несомненно, повышают комплайенс и дисциплину больных.
Основными принципами комбинирования гипотензивных препаратов являются: потенциирование гипотензивного эффекта одного вещества другим; расширение спектра органопротекции, так актуальной в связи с поражением при АГ ряда органов-мишеней; синергизм плейотропных влияний; а также максимально полное торможение фундаментальных «китов» патогенеза АГ, а именно: симпатической нервной системы (СНС), ренин-ангиотензин-альдостероновой системы (РААС) и натрий-объем-зависимого механизма повышения АД [1].
Помнить о приверженности к лечению следует с первого контакта с больным, так как задатки адекватного комплайенса должны быть сформированы в сравнительно молодом возрасте, когда пациенты еще не считают нужным регулярно принимать медикаменты и уверены, что справятся с начальными проявлениями своих заболеваний (так называемыми «факторами риска») посредством отказа от вредных привычек, ведения спортивного образа жизни и силы воли.
Несомненными преимуществами разносторонних фиксированных комбинаций в терапии коморбидных больных являются, прежде всего, ощутимое повышение приверженности пациента к лечению, улучшение его переносимости и возможность привнести в него дополнительные медикаментозные агенты за счет уменьшения числа таблеток и прочих лекарственных форм, принимаемых пациентом в течение суток.
Кроме того, применение фиксированных комбинаций, содержащих в своем составе сбалансированные дозы лекарственных веществ, не взаимодействующих между собой на различных уровнях, освобождает врача от очевидных сомнений в правильности своих назначений с позиции безопасного сочетания данных медикаментов.
Закономерно, что подобные высокоорганопротективные фиксированные комбинации должны присутствовать в лекарственных формулярах лечебно-профилактических учреждений и предназначаться больным как с начальными проявлениями АГ, так и пациентам с высоким риском развития ее осложнений.
Одним из современных многокомпонентных низкодозовых отечественных лекарственных средств, направленных на повышение комплайенса больных АГ 1-й и 2-й степени, является препарат Гипотэф.
Неподдельный интерес исследователей и врачей к данному препарату связан прежде всего с его уникальным составом и способностью к комплексной цито- и органопротекции.
Влияние ранней Фармакологической Органопротекции на Развитие оСложнений Артериальной гипертензии в условиях низкой приверЖенности к лечению (ФОРСАЖ)
Целью исследования было определить влияние ранней фармакологической органопротекции на течение основного заболевания, качество жизни и прогноз больных артериальной гипертензией 1–2 степеней.
Задачи исследования:
- изучить спектр органопротективных свойств различных лекарственных препаратов (в т. ч. комбинированных), применяемых в терапии АГ;
- изучить особенности органопротекции, оказываемой фиксированной низкодозовой комбинацией эналаприла, метопролола тартрата, индапамида и винпоцетина (препарат Гипотэф);
- определить эффективность и безопасность данной фиксированной комбинации.
Материалы исследования
Авторы провели ретроспективный анализ медицинской документации 517 амбулаторных пациентов трудоспособного возраста (средний возраст 51,8 ± 4,3 года) с верифицированным диагнозом АГ 1-й и 2-й степени и дополнительными факторами риска развития сердечно-сосудистых заболеваний (ССЗ) (в т. ч. избыточная масса тела, дислипидемия, частые стрессы на работе и дома, малоподвижный образ жизни, курение и т. д.).
Данные пациенты не переносили кардио- и цереброваскулярных катастроф (инсульт, инфаркт миокарда, транзиторная ишемическая атака, острый коронарный синдром, тромбоэмболия легочных артерий), а также хирургических вмешательств на сосудах; не имели тяжелых декомпенсированных заболеваний, хронических привычных интоксикаций (кроме курения), а также признаков активной инфекции, включая гнойные процессы, туберкулез и инфекционный эндокардит.
Согласно современным рекомендациям Европейского общества кардиологов (European Society of Cardiology, ESC) [2] и Российского кардиологического общества (РКО) [3] подобным пациентам следует заниматься модификацией своего образа жизни, а также коррекцией и устранением факторов, предрасполагающих к развитию ССЗ. С целью первичной профилактики ССЗ им рекомендуется ежедневно получать плановую консервативную терапию АГ, в составе которой должны быть современные эффективные и безопасные антигипертензивные препараты, обладающие органопротективными и плейотропными свойствами (как в режиме монотерапии, так и в виде комбинаций (в т. ч. фиксированных)).
Так, из 517 человек 284 пациента (54,9%) некоторое время назад начали получать гипотензивные препараты в режиме монотерапии, а 233 пациента (45,1%) — в виде комбинаций. Из 233 человек, находящихся на комбинированной терапии, 113 пациентов (48,5%) лечились комбинациями раздельных препаратов, а 120 пациентов (51,5%) — фиксированными комбинациями. Детализация основных классов гипотензивных препаратов представлена в табл. 1.
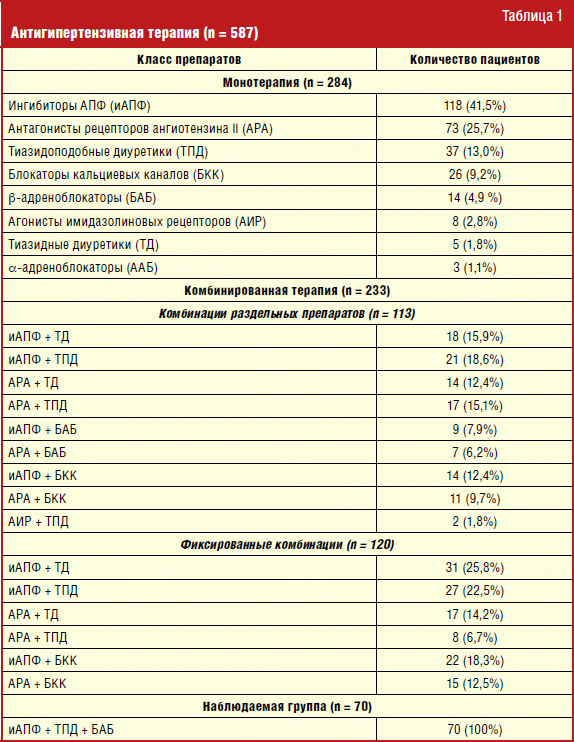
В наблюдаемую группу (группа 1) вошли дополнительные 70 пациентов (40 мужчин (57,1%) и 30 женщин (42,9%), средний возраст 52,6 ± 3,9 года), которые получали фиксированную низкодозовую комбинацию Гипотэф, включающую 5 мг эналаприла; 25 мг метопролола тартрата; 0,75 мг индапамида и 2,5 мг винпоцетина). Данная фиксированная комбинация была назначена пациентам их лечащими врачами на свое усмотрение до включения в настоящую неинтервенционную программу.
Для изучения эффективности и безопасности терапии, проводимой у пациентов группы 1, из пациентов, вошедших в ретроспективный анализ (n = 517), была сформирована такая же по численности группа сравнения (группа 2), в которую вошли больные (n = 70), сопоставимые с пациентами из группы 1 по возрасту (средний возраст 50,1 ± 4,2 года), полу (33 мужчины (47,1%) и 37 женщин (52,9%)), степени тяжести АГ, набору и выраженности факторов риска, а также спектру, давности и тяжести сопутствующих заболеваний (p > 0,05).
Дальнейшее наблюдение авторы проводили за 140 больными: 70 пациентами группы 1 (комбинированная гипотензивная терапия 5 мг эналаприла, 25 мг метопролола тартрата, 0,75 мг индапамида и 2,5 мг винпоцетина) и 70 пациентами группы 2 (стандартная комбинированная гипотензивная терапия в средних дозах один раз в день) (табл. 2).
Сравнение факторов риска и соматического статуса у наблюдаемых пациентов представлено в табл. 3.
После сопоставления тяжести коморбидной патологии с опросником CIRS суммарный балл для пациентов группы 1 составил 9,6, а пациентов группы 2 — 10,8 (p < 0,05). Таким образом, в обеих подгруппах тяжесть коморбидности была примерно одинакова и соответствовала легкой степени.
В связи с основной и сопутствующей патологией все пациенты получали комплексную медикаментозную терапию, которая была сопоставима в основной и контрольной группах (p > 0,05) (табл. 4).
Среднее количество международных непатентованных наименований (МНН), принимаемых одним больным в группе 1 дополнительно к лечению основного заболевания, составило 2,7, а в группе 2 — 2,4 (p > 0,05).
Таким образом, начиная с молодого и среднего возраста у большинства пациентов присутствует ряд факторов риска, которые не воспринимаются ими в качестве начальных проявлений неосложненного течения их потенциальных заболеваний, а также имеются множественные предпосылки для появления феноменов, сопровождающих будущую коморбидную патологию (полипрагмазия, низкий комплайенс, бесконтрольный прием медикаментов, отсутствие самоконтроля симптомов заболеваний).
Методы исследования
Оценку клинических (частота сердечных сокращений (ЧСС)); уровень систолического (САД) и диастолического (ДАД) артериального давления; приверженность к терапии) и лабораторных (общий и биохимический анализ крови) параметров проводили исходно, а также через 6 месяцев (180 дней) и 12 месяцев (360 дней) после подписания информированного согласия. Оценку инструментальных (основные показатели эхокардиографии (ЭХО-КГ); системной артериальной жесткости (индекс CAVI); ультразвуковой допплерографии (УЗДГ) магистральных артерий головы; суточного мониторирования АД (СМАД)) параметров проводили исходно, а также через 12 месяцев (360 дней) после подписания информированного согласия.
Синопсис наблюдательной программы представлен в табл. 5.
Скрининговые процедуры подразумевали общеклинический осмотр больного, сбор жалоб и анамнеза, выявление АГ 1-й и 2-й степени на фоне общепринятых факторов риска (курение, дислипидемия, стрессы, склонность к тахикардии, малоподвижный образ жизни и т. д.), а также получение письменного информированного согласия пациента на участие в настоящем наблюдательном исследовании, включающего указание на минимальную нагрузку на больного.
Сбор информации о нежелательных явлениях начинался с момента подписания пациентом информированного согласия.
Статистическую обработку результатов осуществляли в программах Microsoft Excel и Statistica (version 6.0) с применением следующих статистических методик: вычисление среднего значения, вычисление стандартного отклонения, расчет достоверности и критерия Стьюдента, построение диаграмм и гистограмм.
Различия между группами считали достоверно значимыми при p < 0,05.
Результаты исследования
За 360 дней амбулаторного наблюдения в сравниваемых группах претерпело изменение большинство мониторируемых параметров.
Ни в одной из наблюдаемых групп/подгрупп случаев смерти (от любой причины), а также случаев развития сосудистых «катастроф» зафиксировано не было.
У всех мониторируемых больных АГ за время наблюдения отмечалось отчетливое снижение цифр как систолического (САД), так и диастолического (ДАД) артериального давления (рис. 1 и 2).
Как видно из рис. 1, в группе 1 динамика снижения САД составила 11,1%, (p < 0,05), а в группе 2 — 10,7% (p < 0,05). Различия в снижении САД между наблюдаемыми группами были недостоверными (p > 0,05).
Как следует из рис. 2, в группе 1 ДАД снизилось на 10,3% (p < 0,05), а в группе 2 — на 10,1% (p < 0,05). Различия в снижении ДАД между наблюдаемыми группами были недостоверными (p > 0,05).
Для более полной оценки гипотензивного эффекта сравниваемых комбинаций дважды за год всем пациентам было проведено СМАД, результаты которого представлены в табл. 6.
Как следует из табл. 6, в обеих наблюдаемых группах отмечалось достоверное снижение дневного и ночного САД, ночного ДАД, пульсового АД (ПАД), суточного индекса (СИ) САД и ДАД, индекса времени (ИВ) САД и ДАД, а также дневной вариабельности САД (p < 0,05). Различие между группами по динамике данных показателей было незначительным (p > 0,05).
Таким образом, комбинация эналаприла, индапамида, метопролола тартрата и винпоцетина при правильном режиме дозирования, титрации дозы и соблюдении комплайенса пациентами показала гипотензивный эффект, сопоставимый с таковым большинства современных комбинаций (в т. ч. фиксированных).
Возвращаясь к режиму дозирования, исходно данную комбинацию 56 человек получали в виде приема один раз в день, а 14 пациентов — дважды в день. К 180-му дню было отмечено, что удвоение дозы препарата потребовалось еще 23 больным, а к 360-му дню — еще 21 пациенту. В итоге к завершению наблюдения Гипотэф дважды в сутки принимали 58 (82,9%) из 70 больных, при этом ни у одного мониторируемого пациента не было отмечено резкого или избыточного снижения АД, а также случаев гипотонии, что свидетельствует о безопасности данной комбинации в терапии АГ.
Из 70 пациентов группы 2 к 360-му дню назначенную один раз в день комбинированную гипотензивную терапию пришлось видоизменять 48 больным (68,6%): усиливать утренний прием введением дополнительного приема одного из компонентов терапии вечером и/или делить фиксированную комбинацию на отдельные компоненты, при этом в группе 2 констатировано 3 случая гипотонии (p > 0,05), не повлекших отказ от назначенной терапии, но потребовавших коррекции режима ее дозирования и кратности приема.
Учитывая данные результаты, следует сделать вывод о мягком гипотензивном эффекте препарата Гипотэф, который обусловлен низкими дозами его составляющих, а также, вероятно, об его недостаточной эффективности в качестве препарата выбора у больных, нуждающихся в усилении ранее назначенной гипотензивной терапии, в т. ч. у пациентов с плохо контролируемой, рефрактерной и тяжелой АГ 3-й степени.
Говоря о приверженности к лечению, к 360-му дню наблюдения регулярного приема ранее назначенные гипотензивные препараты продолжали исправно принимать 106 из 140 пациентов с АГ 1-й и 2-й степени. Значит, от проводимой терапии полностью (самостоятельная отмена препарата и/или замена препарата лечащим врачом) или частично (пропущен очередной прием лекарства) в общей сложности отказались 34 пациента: 15 человек (44,1%) из группы 1 и 19 человек (55,9%) из группы 2 (рис. 3).
Как следует из рис. 3, четырехкомпонентная фиксированная комбинация сохраняла комплайенс пациентов на высоком уровне на 11,8% эффективнее большинства двойных комбинаций (p < 0,05).
Таким образом, в отношении комплайенса фиксированные комбинации в очередной раз зафиксировали свое преимущество перед монотерапией, при этом комбинациям с бóльшим количеством компонентов пациенты, по-видимому, отдают большее предпочтение, чем двойным комбинациям, что связано с желанием больных принимать меньшее количество таблеток в день.
За год наблюдения за 140 пациентами случилось 16 неосложненных гипертонических кризов, потребовавших замены терапии: 7 случаев (43,8%) в группе 1 и 9 случаев в группе 2 (56,2%). Экстренная госпитализация по поводу внезапного неосложненного повышения артериального давления потребовалась 2 из 7 пациентов в группе 1 и 3 из 9 пациентов в группе 2. Различия по частоте развития неосложненного гипертонического криза и связанной с ним экстренной госпитализации были недостоверными (p > 0,05).
Как видно из табл. 6, за время наблюдения пациенты обеих групп отмечали снижение ЧСС, однако более отчетливым оно было в группе 1, получавшей Гипотэф (рис. 4).
Как видно из рис. 4, в группе 1 динамика снижения ЧСС составила 13,5% (p < 0,05), а в группе 2 — 6,3% (p > 0,05). Различие степени снижения ЧСС между наблюдаемыми группами составило 7,2% (p < 0,05), что, с большой вероятностью, обусловлено наличием в терапии пациентов группы 1 бета-адреноблокатора.
Таким образом, учитывая достаточный отрицательный хронотропный эффект 25 мг метопролола тартрата, одной из клинико-фармакологических ниш данной комбинации является АГ 1-й и 2-й степени у пациентов со склонностью к тахикардии.
За 360 дней амбулаторного наблюдения дважды у всех пациентов были оценены такие эхокардиографические параметры, как фракция выброса (ФВЛЖ) и масса миокарда левого желудочка (ММЛЖ), их динамика отражена на рис. 5 и 6.
Как видно из данных, представленных на рис. 5 и 6, в зависимости от варианта терапии за время амбулаторного наблюдения (исходно и через 360 дней) практически не различались как годовая динамика ФВЛЖ (увеличение на 2,6% в группе 1 (p > 0,05), увеличение на 3,5% в группе 2 (p > 0,05)), так и ММЛЖ (уменьшение на 0,8% в группе 1 (p > 0,05), уменьшение на 0,6% в группе 2 (p > 0,05)).
Таким образом, фиксированная низкодозовая комбинация эналаприла, индапамида, метопролола тартрата и винпоцетина продемонстрировала собственные кардиопротективные свойства (контроль АД, нормализация вариабельности АД, контроль ЧСС, уменьшение числа экстрасистол, замедление прогрессирования ремоделирования левого желудочка, профилактика систолической дисфункции), сопоставимые с таковыми у основных рациональных гипотензивных комбинаций, доступных для назначения в настоящее время.
В дополнение к инструментальным методам обследования всем пациентам дважды с помощью измерения сердечно-лодыжечного сосудистого индекса (CAVI) была оценена динамика системной артериальной жесткости (рис. 7).
Как видно из кривых на рис. 7, у пациентов с АГ 1-й и 2-й степени и наличием факторов риска сердечно-сосудистых заболеваний и их осложнений, исходные значения индекса CAVI были повышены незначительно. На фоне модификации образа жизни и комбинированной гипотензивной терапии, включающей в себя блокаторы кальциевых каналов, тиазидоподобные диуретики и прочие препараты, способные уменьшать сосудистую жесткость, данный показатель уменьшился в течение года в обеих группах. Так, в группе 1 системная артериальная жесткость снизилась на 22,1% (p < 0,05), а в группе 2 — на 15,3% (p < 0,05). Динамика снижения показателей сердечно-лодыжечного сосудистого индекса между группами составила 6,8% (p < 0,05).
В дополнение к индексу CAVI всем больным за период наблюдения дважды проведена УЗДГ магистральных сосудов головы и шеи (общие сонные артерии (ОСА), среднемозговые артерии (СМА), позвоночные артерии (ПА)), выявившая отсутствие отрицательной церебральной динамики, связанной с сохранением на прежнем уровне их просвета, толщины и структуры стенок, а также линейной скорости кровотока (табл. 7).
Таким образом, Гипотэф при условии коррекции образа жизни и устранения негативного воздействия факторов риска способен оказывать собственные ангио- и церебропротективные эффекты (снижение системной и церебральной артериальной сосудистой жесткости, вазодилатация магистральных сосудов головы и шеи), сопоставимые и превышающие таковые у большинства современных гипотензивных комбинаций, что делает его препаратом выбора для профилактики и базовой терапии когнитивных нарушений.
Изучение лабораторной динамики большинства показателей общего и биохимического анализов крови продемонстрировало безопасность современных гипотензивных препаратов, в т.ч. в составе комбинаций в отношении негативного влияния на них (табл. 8).
Так, на фоне проводимой гипотензивной терапии средние величины показателей, представленных в табл. 8, не претерпели достоверных изменений как внутри какой-либо группы, так и при сопоставлении групп. При этом, как следует из табл. 8, единственным параметром, изменившимся за 360 дней терапии в положительную сторону, была скорость клубочковой фильтрации (СКФ), которая увеличилась на 9,6% в группе 1 (p < 0,05) и на 9,8% в группе 2 (p < 0,05). Различия между группами по динамике СКФ были недостоверными (p > 0,05).
Таким образом, фиксированная комбинация эналаприла, индапамида, метопролола тартрата и винпоцетина показала способность к опосредованной нефропротекции (повышение скорости клубочковой фильтрации), сопоставимой с таковой у широкого круга современных гипотензивных лекарственных средств.
В то же время следует помнить, что почками осуществляется элиминация 20% неизмененного эналаприла (+ до 40% его метаболитов), 5% неизмененного индапамида (+ до 80% его метаболитов) и лишь 5% метопролола тартрата, что, с одной стороны, требует индивидуального подбора и титрации их доз (кроме метопролола тартрата) при лечении больных с почечной дисфункцией, а, с другой стороны, исходно низкие дозы ингредиентов в составе препарата Гипотэф могут являться дополнительным аргументом в пользу его почечной безопасности.
Выводы
У больных среднего (трудоспособного) возраста АГ 1-й и 2-й степени, имеющих множественные факторы риска развития сердечно-сосудистых заболеваний и их осложнений, стартовая терапия фиксированной комбинацией, содержащей низкие дозы эналаприла, индапамида, метопролола тартрата и винпоцетина (в составе препарата Гипотэф, принимаемого внутрь один или два раза в день), [4] обеспечивает должную приверженность к лечению; эффективно и мягко снижает артериальное давление; обладает высоким профилем безопасности в отношении липидного, углеводного и водно-электролитного профилей; а также характеризуется рядом органопротективных свойств, способствующих:
- повышению эффективности начальной терапии ишемической болезни сердца (замедление прогрессирования системной сосудистой жесткости; уменьшение частоты сердечных сокращений);
- профилактике формирования хронической сердечной недостаточности (замедление ремоделирования миокарда левого желудочка; уменьшение количества экстрасистол и других случаев перебоев в работе сердца);
- предотвращению развития хронической ишемии головного мозга (замедление прогрессирования церебрального атеросклероза, обеспечение церебральной вазодилатации);
- первичной профилактике сосудистых «катастроф» (контроль стабильности АД, уменьшение вариабельности АД, контроль частоты сердечных сокращений; повышение СКФ);
- улучшению качества жизни больных (облегчение клинического течения АГ; предупреждение раннего поражения органов-мишеней; уменьшение числа медикаментов, принимаемых в течение дня).
Литература
- Wald D. S., Law M., Morris J. K. et al. Combination Therapy Versus Monotherapy in Reducing Blood Pressure: Meta-analysis on 11000 Participants from 42 Trials // The American Journal of Medicine. 2009, 122, 290–300.
- ESH/ESC Guidelines for the management of arterial hypertension // European Heart Journal. 2013, 34, 2159–2219 (doi:10.1093/eurheartj/eht151);
- Клинические рекомендации «Диагностика и лечение артериальной гипертензии» Российского медицинского общества по артериальной гипертонии, 2013.
- Скотников А. С., Селезнева М. Г., Хамурзова М. А. Обоснованное назначение комбинированной терапии (на примере артериальной гипертензии) как задача клинического фармаколога // Лечащий Врач. 2016, № 2, с. 30–35.
А. С. Скотников*, 1, кандидат медицинских наук
М. А. Хамурзова**
* ФГБОУ ВО Первый МГМУ им. И. М. Сеченова МЗ РФ, Москва
** ГБУЗ ГП № 6 ДЗМ, Москва
1 Контактная информация: skotnikov.as@mail.ru
Купить номер с этой статьей в pdf