В настоящее время лечение хламидийной инфекции вызывает определенные трудности в связи с уникальным жизненным циклом развития возбудителя. Так, репродукция хламидий представляет собой процесс последовательного образования отличающихся по морфологическим и биологическим свойствам двух форм возбудителя: элементарных телец и ретикулярных телец. Элементарные тельца представляют собой мелкие, внеклеточные микроорганизмы, не чувствительные к антибиотикам и метаболически малоактивные. С функциональной точки зрения элементарные тельца напоминают бактериальные эндоспоры, предназначенные для внедрения в новые клетки-мишени, и поэтому являются инфекционной формой хламидий. Ретикулярные тельца представляют собой более крупные, метаболически активные внутриклеточные образования, чувствительные к антибиотикам, интерферону и являющиеся репродуктивной формой существования возбудителя. Учитывая особенности существования хламидий, лечение заболеваний, инициируемых этой инфекцией, должно быть комплексным, включающим назначение этиотропных, симптоматических, иммуномодулирующих средств, эубиотиков. Однако основная роль в лечении хламидийной инфекции все же должна отводиться антимикробным средствам, способным проникать в клетку-мишень и действовать непосредственно на возбудителя [1]. Известны лишь несколько групп антимикробных препаратов, эффективных в отношении хламидий: макролиды, тетрациклины, фторхинолоны и рифампицин [2, 3]. Поскольку при выборе антибиотика для лечения ребенка необходимо учитывать не только эффективность, но и безопасность, спектр перечисленных лекарственных средств сужается до группы макролидов, безвредность которых для детей подтверждена рядом клинических испытаний [4–7]. Кроме этого, препараты данной группы способны накапливаться в очаге воспаления, в инфицированных клетках, нейтрофилах, макрофагах, имеют хорошую переносимость, низкую токсичность, оказывают иммуномодулирующее действие, а некоторые из них, в частности азитромицин, — выраженный постантибиотический эффект.
Важным условием эффективности антихламидийной терапии является выбор адекватных схем применения этиотропных средств, учитывающих длительность воспалительного процесса, вероятность персистирования хламидийной инфекции и фазу репродуктивного цикла, в которой находится возбудитель.
В последние два десятилетия достигнуты определенные успехи в лечении хламидийной инфекции, сопряженной с патологией урогенитального тракта. С этой целью разработаны различные схемы этиотропного лечения, включающие назначение как моноантибиотикотерапии, так и комбинации противомикробных препаратов. Причем длительность курса варьирует от 5 до 21 дня непрерывного приема препарата. Ряд исследователей рекомендует однократный прием антибиотика, при этом констатируя этиологическое излечение у 84% больных [8, 9]. Достаточно высокая эффективность противохламидийного антибактериального лечения, предложенная рядом ученых, вызывает сомнения в корректности организации проведения клинических испытаний, особенно это касается однократного приема антибактериальных средств. При наличии у больного сопутствующих болезней, повышенной чувствительности к химиопрепаратам, выраженной полиантибиотикорезистентности у хламидий некоторые ученые считают целесообразным антимикробную терапию проводить методом «пульс-терапии» по 3 или 4 цикла продолжительностью по 6–7 дней с восстановительным интервалом в 5–6 суток [10].
Информации, касающейся лечения острых синуситов у детей, ассоциированных с хламидийной инфекцией, нет, и вопрос о рациональных методах лечения, в том числе и схемах этиотропной терапии, остается не решенным. Зачастую таким больным с нераспознанной хламидийной инфекцией назначаются стартовые антибактериальные препараты группы пенициллинов, не эффективные в отношении внутриклеточных возбудителей, что способствует трансформации хламидий в L-формы с последующей персистенцией и хронизацией инфекционного процесса. Целью настоящего исследования явилась разработка рациональной и эффективной схемы антибактериального лечения острых хламидийных поражений верхнечелюстных пазух у детей.
Материалы и методы исследования
Всего в исследование было включено 36 детей с острым синуситом, поступивших в ЛОР-отделение ФГБУ НИИМПС, у которых была идентифицирована хламидийная инфекция. Необходимый объем выборки детей, включенных в клиническое испытание, осуществлялся по методике А. Б. Файншмидта, согласно которой группа считается репрезентативной при величине критерия t более или равного 1,96 [11]. Репрезентативный объем основной и контрольной групп, согласно расчетам, составил по 18 человек в каждой из них (t = 1,99).
Эффективность предложенной схемы антибактериального лечения изучалась с применением рандомизированного контролируемого испытания на независимых выборках. Для формирования выборки по таблице случайных чисел дети с выявленной хламидийной инфекцией распределялись в опытную и контрольную группы. Оценка результатов эффективности лечения проводилась на общей группе детей в количестве 28 человек (16 детей в основной, 12 детей в контрольной группах), это связано с неявкой 8 детей на контрольное лабораторное исследование на наличие возбудителя.
Критериями включения в основную и контрольные группы являлись наличие острого верхнечелюстного синусита, ассоциированного с хламидиями, у детей в возрасте от 3 до 13 лет. Диагностика ЛОР-заболеваний проводилась по общепринятой в оториноларингологии семиотике болезней [12]. Критериями исключения являлись сопутствующие заболевания, сочетанная ЛОР-патология, антибактериальное лечение в течение последнего месяца. Родители детей, включенных в клиническое исследование, дали письменное согласие на их участие в испытаниях.
Всем больным проводилась верификация двух видов хламидий: Chlamydia trachomatis и Chlamydophila pneumoniae. Для выявления хламидийной инфекции использовался разработанный нами алгоритм комплексной лабораторной диагностики, включающий два прямых метода индикации возбудителя и один непрямой. Для непосредственного обнаружения поверхностных антигенов хламидийного возбудителя применялся прямой иммунофлюоресцентный анализ с использованием тест-систем «Хламислайд» («Лабдиагностика»). ДНК хламидий определялась методом полимеразно-цепной реакции тест-системой «ВектоХлами-ДНК-ампли» («Вектор-Бест»). В качестве вспомогательного теста диагностики хламидиоза применялся иммуноферментный анализ, позволяющий определить видоспецифические антитела A, M, G против основного белка наружной мембраны возбудителя с использованием тест-системы «ХламиБест-стрип». Материалом для прямой идентификации хламидийного антигена являлись мазки-соскобы со слизистой оболочки носа [13, 14].
Анализируемые качественные признаки представлены в виде относительной частоты и 95% доверительного интервала (ДИ). Для оценки эффективности предложенной схемы антибактериального лечения использовались точный критерий Фишера, определение абсолютных и относительных вероятностей и доверительных интервалов их соотношений.
Результаты исследований и их обсуждение
Детям опытной группы назначалась цикличная полиантибиотикотерапия, заключающаяся в последовательном применении двух антибиотиков: азитромицина и джозамицина. Азитромицин в 1-й день из расчета 10 мг/кг, последующие 4 дня 5 мг/кг 1 раз в день за 1 час до еды. Затем, после 5-дневного перерыва — джозамицин из расчета 40 мг/кг массы ребенка, разделенный на 2 приема, в течение 10 дней. Прерывистый курс полиантибиотикотерапии применялся с учетом особенностей жизненного цикла хламидий. При этом наш расчет строился на уничтожении внутриклеточных ретикулярных телец, затем на элиминации вновь возникших во время перерыва эрадикационной терапии вегетативных форм хламидий из нечувствительных к антибиотикам элементарных телец.
Дети контрольной группы получали один антибиотик джозамицин из расчета 40 мг/кг массы ребенка 2 раза в день в течение 14 дней. Помимо этиологической терапии дети обеих групп получали идентичное комплексное лечение, включающее физиопроцедуры, иммуномодуляторы, эубиотики и местную терапию.
Перед началом медикаментозного лечения всем детям проводилось физиолечение с применением низкоинтенсивного лазерного излучения с использованием аппарата магнитно-инфракрасной лазерной терапии «РИКТА». При воздействии лазерного облучения на ткани достигается улучшение микроциркуляции, раскрываются коллатерали, активизируется трофика, нормализуется нервная возбудимость, а самое важное, повышается чувствительность хламидий к антибиотикам вследствие выхода микроорганизмов из состояния возможной персистенции. При остром синусите детям проводилось облучение в течение 2 минут области передних стенок верхнечелюстных пазух и эндоназальное воздействие в течение 3 минут.
Учитывая стандартные схемы лечения хламидийного поражения урогенитального тракта, а также результаты проведенных нами исследований иммунного ответа у детей с респираторным хламидиозом, указывающие на выраженный дисбаланс в клеточном звене, обусловленный активацией CD8+ Т-лимфоцитов, и недостаточно выраженную активность гуморального иммунитета, в схему лечения были включены иммунокорректоры [15, 16]. Детям старше 4 лет назначался Циклоферон (по схеме), который является индуктором эндогенного интерферона и выполняет важную роль в борьбе с внутриклеточной хламидийной инфекцией. В частности, интерферон является самым сильным активатором макрофагов, усиливает эффекторные функции естественных киллеров, нейтрофилов, повышает резистентность клеток к внутриклеточным микроорганизмам, стимулирует выработку интерлейкинов ИЛ-1, ИЛ-2 и иммуноглобулинов.
Кроме циклоферона в комплекс лечения инфицированных хламидиями детей был включен Иммунал в возрастной дозировке в течение 30 дней. Данный препарат является неспецифическим иммуномодулятором растительного происхождения и обладает противовирусным действием. Входящий в состав Иммунала сок эхинацеи пурпурной стимулирует костномозговое кроветворение, следствием чего является увеличение количества гранулоцитов, повышение активности фагоцитов, клеток ретикуло-эндотелиальной системы печени.
Для повышения барьерного иммунитета и восстановления нарушенной колонизационной резистентности слизистой оболочки верхнего отдела респираторного тракта у детей с верифицированной хламидийной инфекцией нами применялся в течение 14 дней местный иммуномодулятор микробного происхождения — ИРС 19. Этот препарат представляет собой респираторный спрей, содержащий лизаты инактивированных бактерий, включающие антигены основных возбудителей заболеваний верхних дыхательных путей, сохранившие антигенные и иммуногенные свойства. Их действие основано на повышении специфического и неспецифического иммунитета за счет увеличения синтеза секреторных иммуноглобулинов класса А, препятствующих фиксации и размножению патогенных возбудителей, а также на повышении фагоцитарной активности макрофагов и увеличении содержания лизоцима.
Дополнительно в качестве местного лечения, а также с целью механического удаления хламидий нами был использован еще один препарат, обладающий антихламидийной активностью, — 0,1% раствор мирамистина, которым осуществлялось промывание носовых ходов, полоскание глотки 1 раз в день в течение 14 дней. Помимо противомикробного действия мирамистин повышает функциональную активность иммунных клеток, стимулирует местный неспецифический иммунный ответ, снижает резистентность микроорганизмов к антибиотикам, обладает противогрибковым действием.
Учитывая факт достаточно длительного применения антибиотиков, с целью профилактики и восстановления возможных дисбиотических нарушений в микрофлоре пищеварительного тракта всем детям назначался пробиотик — Линекс по 1 капсуле 3 раза в день, 14 дней.
Дополнительно в комплекс лечения детей с острым гнойным воспалением пазух входило проведение оториноларингологических лечебных мероприятий (пункции, промывание носа методом перемещения по Проетцу и пр.).
В ходе проводимого клинического испытания осложнения и побочные эффекты не были выявлены ни у одного из пациентов. Положительный результат лечения оценивался по данным бактериологической эрадикации хламидий.
В таблице сопряженности представлены результаты рандомизированного контролируемого исследования по изучению эффективности поли- и моноантибиотикотерапии у детей с острым синуситом.
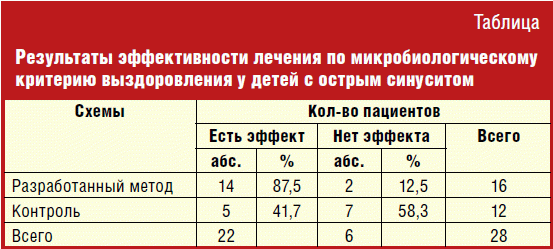
У детей, получавших один антибиотик, эффективность лечения оказалась значительно ниже, чем у детей, получавших полиантибиотикотерапию. Так, микробиологическое выздоровление у детей, у которых в комплексное лечение входил только один джозамицин, имело место у 41,7% (95% ДИ оставил 16,5–69,4). Тогда как у детей, получавших азитромицин и джозамицин, проводимая терапия оказалась эффективной у 87,5% (95% ДИ 67,5–98,7). Проверка нулевой гипотезы о вероятности отрицательного результата лечения разработанным методом, учитывая объем выборок, осуществлялась с применением точного критерия Фишера. Результаты теста показали, что с 99,9% доверительной вероятностью (р = 0,01) следует принять альтернативную гипотезу о существовании различий между опытной и контрольной группами (р = 0,001).
Абсолютная вероятность получения положительного результата в опытной и контрольной группах составила соответственно 0,88 и 0,42. Разность относительных частот и относительная вероятность составила соответственно 0,46 (терапевтический эффект) и 2,2.
Различия между группами определялись тремя способами: расчетами ДИ для разности абсолютных вероятностей, ДИ для отношения относительной вероятности и ДИ отношения шансов, которые составили соответственно 0,12–0,80, 1,02–4,35 и 1,38–69,71.
Так как ДИ для разности абсолютных вероятностей не включает ноль, а ДИ для отношения относительной вероятности и отношения шансов правее единицы, следовательно, различия между группами статистически значимые.
Выводы
- Лечение хламидийных поражений околоносовых пазух у детей должно быть комплексным и включать применение антимикробных препаратов, иммуномодуляторов, местного лечения, физиопроцедур, пробиотиков.
- Результаты проведенного контролируемого клинического испытания показали высокую эффективность и целесообразность использования в практической медицине цикличной полиантибиотикотерапии макролидами острого верхнечелюстного синусита, ассоциированного с хламидийной инфекцией, у детей, позволяющей добиться клинико-микробиологического выздоровления в 87,5% случаев.
- С учетом того, что прямые тесты на хламидийные антигены и ДНК остаются положительными в течение 1,5 месяцев после лечения, то этиологический контроль выздоровления должен осуществляться также через 1,5 месяца после проведенной антихламидийной терапии.
- Hammerschlag M. R. Antimicrobial susceptibility and therapy of infections caused by chlamydia pneumoniae // Antimicrob. Agents Chemother. 1994. V. 38. P. 1837–1878.
- Страчунский Л. С., Козлов С. Н. Современная антимикробная химиотерапия: Рук-во для врачей. М.: Боргес, 2002. 429 с.
- Аверьянов А. В. Хламидийная и микоплазменная инфекция при патологии нижних дыхательных путей // Лечебное дело. 2009. № 4. С. 52–62.
- Таточенко В. К., Федоров А. М. О клиническом многообразии респираторного хламидиоза у детей первых месяцев жизни // Актуальные вопросы диагностики и лечения хламидийных инфекций: матер. всесоюз. совещ. М., 1990. С. 34–36.
- Карбон К., Пул М. Д. Значение новых макролидов при лечении внебольничных инфекций дыхательных путей: обзор экспериментальных и клинических данных // Клиническая микробиология и антимикробная терапия. 2000. № 1. С. 47–58.
- Самсыгина Г. А., Охлопкова К. А. Кларитромицин в лечении острых бактериальных бронхитов у детей раннего возраста // Педиатрия. 2001. № 1. С. 47–49.
- Moulder J. W. Genus Chlamydia // Bergey, s Manual of Bacteriology. 2000. V. 1. P. 729–739.
- Чеботарев В. В. Урогенитальный хламидиоз: современные проблемы диагностики, патогенеза, лечения // Венерология. 2004. № 1. С. 43–48.
- Гомерг М. А., Поздняков О. Л., Соловьев А. М. Урогенитальная хламидийная инфекция: лечить или не лечить? // Consilium medicum Ucraina. 2008. № 4. С. 8–11.
- Лобзин Ю. В., Ляшенко Ю. И., Позняк А. Л. Хламидийные инфекции. СПб.: Фолиант, 2003. 396 с.
- Файдшмидт А. Б. Руководство к практическим занятиям. Красноярск, 1976. 75 с.
- Солдатов И. Б., Гофман В. Р. Оториноларингология. СПб.: ЭЛБИ, 2001. 472 с.
- Капустина Т. А., Парилова О. В., Кин Т. И., Маркина А. Н. Лабораторная диагностика хламидийной инфекции верхнего отдела респираторного тракта // Сибирский медицинский журнал. 2010. Т. 96. № 5. С. 23–26.
- Капустина Т. А., Парилова О. В., Маркина А. Н., Кин Т. И. Хламидийная инфекция верхнего отдела респираторного тракта. Новосибирск: Наука, 2012. 139 с.
- Ершов Ф. И., Романцева В. Г. Циклоферон: от эксперимента в клинику. М., 1997. 89 с.
- Белова Е. В., Капустина Т. А., Манчук В. Т., Коленчукова О. А. Эпидемиологическая и клинико-патогенетическая характеристика хронического аденоидита, ассоциированного с хламидийной инфекцией // Бюл. СО РАМН. 2008. № 1. С. 101–105.
Е. В. Белова1, кандидат медицинских наук
Т. А. Капустина, доктор медицинских наук
О. В. Парилова, кандидат медицинских наук
А. Н. Маркина, кандидат медицинских наук
* ФГБУ НИИ МП Севера СО РАМН, Красноярск
1 Контактная информация: belova.ev@bk.ru
Купить номер с этой статьей в pdf