Согласно современным представлениям, питание — это синхронизация взаимодействия и ассимиляции нутриентов по всей трофической цепи организма — доставка и усвоение питательных веществ клетками организма, удаление продуктов жизнедеятельности, ресинтез веществ, уравновешенность процессов (анаболизм и катаболизм) и т. д. [1, 2]. Поэтому вопросы адекватного питания как здоровых детей раннего возраста, так и детей с синдромом недостаточности питания широко обсуждаются и являются актуальными. И в настоящее время уже определены количественные и качественные составляющие рационов питания, учитывающие возраст и степень тяжести недостаточности питания.
Для нормального жизнеобеспечения ребенку необходимо ежедневно с рационом питания получать более 75 нутриентов, 45–50 из которых являются незаменимыми.
Обмен веществ в организме — это единый процесс, который поддерживает равновесие, перераспределяя потоки питательных веществ, и может обеспечивать свои энергетические и пластические потребности при отсутствии поступления тех или иных нутриентов. Установлено, что углеродные цепи глюкозы могут трансформироваться в углеродные цепи всех эссенциальных аминокислот. При дефиците белка в рационе из углеводов в тканях, в результате химических реакций, могут синтезироваться аланин, аспарагиновая и глутаминовая кислоты. Из белков путем глюконеогенеза могут образовываться углеводы. Ряд аминокислот может трансформироваться в жирные кислоты, а глицерин, образующийся при расщеплении жиров, в свою очередь, может превращаться в углеводы [1].
Важно отметить, что постоянный избыток или, напротив, недостаток какого-либо нутриента, особенно в рационе питания ребенка, может приводить к негативным последствиям. Например, избыток белка в рационе ведет к снижению его утилизации, накоплению аммиака и азотистых продуктов, что способствует развитию ацидоза. Недостаточное поступление в организм ребенка питательных веществ и, как правило, уменьшение общей калорийности рациона способствует развитию или первичной трофической (алиментарной) недостаточности, или вторичной, обусловленной дисбалансом между неучтенными повышенными потребностями детского организма при болезни и поступлением питательных веществ.
Как отмечено ранее, первичная алиментарная недостаточность формируется при нарушениях качества и режима вскармливания. Неправильное вскармливание подразумевает неадекватно подобранное питание в соответствии с возрастом или индивидуальными потребностями ребенка. У детей, получающих грудное вскармливание, наиболее частой причиной недокорма является гипогалактия у матерей [3].
Проблемы с приемом пищи нередко отмечаются у детей с нарушенным актом сосания (например, при пороках развития лицевого скелета), глотания (при синдроме мышечной слабости), обильных срыгиваниях и рвотах, критических ситуациях (при утрате сознания).
В настоящее время в клинической практике редко встречается первичная алиментарная недостаточность питания. Чаще — это вторичная недостаточность питания, обусловленная повышенным расходом энергии, нарушением ассимиляции или метаболизма нутриентов вследствие тяжелых врожденных или приобретенных патологических состояний (инфекционные заболевания, наследственные или врожденные энзимопатии, эндокринные заболевания, органическая патология ЦНС и др.), травм [3].
В этой связи при трофической недостаточности питание не может быть интерпретировано как простое снабжение организма определенным набором нутриентов, так как это гораздо более сложный процесс, в котором пищеварительная система осуществляет активные взаимодействия с другими органами и системами организма.
Важно подчеркнуть, что в основе трофической недостаточности лежат нарушения белково-энергетического, водно-электролитного, витаминного гомеостаза — сложнейшего процесса взаимодействия жизненно необходимых питательных веществ с рядом гормонов, регуляторных веществ, приводящего к нарушению доставки питательных веществ к органам-мишеням и их усвоения ими [2].
Патогенез трофической недостаточности определяется постепенным нарастанием степени нарушений в обмене веществ на фоне дефицита питательного субстрата и изменениями в трофической цепи.
Первоначально истощаются запасы субстратов, несущих энергетическую функцию, — углеводов, а затем — жиров. Следующим этапом является катаболизм белка мышечной ткани. Важно отметить, что при дефиците белков плазмы внутриклеточные белки могут быстро преобразовываться в аминокислоты под влиянием внутриклеточных лизосомальных пищеварительных ферментов [1]. Исключение составляют лишь белки ядра клетки и хромосом, а также структурные белки (например, белки коллагеновых волокон и сократительные белки мышц). Аминокислоты активно используются для синтеза крайне необходимых транспортных, иммунных, острофазных и некоторых других белков, а также расходуются на энергетические нужды. В условиях энергетического голода часть белков метаболизируется до углеводов (глюконеогенез), а часть до жирных кислот. При катаболической направленности обменных процессов энергия (глюкоза) используется преимущественно мозгом, нарушается инсулинозависимый рост тканей, что является дополнительным фактором в снижении массы тела и замедлении роста ребенка.
При продолжающемся отсутствии коррекции трофической недостаточности организм приспосабливается к недостатку нутриентов и переходит на режим максимальной экономии энергии путем замедления распада белка и жира. При этом период полужизни белков увеличивается (например, период полужизни альбумина удваивается). Нарушения метаболизма белка приводят к нарушениям в функционировании иммунной системы в связи с изменением синтеза иммуноглобулинов, а также антиоксидантной активности, сопровождающейся повреждением клеточных мембран. Нарушению строения и функционирования клеточных мембран способствует возникающее ухудшение ассимиляции тканями триглицеридов и, соответственно, неэстерифицированных жирных кислот, снижение концентрация фосфолипидов и холестерина в крови: развивается дефицит эссенциальных жирных кислот. Дальнейшие нарушения связаны со снижением уровня короткоживущих белков крови (транстиретина, трансферрина, церулоплазмина и др.), затем уменьшается концентрация альбумина и общего белка в крови [3].
Недостаточность питания формирует дефицит не только основных нутриентов, но и многих эссенциальных веществ — витаминов, макро- и микронутриентов. В результате развиваются такие дефицитные состояния, как остеопения, анемия и др. [4]. При этом изменения, происходящие при трофической недостаточности во всех органах и системах организма, в том числе и в желудочно-кишечном тракте, усугубляют ситуацию. Так, возникает дистрофия и атрофия слизистой оболочки кишечника, что сопровождается нарушением внутриполостного и мембранного пищеварения, нарушается моторика желудочно-кишечного тракта, страдает местный иммунитет, возможна контаминация условно-патогенной кишечной микрофлоры из дистальных в проксимальные отделы кишечника. Все эти изменения ухудшают всасывание и усвоение пищи.
Таким образом, результатом продолжительной недостаточности питания является снижение массы тела и скорости роста, а также отставание в психомоторном развитии, задержка речевых и когнитивных навыков и функций, высокая инфекционная заболеваемость вследствие снижения иммунитета, что в свою очередь усугубляет расстройство питания [3].
В отечественной педиатрии, говоря о трофической недостаточности у детей первого года жизни, используют термин «гипотрофия». Однако при постановке диагноза гипотрофии врачи руководствуются обычно только отклонениями в антропометрических данных ребенка (массоростовых показателях), по которым сложно оценить степень нарушений, происходящих в организме. Понятие трофической недостаточности наиболее широкое и включает обязательную оценку соматического и висцерального пула белка (определение в крови уровня короткоживущих белков, альбумина, общего белка, абсолютного числа лимфоцитов). Соматический пул белка отражает состояние мышечной массы и определяется путем измерения окружности плеча, толщины кожно-жировых складок, вычислением окружности мышц плеча [5]. Перечисленные показатели достаточно информативны для оценки состояния мышечной массы и жировых депо и позволяют диагностировать недостаточность белка или белка и энергии, а также предположить наличие дистрофических изменений внутренних органов по величине содержания жира. К сожалению, центильные таблицы по таким параметрам, как окружность плеча, толщина кожных жировых складок, разработаны лишь для детей с года жизни. Помимо соматометрических показателей для оценки состояния соматического пула белка применяется суточная экскреция креатинина с мочой (показатель отражает тощую массу). Однако, как и другие методы определения состава тела у детей раннего возраста (биоимпедансометрия, денситометрия), они не являются рутинными. Поэтому основными критериями диагностики трофической недостаточности у детей первого года являются клинические (оценка соматического состояния, кожных покровов, слизистых, тургора тканей и т. д.); среди соматометрических — массоростовые параметры; данные лабораторных исследований (клинический и биохимический анализ крови, мочи, копрограмма) и морфофункциональные критерии (ультразвуковое исследование, фиброэзофагогастродуоденоскопия и т. п.).
Дефицит массы тела (ДМТ) определяют по формуле:
(РМТ – ФМТ)/(РМТ × 100%),
где РМТ — рекомендуемая масса тела, ФМТ — фактическая масса тела.
При дефиците массы тела 10–20% диагностируют легкую, 20–30% — среднетяжелую, более 30% — тяжелую недостаточность питания.
Тактика диетотерапии и метаболической терапии напрямую зависит от степени выявленных нарушений и тяжести состояния ребенка. Необходимо подбирать оптимальное питание и проводить коррекцию нарушенной трофической цепи — оптимизировать процессы пищеварения и всасывания, сохранить кишечный микробиоценоз, обеспечить должный внутриклеточный метаболизм, активировать анаболические процессы [2].
При выборе питания следует отдавать предпочтение грудному молоку, а при его недостатке или отсутствии — современным смесям, сбалансированным по составу основных пищевых веществ, макро- и микронутриентам, обогащенных нуклеотидами, полиненасыщенными жирными кислотами, пре- и пробиотиками. Так как указанные факторы питания способствуют восстановлению нарушенной трофической цепи.
Например, нуклеотиды участвуют в синтезе нуклеиновых кислот, построении АТФ, положительно влияют на обмен липидов и, что очень важно в условиях недостаточности питания, — повышают уровень секреторного IgA, ускоряют созревание эпителия тонкой кишки. Показано улучшение соматометрических показателей (масса тела, рост, окружность головы) у детей с задержкой внутриутробного развития при вскармливании смесями, содержащими нуклеотиды [4].
Полиненасыщенные жирные кислоты — эйкозапентаеновая и докозагексаеновая, обладают противовоспалительным эффектом, позволяют уменьшить спазм сосудов, агрегацию тромбоцитов, улучшить перфузию кишечника, повысить иммунную защиту [6].
Обеспечение организма нутриентами достигается как за счет активного пищеварения, так и синтеза бактериальной флорой кишечника целого ряда незаменимых регуляторных веществ. Облигатная бактериальная флора желудочно-кишечного тракта необходима для поддержания трофического гомеостаза, так как участвует в синтезе витаминов, аминокислот, регуляторных пептидов [7]. Кроме того, поступление нутриентов во внутреннюю среду организма зависит от состояния пристеночного пищеварения и возможностей их всасывания, а также оптимальной моторно-эвакуаторной функции желудочно-кишечного тракта. Поэтому важно проведение деконтаминации кишечника ребенка при наличии патогенных и условно-патогенных бактерий и поддержание индигенной нормофлоры вводимыми в состав смеси пре- и пробиотическими факторами.
При назначении диетотерапии следует учитывать количество вводимых белковых и небелковых килокалорий для того, чтобы достичь должной ассимиляции белка и активации оптимального белкового синтеза. При этом необходимо обеспечивать на 1 г вводимого азота 150 небелковых килокалорий или на 1 г вводимого белка — 30 небелковых килокалорий. Среди небелковых килокалорий соотношение углеводных и липидных килокалорий колеблется от 70:30 до 50:50 [2]. Особенно это следует учитывать при проведении парентерального питания. При отсутствии должного энергетического обеспечения организм через глюконеогенез использует циркулирующие в крови аминокислоты не для пластических целей, а в качестве источника энергии. В свою очередь, дефицит энергии усиливает белковый катаболизм. Большинство современных смесей для питания детей первого года жизни отвечают данным требованиям.
Для детей с недостаточностью питания, получающих искусственное вскармливание, важно наличие в составе смеси легкоусвояемых нутриентов, подобных грудному молоку. Так, в состав жирового компонента смесей на основе козьего молока Kabrita® Gold (1, 2, 3 формулы) включен DigestX® — липидный комплекс с высоким содержанием в нем пальмитиновой кислоты в sn-2-позиции (42%) в молекуле глицерола, аналогично грудному молоку. Дополнение смеси DigestX® способствует улучшению усвоения жира путем уменьшения экскреции жирных кислот с калом, а также уменьшению экскреции кальция с калом, что ведет к улучшению усвоения кальция. Благодаря наличию пальмитиновой кислоты в sn-2-позиции, уменьшается содержание кальциевых солей жирных кислот в кале — облегчается пищеварение и формируется мягкий стул. Эффективность и безопасность DigestX® подтверждена клинически [8, 9].
Таким образом, модификация жирового состава смеси способствует ее легкой и лучшей усвояемости, что важно для пациентов с недостаточностью питания. Cостав белка смеси на основе козьего молока (Kabrita® Gold) отличен от коровьего, так как имеет низкое содержание альфа-s1-казеина и высокое — бета-казеина. Известно, что альфа-s1-казеин определяет уровень коагуляции белка, поэтому белок козьего молока образует мягкий, легко перевариваемый сгусток в желудке, подобный сгустку белка грудного молока [10]. Смеси Kabrita® Gold являются сывороткодоминирующими. Установлено, что смеси, обогащенные сывороточными белками, способствуют более оптимальному составу кишечной микрофлоры, чем казеиндоминирующие смеси, реже вызывают срыгивания и другие функциональные нарушения со стороны желудочно-кишечного тракта [11].
В смесях Kabrita® Gold помимо легкоусвояемого белка козьего молока и жира, дополненного DigestX®, содержатся пребиотики GOS и FOS, бифидобактерии ВВ-12, нуклеотиды, длинноцепочечные полиненасыщенные жирные кислоты — докозагексаеновая и арахидоновая кислоты, витамины, макро- и микронутриенты.
По данным Т. В. Белоусовой, при применении смеси на основе козьего молока Kabrita® Gold (1 формула) у детей с недостаточностью питания легкой степени в постнатальном периоде и с исходной гипотрофической задержкой внутриутробного развития I степени, с наличием гастроинтестинальной дисфункции (срыгивания, метеоризм), была достигнута положительная динамика в нутритивном статусе в сравнении с показателями при использовании формул на основе сывороточных белков коровьего молока [12]. В группу исследования включен 21 ребенок первых 2–3 месяцев жизни. Пациенты изначально получали заменители грудного молока на основе сывороточных белков коровьего молока, базовые формулы. До момента назначения смеси Kabrita® Gold среднесуточные прибавки в массе тела у детей на предшествующей исследованию неделе отличались от средних значений и составляли в среднем не более 15 г, что послужило основанием смены питания. Уже к концу первой недели приема смеси Kabrita® Gold среднесуточные прибавки у них возросли до 25 г, а к концу 2-й недели составили в среднем 35 г (рис.).
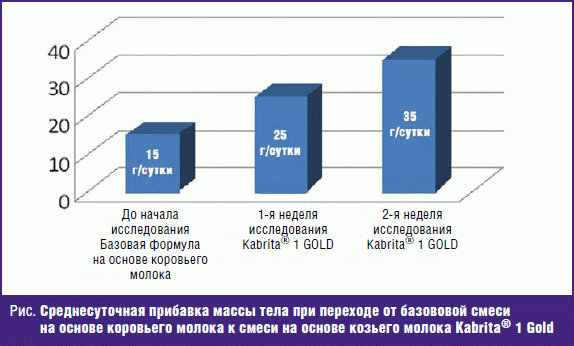
Выраженный метеоризм и срыгивания (1–2 балла) отмечались у пациентов до начала применения смеси Kabrita® Gold. Тогда как в динамике наблюдалось уменьшение степени выраженности и купирование симптомов на второй неделе использования смеси, при этом объем потребляемого продукта увеличился в среднем в 1,3 раза. Исследователь отмечает, что до перехода на данную смесь эти дети нуждались в назначении прокинетиков и препаратов, содержащих симетикон, и уже к концу первой недели приема смеси указанные препараты были отменены. Кроме того, при опросе матерей относительно толерантности к питанию и комфортности в поведении детей были получены положительные отзывы. Таким образом, молочная смесь на основе козьего молока Kabrita® Gold, содержащая пре- и пробиотики, может быть рекомендована в качестве базового питания детей с периода новорожденности и детей раннего возраста, в том числе при умеренном дефиците питания, как продукт с хорошей переносимостью при отсутствии грудного молока у матери [12].
При среднетяжелой и тяжелой недостаточности питания требуется высококалорийная/высокобелковая диета [3]. В данной ситуации возможно использование смесей с более высоким содержанием белка, например, смесей для недоношенных и маловесных детей, а также специализированных продуктов энтерального питания для детей раннего возраста. При выявлении нарушений расщепления/всасывания пищевых ингредиентов целесообразно применение лечебных продуктов — смесей на основе высокогидролизованного молочного белка со среднецепочечными триглицеридами [4].
При назначении диетотерапии рекомендуется постепенное увеличение пищевой нагрузки с учетом толерантности ребенка к пище. При недостаточности питания легкой степени расчет питания проводится на ДМТ. Необходимо также учитывать наличие заболеваний у ребенка, при которых требуется повышение энергетической ценности рациона питания (например, бронхолегочная дисплазия, врожденные пороки сердца и т. д.).
Алгоритм пошаговой коррекции недостаточности питания среднетяжелой степени выглядит следующим образом: в первые 2–5 дней (период адаптации) расчет питания проводится на ФМТ, количество кормлений увеличивается на 1–2. Затем следует период репарации (5–7 дней), когда расчет питания проводится на ДМТ. При достижении ребенком ДМТ дальнейшее питание назначается в соответствии с возрастом и заболеванием. При отсутствии ДМТ рекомендуется период усиленного питания (повышение калорийности рациона до 130–145 ккал/кг/сут, белка до 4,5 г/кг/сут) на 1–2 месяца [3].
Питание ребенок получает через рот при сохранном сосательном рефлексе и глотании. В тяжелых случаях (при тяжелой недостаточности питания) доставка грудного молока/смеси осуществляется через зонд и/или дополняется парентеральным питанием.
Начиная с периода репарации целесообразна заместительная ферментотерапия препаратами поджелудочной железы, коррекция железодефицитной анемии, рахита, поливитаминные комплексы и средства, положительно влияющие на обменные процессы.
Таким образом, при недостаточности питания у детей раннего возраста необходима продуманная комплексная метаболическая и диетологическая коррекция, способствующая восстановлению нарушенной трофической цепи организма и, в итоге, достижению положительного результата.
Литература
- Циганенко А. Я., Жуков В. И., Мясоедов В. В. Клиническая биохимия. М.: Триада-Х, 2002, 506 с.
- Руководство по клиническому питанию. Под ред. Луфта В. М., Багненко С. Ф., Щербука Ю. А. СПб, 2010. 428 с.
- Национальная программа оптимизации вскармливания детей первого года жизни в Российской Федерации. Под ред. Баранова А. А., Тутельяна В. А. М., 2010. 68 с.
- Клиническая диетология детского возраста. Рук-во для врачей. Под ред. Т. Э. Боровик, К. С. Ладодо. М.: Медицина, 2008. 606 с.
- Углицких А. К. Комплексная оценка пищевого статуса у детей в стационаре // Анестезиол. и реаниматол. 2005. № 2, с. 52–57.
- Сalder P. C. ω-3 fatty acid, inflammation and immunity-relevance to postsurgical and critically ill patients // Lipids. 2004; 39: 1147–1161.
- AFSSA. Rapport du groupe de travail «Alimentation infantile et modification de la flore intestinale». Juin 2003.
- Lopez-Lopez A. The influence of dietary palmitic acid triacylglyceride position on the fatty acid, calcium and magnesium contents of at term newborn faeces // Early Hum Dev, 2001. 65 Suppl: p. S83–94.
- Kennedy K. Double-blind, randomized trial of a synthetic triacylglycerol in formula-fed term infants: effects on stool bio- chemistry, stool characteristics, and bone mineralization // Am J Clin Nutr. 1999. 70 (5): p. 920–7.
- Juarez M., Ramos M. Physico-chemical characteristics of goat milk as distinct from those of cow’s milk. Int // Dairy Fed Buffl. 1986, № 202, p. 54–67.
- Детское питание. Рук-во для врачей. Под ред. В. А. Тутельяна, И. Я. Коня. М.: ООО «Медицинское информированное агенство», 2009. 952 с.
- Белоусова Т. В. Оценка клинической эффективности и переносимости новой молочной смеси на основе козьего молока // Лечащий Врач. 2014. № 6, с. 87–88.
О. Н. Комарова1, кандидат медицинских наук
А. И. Хавкин, доктор медицинских наук, профессор
ГБОУ ВПО РНИМУ им. Н. И. Пирогова МЗ РФ, Москва
1 Контактная информация: komarovadoc@yandex.ru
Купить номер с этой статьей в pdf