Хроническая ежедневная головная боль (ХЕГБ) беспокоит пациентов более 15 дней в месяц на протяжении более трех месяцев. ХЕГБ не является самостоятельной нозологической формой, а представляет синдром, включающий различные первичные и вторичные головные боли (ГБ). Распространенность ХЕГБ в популяции составляет примерно 3–5%, а в специализированных клиниках доля пациентов с ежедневной или почти ежедневной ГБ достигает 70–80%. Заболевание обуславливает значительное снижение качества жизни, нарушает социальную активность пациентов и их трудоспособность, а также представляет собой сложную проблему с точки зрения терапии.
Самыми частыми формами ХЕГБ являются хроническая мигрень (ХМ), хроническая ГБ напряжения (ХГБН) и абузусная ГБ. ХЕГБ в большинстве случаев является осложнением длительно существующей эпизодической ГБ и лишь у немногих пациентов с момента своего дебюта принимает ежедневный или почти ежедневный характер.
Среди факторов хронизации ГБ описаны ожирение, женский пол, исходно частая ГБ (более 1 раза в неделю), чрезмерное употребление анальгетических препаратов (более 10 дней в месяц) и эмоциональный стресс. У более чем половины пациентов с ХЕГБ выявляются нарушения сна и расстройства настроения депрессивного и тревожного характера.
Патогенез ХЕГБ в настоящее время изучен недостаточно. Предполагаются два основных механизма, которые могут лежать в основе хронизации разных форм ГБ — сенситизация ноцицептивных структур и снижение активности антиноцицептивных отделов центральной нервной системы (ЦНС).
При мигрени периферическая сенситизация происходит в сенсорных нейронах, иннервирующих внутримозговые сосуды и оболочки. Центральная сенситизация (ЦС) описана в спинномозговом ядре тройничного нерва, куда стекаются импульсы от мозговых оболочек и кожи лица. Многие пациенты испытывают неприятные ощущения во время и между приступами мигрени при бритье, расчесывании волос, ношении очков и украшений. Ощущение боли при воздействии неболевого раздражителя обозначается как аллодиния, которая в настоящее время часто коррелирует с центральной сенситизацией. Различают статическую (от давления или укола) и динамическую (от поглаживания) аллодинию. При дальнейшем течении некупированного приступа мигрени включаются более центральные отделы ноцицептивной системы. Уже при активации таламуса аллодиния становится двусторонней, ее зона может с головы и лица переходить на руку. При эпизодической мигрени в течение 72 часов включаются антиноцицептивные системы, которые приводят к купированию мигренозного приступа.
Со временем признаки ЦС исчезают не полностью после окончания приступа, и постепенно формируется стабильная ЦС, которая поддерживает боль в хроническом состоянии. При этом нейроны в ЦНС становятся слабо или совсем нечувствительными к периферическим воздействиям. На этом этапе терапевтические воздействия должны быть направлены на усиление нисходящих антиноцицептивных влияний — on/off-нейроны в околоводопроводном сером веществе (ОСВ), антиноцицептивная функция которых нарушена при ХЕГБ.
В настоящее время для профилактики ГБ активно используются антидепрессанты. Показано, что анальгетическое действие трициклических антидепрессантов (ТЦА) не зависит от их антидепрессивного действия и обусловлено их сочетанным серотонинергическим и норадреналинергическим действием. В то же время более безопасные селективные ингибиторы обратного захвата серотонина (СИОЗС) недостаточно эффективны в лечении мигрени и ХГБН [21].
Венлафаксин, структурно новый антидепрессант, по химической структуре отличен от ТЦА, однако также угнетает обратный захват серотонина (5-HT) и норадреналина. Кроме того, по сравнению с амитриптилином препарат действует более специфично на эти рецепторы. Венлафаксин облегчает головную боль так же эффективно, как и ТЦА, но вызывает гораздо меньше побочных эффектов. В ходе двойного слепого исследования профилактического эффекта СИОЗС и венлафаксина при мигрени было показано, что процент пациентов, у которых было достигнуто значительное улучшение в группе венлафаксина, превысил этот показатель в группе СИОЗС.
Эффективность венлафаксина неоднократно доказана в исследованиях пациентов с различными формами нейропатической боли: при диабетической полинейропатии, нейропатии после химиотерапевтического лечения и др. Проведен также ряд исследований профилактического действия венлафаксина при хронической мигрени и ХГБН.
Целью настоящей работы явилось изучение феномена ЦС при ХЕГБ, ее роли в хронификации ГБ и эффективности венлафаксина для ее урежения.
Материал. В исследовании приняли участие 69 пациентов с ХЕГБ и 30 пациентов с эпизодической мигренью (ЭМ) в соответствии с критериями ICHD-2, а также 15 участников группы контроля с ГБ не чаще 1 дн./мес. Группа ХЕГБ была представлена пациентами с ХМ, ХГБН и пациентами со смешанными формами ГБ.
Методы исследования. Всем пациентам была предложена анкета для изучения демографических данных, анамнеза и клинической картины головной боли. Кроме того, пациенты заполняли анкету для изучения симптомов аллодинии.
Статическая аллодиния (СА) исследовалась при помощи альгометра в 5 парах симметричных точек на голове и шее (лоб, висок, темя, задняя поверхность шеи, плечо/трапециевидная мышца).
Порог боли от давления определяется как сила давления, которая необходима для вызывания субъективно неприятного/болезненного ощущения. Использовался ручной альгометр (Commander Algometer™, JTech). В каждой точке выполнялось два последовательных измерения с интервалом в 20 секунд. Для анализа использовалось среднее значение.
СА также измерялась при помощи уколов механическим стимулятором (Neuropen®, Owen Mumford) с нанесением силы укола в 40 г в тех же точках. Выраженность боли или неприятного ощущения измерялась по 100-бальной шкале.
Феномен wind-up (временная суммация боли) исследовался при помощи нанесения серии из 10 уколов на участок кожи площадью 1 см2 на лбу, виске и шее стимулятором Neuropen®. Участники исследования оценивали силу единичного укола и всей серии.
Мигательный рефлекс (МР) вызывался при помощи электрической стимуляции правого надглазничного нерва, подаваемой через поверхностные электроды диаметром 5 мм. Катод располагался над наглазничным отверстием, а анод приблизительно на 2 см выше на коже лба. Наносились одиночные электрические стимулы прямоугольной формы длительностью 0,2 мс с произвольными интервалами не менее 30 секунд для минимизации габитуации и регистрировались четкие R1-, R2- и R3-компоненты мигательного рефлекса. В работе анализировались пороги возникновения позднего компонента R3, для которого описан полисинаптический путь, проходящий от ствола головного мозга до спинального ядра тройничного нерва и затем в латеральную ретикулярную формацию.
Ноцицептивный флексорный рефлекс (НФР) регистрировался при стимуляции правого икроножного нерва трендами длительностью 20 мс и частотой 300 Гц с произвольными интервалами не менее 15 секунд. Катод располагался в проекции нерва, а анод на 2 см ниже в области латеральной лодыжки. Референтный электрод располагался над сухожилием двуглавой мышцы бедра, а заземляющий — на середине голени. Регистрировался порог возникновения R3-ответа и порог субъективной болевой чувствительности (когда пациент болевое ощущение оценивал на 5 баллов по 10-бальной шкале ВАШ). Также рассчитывалось соотношение порог боли/порог рефлекса. R3-компонент замыкается через ретикулярную формацию ствола мозга.
Результаты анализировались при помощи компьютерного пакета Statistica (U-тест Манна–Уитни для сравнения групп, корреляционный тест Спирмена, точный тест Фишера для сравнения пропорций, например, распространенности аллодинии). Все показатели приведены в формате Х ± SD.
Результаты исследования
1. Клинические и демографические характеристики пациентов
Группа ХЕГБ была представлена 28 пациентами с ХМ, 31 пациентом с ХГБН и 10 пациентами со смешанными формами ГБ (ХМ или ХГБН в сочетании с цервикогенной ГБ) в соответствии с критериями ICHD-2. В группу вошли 57 женщин и 12 мужчин, средний возраст 40 лет. Средняя частота ГБ составила 25 дн./мес, сила боли 7 баллов. При общей длительности ГБ в анамнезе в 19 лет, наши пациенты страдали ХЕГБ в среднем 6 лет. О злоупотреблении анальгетическими препаратами сообщили 33% пациентов (табл. 1).
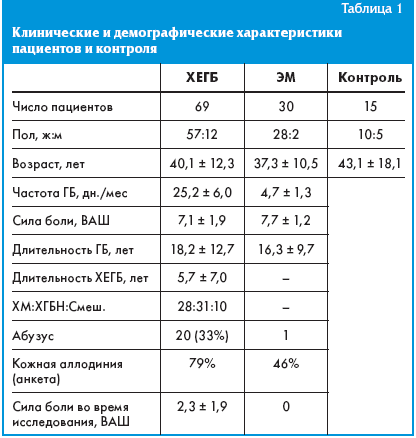
По данным анкеты аллодинии, в группе ХЕГБ распространенность ЦС во время интенсивной ГБ составила 79%.
2. Статическая аллодиния, феномен wind-up и порог R3 МР и НФР у пациентов с ХЕГБ
Чувствительность к боли от давления достоверно выше в группе ХЕГБ во всех точках, кроме висков, к боли от укола и wind-up во всех точках, кроме лба, по сравнению с группой контроля.
Для удобства расчетов использовался индекс альгометрии. Это сумма порогов боли от давления во всех точках. Так как нет данных о том, какой порог боли от давления указывает на аллодинию, мы использовали группу контроля для получения нормативных данных. Об аллодинии свидетельствует индекс, выше которого указали свои пороги 95% участников группы контроля (в нашем исследовании пороговый индекс альгометрии составил 41,9 фунта). Таким образом, распространенность ЦС во время наименьшей боли в группе ХЕГБ составила 70%. Группа ХЕГБ достоверно отличалась от контроля по индексу альгометрии.
Более того, отсутствие различий в болевых порогах справа и слева, независимо от преимущественной стороны боли при ее усилениях, говорит о стабильности ЦС, так как в приступе мигрени аллодиния всегда развивается на стороне боли и переходит на противоположную сторону, шею и плечи только при длительных приступах.
Для определения нормативных данных порога R3 МР это исследование было проведено на 15 участниках группы контроля. По нашим данным, порог R3-компонента составил 9,6 ± 1,5 мА. В группе ХЕГБ выявлено достоверное снижение порога R3 мигательного рефлекса (7,6 ± 2,16 мА). Нормативный порог НФР составил 10,3 ± 1,7 мА, порог боли 9,8 ± 1,8 мА. В группе ХЕГБ выявлено достоверное снижение порога НФР (9,0 ± 2,2 мА) и порога боли (6,2 ± 1 мА).
3. Статическая аллодиния, феномен wind-up в группе сравнения с ЭМ
Для изучения закономерностей развития ЦС и ее влияния на хронизацию ГБ была исследована группа пациентов с ЭМ с частотой ГБ более 2 дн./мес и менее 15 дн./мес. Возраст пациентов, длительность заболевания и сила боли не отличались в группах ЭМ и ХЕГБ. Средняя частота приступов составила 5,2 дн./мес.
У пациентов группы ЭМ выявлены достоверно более высокие пороги боли от давления и укола во всех точках по сравнению с группой ХЕГБ. Пороги боли при ЭМ достоверно не отличались от показателей контрольной группы испытуемых, что свидетельствует об отсутствии СА при эпизодической мигрени в межприступном периоде. Средний индекс wind-up, напротив, достоверно не различался при ЭМ и ХЕГБ.
Таким образом, группа ЭМ отличается от контроля только по индексу wind-up и от ХЕГБ по остальным показателям сенситизации.
Пациентов с ЭМ можно разделить на 2 подгруппы по индексу wind-up: с высоким и низким индексом. Точка раздела была определена аналогично точке раздела для альгометрии и составила 14,1. В подгруппе с более высоким wind-up выявлена более высокая частота приступов (7,5 дн./мес vs. 3,5 дн./мес) и меньшая длительность заболевания (12,1 года vs. 19,1 года). В подгруппе пациентов, указывающих на признаки кожной аллодинии в анамнезе, выявлена большая частота приступов.
4. Терапия венлафаксином
В качестве профилактического лечения головной боли 18 пациентам из вышеописанной группы пациентов с ХЕГБ был назначен прием венлафаксина (Велафакс®) курсом продолжительностью 1,5 месяца. Схема дозирования: 37,5 мг (18,9 мг × 2 раза в сутки) в течение 7 дней с последующим повышением до 75 мг (37,5 мг × 2 раза в сутки).
5 пациентов (28%) закончили исследование преждевременно: 3 пациента (17%) из-за побочных эффектов, развившихся на стадии титрования препарата и помешавших поднять дозу до минимальной терапевтической; 2 пациента (11%) — из-за отсутствия эффекта от лечения. 13 пациентов прошли полный курс лечения и были включены в анализ. Им также было проведено повторное обследование (аналогичное описанному выше) после окончания 6-недельного курса лечения.
По результатам лечения было достигнуто достоверное снижение средней силы боли (с 6,6 до 4 баллов) и ее частоты (с 26 до 12 дн./мес). У 10 пациентов (77%) частота боли снизилась достоверно, а 54% пациентов отметили как минимум 50%-ное урежение ГБ. У 70% пациентов было достигнуто урежение ГБ более чем на 10 дн./мес (табл. 2).
Заметное снижение частоты и интенсивности ГБ позволило пациентам сократить количество принимаемых анальгетиков (с 21,8 до 5,1 таблетки в месяц), что значительно снижает риск развития абузусной ГБ.
Кроме того, в ходе лечения было достигнуто достоверное повышение индекса альгометрии до нормальных значений и уменьшение выраженности и распространенности аллодинии. У 54% пациентов клинические признаки аллодинии исчезли полностью.
По данным нейрофизиологических исследований, порог R3 МР достоверно повысился и достиг нормального диапазона значений (с 7,3 до 9,2 мА). Пороги боли и рефлекса НФР, а также соотношение порог боли/порог рефлекса также имели тенденцию к повышению, но не достигли нормальных значений.
78% пациентов указали на наличие побочных эффектов в ходе лечения. Наиболее частыми среди них были: тошнота, урежение стула, нарушение концентрации внимания, снижение аппетита. У большинства пациентов эти эффекты были легкими и быстро проходящими. Они развивались в большинстве случаев в течение первой недели приема (на субтерапевтической дозе в 37,5 мг) и исчезали в среднем через 5–7 дней, что не препятствовало повышению дозы до терапевтической.
Обсуждение
В группе пациентов с ХЕГБ выявлена сенситизация центральных ноцицетивных структур — статическая аллодиния, которая сохраняется даже в период наименьшей боли или ее отсутствия. В то же время при ЭМ у большинства пациентов в межприступном периоде аллодиния отсутствует. Однако в группе ЭМ выявляются также пациенты с повышенным индексом wind-up, т. е. те, у кого признаки сенситизации проявляются даже в межприступном периоде. У таких пациентов отмечена более высокая частота приступов и меньшая длительность заболевания. Можно сделать вывод о том, что со временем элементы ЦС не полностью исчезают после окончания мигренозного приступа и пациент становится более восприимчивым к следующему приступу, т. е. встает на путь хронизации ГБ. После того как боль приобретает ежедневный или почти ежедневный характер, она существует самостоятельно, независимо от наличия или отсутствия провоцирующих факторов, и поддерживается в результате центральной сенситизации ноцицептивных структур.
Более низкая длительность ЭМ в подгруппе с высоким wind-up говорит о том, что сам фактор длительности заболевания не приводит к хронизации ГБ. Из клинического опыта известно, что некоторые пациенты могут в течение многих лет страдать ЭМ с неизменной частотой приступов. У другой части пациентов частота приступов начинает неуклонно нарастать вскоре после дебюта заболевания. Таким образом, измерение феномена wind-up позволяет выделить пациентов, у которых началась динамика ЭМ в направлении хронизации и трансформации ГБ.
По нашим данным, пациентов с ГБ можно разделить на несколько стадий вне зависимости от диагноза по критериям ICHD-2 (рисунок):
- эпизодическая ГБ с признаками аллодинии только во время приступа;
- эпизодическая ГБ, при которой повышение wind-up сохраняется между приступами;
- ХЕГБ со стабильными признаками ЦС во время усилений боли, фоновой ГБ и безболевом периоде.
Выявление ЦС с помощью простого метода wind-up у пациентов с эпизодической ГБ в межприступном периоде позволяет выделить группу риска, уже вступившую на путь хронизации ГБ, и является показанием к началу профилактического лечения.
В ходе исследования было показано, что венлафаксин является эффективным и безопасным средством для урежения ГБ. Профилактическое лечение Велафаксом приводит к выраженному клиническому облегчению состояния пациентов, сокращению приема анальгетиков. Позитивный эффект препарата подтверждается уменьшением выраженности аллодинии, а также нормализацией порога болевого R3-компонента мигательного рефлекса, который отражает функциональное состояние стволовых структур и спинномозгового ядра тройничного нерва, участвующих в поддержании ЦС.
По вопросам литературы обращайтесь в редакцию.
Н. В. Латышева
Е. Г. Филатова, доктор медицинских наук, профессор
ММА им. И. М. Сеченова, Москва
Купить номер с этой статьей в pdf