В последнее десятилетие синтезировано много новых оригинальных антиэпилептических препаратов (АЭП), которые входят в повседневную клиническую практику как детских, так и взрослых эпилептологов. Основная цель современной фармакологии в лечении эпилепсии — создание «идеального» препарата, подавляющего не только припадки, но и обладающего истинным антиэпилептогенным действием с максимальным соотношением эффективность/переносимость. Увеличение числа АЭП существенно расширяет возможности в лечении эпилепсии, особенно при фармакорезистентных формах, и в то же время ставит врача в трудное положение выбора адекватного препарата. Положение усугубляется с появлением каждого нового препарата, поскольку у больных с фармакорезистентной эпилепсией может наблюдаться преходящее улучшение после приема каждого из вновь назначенных АЭП, и это создает иллюзию их эффективности. В то же время только накопление опыта применения этих препаратов дает возможность расширять группу АЭП. Новые препараты показали лучшую переносимость, более низкий потенциал взаимодействия с другими АЭП; кроме того, они проще в применении. Одним из таких препаратов является топирамат (Топамакс).
Топамакс относится к классу сульфаматзамещенных моносахаридов. Действие препарата осуществляется благодаря нескольким механизмам: блокада вольтажзависимых кальциевых и натриевых каналов (препятствующая активации ГАМКергической трансмиссии), подавление медиаторов возбуждения (глутамат), угнетение карбоангидразы. Таким образом, происходит коррекция нарушенного баланса тормозной ГАМКергической и возбуждающей глутаматергической систем. Благодаря такому действию расширяется спектр применения препарата при различных формах эпилепсии как в виде моно-, так и в составе комплексной терапии.
Топамакс характеризуется линейной фармакокинетикой, быстрой абсорбцией; в дозе до 200 мг/сут не метаболизируется в печени. Поскольку период полувыведения составляет примерно 21 ч, оптимальный прием препарата 1–2 раза в сутки, независимо от приема пищи. У Топамакса отсутствует влияние на концентрацию других АЭП, которые, в свою очередь, не действуют на его терапевтическую активность. К недостаткам Топамакса можно отнести медленную титрацию. «Терапевтическое окно» препарата очень широко — от 2 до 10 мг/кг/с. У детей показатели клиренса топирамата повышены, а период полувыведения более короткий. Следовательно, при одной и той же дозе в расчете на 1 кг массы тела концентрации Топамакса в плазме у детей могут быть ниже. В связи с этим необходим подбор более высоких доз по сравнению с взрослыми — до 15 мг/кг/с. Следует подчеркнуть, что Топамакс отнесен к третьей группе АЭП по потенциальному тератогенному влиянию, т. е. обладает минимальной тератогенностью (L. E. Leppic, 2001).
В публикациях отечественных авторов отмечены перспективность применения препарата в терапии детей и взрослых. Зарубежные врачи имеют большой опыт применения Топамакса в виде моно- и add-терапии с достаточным объемом наблюдения пациентов детского и взрослого возраста. Также за рубежом были проведены двойные слепые исследования по сравнению эффективности применения Топамакса, карбамазепина и вальпроатов (Privitera M. et al., 2003; и др.).
Цель данного исследования заключалась в оценке эффективности и безопасности применения Топамакса у детей и взрослых в качестве стартовой терапии, моно- и политерапии.
Открытое рандомизированное исследование включало 199 больных (100 мужчин и 99 женщин) в возрасте от 2 до 50 лет, получавших Топамакс в течение 6–36 мес (табл. 1). Все пациенты подвергнуты динамическому клиническому наблюдению, ЭЭГ, МРТ (в нескольких случаях КТ), при необходимости проводилась полиграфическая регистрация сна.
Таблица 1. Распределение пациентов по возрасту |
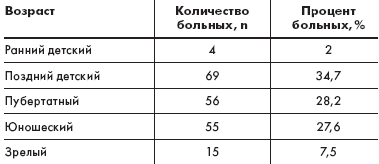
У большинства больных заболевание дебютировало в детском возрасте — 66,7 % (табл. 2).
При анализе факторов риска получены следующие данные. Наследственная отягощенность отмечена у 15 больных, перинатальная патология — у 79, черепно-мозговая травма — у 19 пациентов, нейроинфекции — у 12, церебральные дисплазии — у 22, кисты — у 7, опухоли головного мозга — у 4, мезиальный темпоральный склероз — у 4, сосудистые заболевания — у 3, туберозный склероз — у 1, другие (болезнь Штурге–Вебера, Рандю–Ослера и др.) — у 6; факторы риска не были установлены у 27 пациентов. Приведенные данные показывают, что перинатальная патология является одним из основных факторов риска возникновения эпилепсии.
Таблица 2. Распределение пациентов по дебюту заболеваний |
По формам заболевания больные распределялись следующим образом: симптоматическая/криптогенная эпилепсия — 159 пациентов, идиопатическая: роландическая эпилепсия — 3, эпилепсия с генерализованными судорожными припадками — 2, детская абсансная эпилепсия — 4, юношеская абсансная эпилепсия — 4, ювенильная миоклоническая эпилепсия — 7 больных. Не удалось классифицировать форму заболевания у 20 человек.
Психические нарушения пароксизмального характера наблюдались в анализируемой группе до приема Топамакса у 9 больных, задержка психоречевого развития диагностирована у 10 детей, дисфории отмечены в 18 случаях, депрессия — у 16, когнитивные нарушения имели 23 пациента, нарушение интеллекта различной степени выраженности отмечено в 15 случаях.
У женщин, включенных в данное исследование, выявлены следующие особенности: связь с приходом менструации в дебюте заболевания — у 18 пациенток, катамениальная эпилепсия диагностирована у 6. Беременность состоялась у 2, роды — в одном случае (ребенок здоров). Гормональные нарушения в виде дисменореи и/или поликистоза яичников диагностированы у 17 женщин, из них у 9 до приема АЭП и у 8 после начала лечения (7 пациенток получали одновременно вальпроаты).
Доза Топамакса колебалась от 2 до 15 мг на 1 кг массы в сутки. Монотерапия проводилась 48 больным; в 151 случае препарат использовался как дополнительный.
У 40 больных (20,1 %) препарат был отменен в связи с неэффективностью или отрицательными эффектами: аггравацией припадков в виде их учащения и/или утяжеления, появления приступов другого типа, присоединения к приступам сна приступов бодрствования (всего 14 случаев — 7 %). В 12 случаях (6 %) прием препарата прекращен из-за выраженных побочных эффектов в виде возбудимости, заторможенности, нарушения речи в связи с образованием камней в почках, развитием цистита с гематурией, потерей массы тела более 10 кг, а также неординарными нарушениями: тяжелой инсомнией, психоэмоциональными расстройствами (тоска), пигментацией кожи.
Топамакс продолжали получать 133 пациента; из них в качестве монотерапии — 54 (40,6 %) и политерапии — 79 (59,4 %). В 65 случаях (48,9 %) достигнута ремиссия, в 22 (16,5 %) — припадки купированы на 50 % и более.
В ходе исследования выяснялись причины, послужившие основанием для продления приема Топамакса у 46 больных (34,6 %), у которых по общепринятым критериям значимого улучшения (прекращение или существенное урежение припадков) не наблюдалось. Было установлено позитивное влияние препарата на другие факторы, а именно: устранение вторичной генерализации приступов или переход сложных парциальных приступов в простые (17 больных), более легкий выход из припадка (10 человек), либо сочетание нескольких факторов (19 пациентов).
Побочные эффекты, носившие транзиторный характер, отмечались у 36 пациентов (27 %) в виде возбудимости (11 больных), заторможенности, замедления речи (6 больных), снижения массы тела на 3–10 кг (17 человек), парастезий (2 пациента). Они прекращались самостоятельно или при коррекции дозы Топамакса.
Топамакс является АЭП с разными механизмами действия: подобно карбамазепинам он влияет на натриевые каналы, подобно вальпроатам — на кальциевые каналы, как бензодиазепины и вальпроаты, оказывает ГАМКергический эффект, подобно ацетазоламиду ингибирует угольную ангидразу; не исключается также его антиглутаматное действие. Благодаря этим механизмам препарат оказывает противоэпилептическое действие широкого спектра. Неслучайно наибольшее внимание на последнем европейском (Вена, 2004) и международном (Париж, 2005) конгрессах по проблемам лечения эпилепсии основное внимание было уделено Топамаксу наряду с окскарбазепином и леветирацетамом. Значительный опыт применения Топамакса имеется уже и в России. По нашим данным, лечение Топамаксом проводится не менее чем у 600 пациентов. Большое количество исследований касается детской эпилепсии. В нашем наблюдении 25 % пациентов были в допубертатном возрасте, а начало развития заболевания в этом возрасте отмечено у 75 % больных. И хотя мы не располагаем опытом применения Топамакса у детей младшей возрастной группы, в литературе есть сообщения об успешном применении Топамакса с четырехмесячного возраста (A. Grinspan et al., 2005).
Эффект от применения Топамакса, определяемый в литературе количеством респондентов, отвечающих на терапию прекращением или урежением припадков более чем на 50 %, оценивается по-разному. Например, по исследованию M. Bujand и соавторов (2004), полное прекращение припадков отмечено в 39 %, а по данным J. Kruja и соавторов (2004) — всего лишь у 4,3 %, Y. H. Yi и соавторов (2005) — у 22,2 %. В то же время количество больных, у которых число припадков сократилось более чем на 50 %, составило 56–58 %. В целом столь высокий процент позитивных результатов не соответствует современным данным, согласно которым несмотря на введение новых АЭП, количество фармакорезистентных больных составляет не менее 1/4 — 1/3 наблюдений (W. Loscher, D. Schmidt, 2002; D. Schmidt, W. Loscher, 2004). Такое расхождение требует специального анализа и скорее всего для объективной оценки необходимо длительное проспективное наблюдение. Что касается разброса приведенных данных, то результат может зависеть от того, применялся ли Топамакс при резистентных формах как первый препарат или как дополнительный. Однако и в последнем случае результат (полное прекращение припадков) колеблется от 4,3 % (J. Kruja et al., 2004) до 39 % (M. Bujand et al., 2004). Значение могут иметь только длительные проспективные наблюдения, так как эффективность препарата с течением времени часто снижается. Но сведения о длительности проспективного наблюдения приводятся не всегда. Возможно влияние других факторов или их сочетаний. Так, по некоторым данным, Топамакс, примененный в качестве первого препарата у пожилых, вызывал прекращение припадков у 77,3 % пациентов, улучшение не зарегистрировано лишь в 9,1 % случаев (Y. Chinvarun et al., 2005).
Результаты наших наблюдений подтверждают эффективность Топамакса в терапии эпилепсии. По крайней мере это очевидно для симптоматической/криптогенной эпилепсии, поскольку именно данная группа пациентов была достаточно репрезентативной — 159 человек. Обращает на себя внимание тот факт, что действенность Топамакса была высокой как при моно-, так и при политерапии (соответственно 40,6 % и 59,4 %), тем более что Топамакс не во всех случаях был препаратом первого выбора. Так, у 12 пациентов он заменял назначенные ранее вальпроаты в связи с планируемой беременностью или наличием таких побочных явлений, как дисменорея и поликистоз яичников. При этом у 4 пациенток, у которых припадки не были полностью купированы с помощью вальпроатов, лечение стало успешным после перевода их на Топамакс. S. Rielke и A. Schreinea (2005), располагающие опытом перевода терапии с вальпроатов на Топамакс 65 пациентов в возрасте 12 лет и старше, отметили положительные результаты у 73 % пациентов, в том числе у 48 % прекращение припадков.
В последнеее время в связи с возросшим вниманием к терапии эпилепсии у женщин значимость проблемы замены вальпроатов на современные АЭП, видимо, будет возрастать. Одна из сложных методологических проблем — оценка эффективности лекарств, в частности АЭП. Нами проанализированы данные о пациентах, которые не отказались от Топамакса, хотя частота приступов у них не изменилась. Впервые в качестве критерия эффективности рассматривался не показатель снижения частоты припадков, а возможность упрощения и облегчения выхода из приступа. Таким образом, Топамакс был эффективен в 43,7 % случаев в соответствии с общепринятыми методами и в 66,8 % — с учетом данного фактора.
Эффективность АЭП, в частности Топамакса, по результатам данного исследования составила 66,8 %, у 40,6 % — в качестве монотерапии и у 59,4 % — аддитивной. Топамакс может не только снижать частоту приступов, но и способствовать облегчению их течения и выхода из припадка. У детей доза на 1 кг массы тела требуется большая, чем у взрослых. Препарат обладает высоким показателем эффективность/переносимость как у детей, так и у взрослых.
Литература
- Калинин В. В. Новый антиэпилептический препарат топамакс // РМЖ. Психиатрия. 2002. № 10. С. 25–33.
- Карлов В. А, Власов П. Н., Фрейдкова Н. В. Опыт применения топирамата в комплексной терапии фармакорезистентной эпилепсии // Журнал неврологии и психиатрии им. С. С. Корсакова. 2003. Вып. 7. С. 21–26.
- Мухин К. Ю, Глухова Л. Ю., Петрухин и др. Топамакс при монотерапии эпилепсии // Журнал неврологии и психиатрии им. С. С. Корсакова. 2004. Вып. 8. С. 35–40.
- Albsoul-Younes F., Salem H., Ajlouni S., Al-Safi S. Topiramate slow dose titration: improve efficacy and tolerability. Pediatr Neurol. 2004; 31: 349–52.
- Amerio R., Tonon A., Bonettelo P., Garafalo P. et al. Triveneto study group on epilepsies. Efficacy and tolerability of topiramate in 363 drug-resistant epilepsy patients. Epilepsia 2002; 43 (8): 347.
- Bujand M., Lopex Roa M., Tresierra F. et al. Topiramate as first ad-on option in refractory epilepsy. Epilepsia 2004; 45 (3): 148.
- Carpay J. A., Guerrini R., Lahayl M. Y., Van Ouen J. C. Response of localization-relative or generalized epilepsy in monotherapy in non clinical setting. Epilepsia. 2004; 45 (3): 149.
- Chinvarun Y. Long-term, open-label study of topiramate as monotherapy in the treatment of adult patients with recently diagnosed partial onsed seizures. Epilepsia. 2005; 46 (8): 339.
- Grinspan A., Micaeloff Y., Rey E. et al. Topiramate (TPM): efficacy, tolerability and pharmacokinetics in children with epilepsy aged from 6 months to 4 years. Epilepsia. 2005; 46 (6): 238.
- Kruja J., Qukaj A., Davidhi A. et al. TPM in drug resistant epilepsy. Epilepsia. 2004; 45(3): 148.
- Leppik L. E. Issues in the treatment of epilepsy. Epilepsia 2001; 42 (4): 1–6.
- Loscher W., Schmidt D. New horizon in the development of antiepileptic drugs: search for new targets conference review. Epilepsy Res. 2002; 50: 3–16.
- Marquez-Sanchez J., Marquez-Daniel F. Topiramate in refractory epilepsy: seizure control and assessment of side effects in 108 patients. Epilepsia. 2002; 43 (8): 349.
- Ormrod D., McClellan K. Topiramate: a review of its use in childhood epilepsy. Paediatr Drugs. 2001; 3: 293–319.
- Privitera M., Brodie M., Mattson R. et al. EPMN Study Group. Topiramate, carbamazepine and valproate monotherapy: double-blind comparison in newly diagnosed epilepsy. Acta Neurol Scand. 2003; 107: 165–75.
- Rielke S., Schreiner A. Efficacy and tolerability of topiramate in epilepsy after transition from valproat. Epilepsia. 2005; 46 (8): 183–184.
- Schmidt D., Loscher W. Drug resistance in epilepsy. Epilepsy Res. 2005; 46: 858–870.
- Yi Y. H., Yang S. Q., Liao W. P. et al. An open-label self — controlled study of topiramate as ad-on therapy with lower dose for treatment of refractory epilepsy. Epilepsia. 2005; 46 (3): 275–276.
В. А. Карлов, доктор медицинских наук, профессор, член-корреспондент РАМН
Н. В. Фрейдкова
МГМСУ, Детская городская Морозовская клиническая больница, Москва