Противосудорожные препараты традиционно применяются для лечения эпилепсии. При этом предполагается длительная терапия, которую можно рассматривать как компромисс между клинической эффективностью, токсичностью и стоимостью лечения. Современные антиэпилептические препараты (АЭП) позволяют добиться ремиссии в 65% случаев, снизить частоту приступов — в 85% [1, 4, 20, 25].
Новыми АЭП, эффективно купирующими судорожные состояния различного генеза, являются леветирацетам (кеппра) и топирамат (топамакс), которые пока еще недостаточно широко используются в неврологической практике, хотя отличаются от АЭП первой генерации лучшей переносимостью и безопасностью при длительном применении [1, 2, 3, 4, 5, 6, 7, 14, 15].
Кеппра — структурный аналог пирацетама [20], который по своим свойствам приближается к оптимальной фармакокинетике для АЭП. Его отличают высокая биодоступность при пероральном назначении (90%), причем пиковая концентрация достигается уже через 1–3 ч. Отсутствует известное влияние на другие препараты, в том числе на АЭП при комбинированном лечении. Период полувыведения препарата — около 8 ч (в центральной нервной системе — дольше), что делает возможным его двукратный прием. Дозы кеппры могут варьировать от 500 до 5000 мг/сут (30–40 мг/кг/сут) [7, 23, 24, 25].
Топамакс — сульфатзамещенный моносахарид. Он блокирует вольтажзависимые натриевые и кальциевые каналы, быстро всасывается при приеме внутрь, пик концентрации в плазме крови достигается через 1–4 ч. Дозы топамакса варьируют от 50 до 550 мг/сут (3–10 мг/кг/сут). Средний период полувыведения — 21 ч [18, 22].
Целью исследования стало изучение эффективности данных АЭП в сравнительном аспекте при лечении разных вариантов эпилепсии, в том числе в качестве экстренной помощи, при утратившей эффективность предшествующей противоэпилептической терапии с последующим использованием этих препаратов.
Мы наблюдали 37 пациентов (21 мужчина и 16 женщин) в возрасте от 1 года до 35 лет, страдающих эпилепсией. Симптоматическая височно-лобно-долевая (ЭСВЛД) эпилепсия была диагностирована у 22 больных, симптоматическая височно-долевая (ЭСВД) — у 15. Из 37 больных 14 (37,8%) ранее были оперированы по поводу эпилепсии, но эффект оказался сомнительным [8, 10]. Все пациенты обратились к врачу в связи с резким учащением припадков, которые стали носить серийное, в некоторых случаях статусное течение. До этого больные длительное время применяли различные АЭП (карбамазепин, клоназепам, радедорм, реланиум, ламиктал, вальпроаты). Учитывая отсутствие эффекта от перечисленных АЭП, решено было использовать кеппру и топамакс.
Все больные были разделены на две группы в зависимости от использовавшегося АЭП.
Курс лечения кеппрой прошли 20 больных в возрасте от 1 года до 35 лет (1-я группа наблюдений). Дозы кеппры варьировали от 500 до 2500 мг (30–50 мг/кг/сут) при однократном приеме препарата. Затем пациенты начинали принимать препарат 2 раза в сутки под контролем клинической и электроэнцефалографической (ЭЭГ) картины.
Топамакс применяли у 17 пациентов в возрасте от 1 года до 35 лет (2-я группа наблюдений). Топамакс назначали в два приема в зависимости от возраста и веса, начиная с 25 до 50 мг (от 3,0–12,5 мг/кг/сут); шаг титрования составлял 2 дня. Дозы подбирались в зависимости от динамики клинических данных и ЭЭГ.
Ежедневный клинический осмотр проводили в течение 21 дня, затем каждые 15 дней на протяжении последующих 3 мес и 1 раз в 3 мес в течение последующего года. Общий срок наблюдения составил 16 мес.
Проводилось нейропсихологическое тестирование. Общесоматическое обследование включало клинические и биохимические анализы крови. Перед началом лечения новыми АЭП всем больным для исключения грубых органических поражений головного мозга были проведены магнитно-резонансная томография и компьютерная томография на аппарате PHILIPS Gyroscan NT5 (0,5 Т) и спиральном компьютерном томографе фирмы Филипс AVE 1.
ЭЭГ записывали на мультифункциональном комплексе (Nicolet, базовая программа Bravo, мониторинговая — Endeawor). Ежедневная запись проводилась в течение 10 дней, затем через каждые 3 дня еще 11 дней, затем через каждые 15 дней на протяжении последующих 3 мес и, наконец, 1 раз в 3 мес в течение года.
Использовали гамма-камеру АДАС Solus — EPIC (Филипс), работающую в режиме однофотонного эмиссионного компьютерного томографа (ОФЭКТ). В сочетании с другими адекватными тестами и имеющимися у пациента клиническими симптомами данное исследование позволяет собрать необходимую диагностическую и прогностическую информацию [9, 13]. По результатам ОФЭКТ определяли, как влияют кеппра и топамакс на степень изменения перфузии мозговой ткани.
Кеппру назначали в режиме политерапии. До начала лечения кеппрой пациенты применяли следующие препараты и их сочетания: депакин, топамакс — 6,6%; депакин, финлепсин — 16,6%; финлепсин, ламиктал — 6,6%; депакин хроно — 52%; финлепсин — 13,3%. Принимая во внимание значительное ухудшение состояния всех больных (серии приступов, эпилептические статусы), при том что различные комбинации используемых АЭП и увеличение их доз не оказывали сколько-нибудь положительного эффекта, мы начинали лечение кеппрой с «ударной дозы». Первая доза составляла 500–1500 мг, на вторые сутки ее увеличивали до 1500–2000 мг в два приема. Эта тактика отличалась от рекомендуемой другими авторами [7, 14, 23, 24] и была основана на таких фармакологических данных, как быстрое накопление (достижение пиковой концентрации в сыворотке крови в течение 1–3 ч), длительный период полувыведения, отсутствие метаболической активности и влияния на другие АЭП.
Клинический эффект в виде урежения припадков на 43% (р < 0,001) отмечался в течение первых 12 ч у всех пациентов.
На 3-и сутки начинали уменьшать дозу применяемых ранее АЭП по 1/4 таблетки каждые 3 дня.
На 5-е сутки у 17 из 20 пациентов отмечалось небольшое недостоверное учащение приступов, но их количество не достигало исходного уровня (р > 0,05).
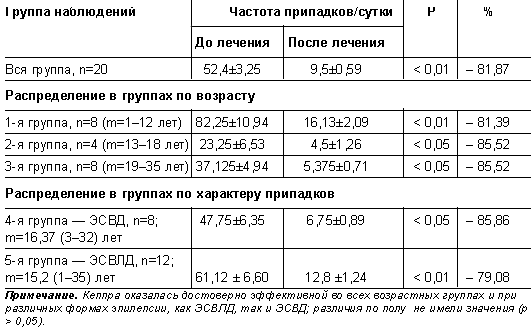
В течение первых 2 сут у больных происходило изменение качества припадков, упрощалась структура приступа: не было генерализованных припадков, уменьшалось время приступа. Значительное урежение припадков происходило в период с 7-х по 10-е сутки и составило в среднем 81,87% (р < 0,01). В таблице 1 представлены данные об изменениях характера припадков у больных, использовавших кеппру.
Для решения вопроса об эффективности препаратов вальпроевой кислоты применяли пробу с внутривенным введением депакина для инъекций [11, 12].
В тех случаях, когда определяли неэффективность депакина, последний отменяли по 1/2 таблетки от исходной дозы каждые 2 дня.
Как уже указывалось, лечение начинали в режиме политерапии в сочетании с препаратами, которые пациенты получали в момент обращения, с постепенным уменьшением доз исходных лекарственных средств. У 17% отмечались сонливость, головокружение, диспепсия. У 6 (75%) из 8 детей на 3–5-е сутки появлялась нервозность, возбуждение, которые регрессировали в течение последующих 3 дней.
При стабилизации состояния пациенты принимали подобранные препараты, «показатель удержания» после 8 мес лечения кеппрой составил 80%. В тех случаях, когда больные по финансовым проблемам не могли получать кеппру длительно, ее постепенно отменяли в течение 7 дней по 1/4 таблетки в сутки. Пациенты снова переходили на использовавшуюся исходно терапию. Состояние было стабильным, но при ухудшении его сами больные использовали кеппру в экстренных ситуациях по 1000–1500 мг одноразово в течение 2–3 дней.
В течение 16 мес подобранную терапию не меняли. Состояние оставалось стабильным. Эпилептические статусы и серии приступов не отмечены. В режиме экстренно кеппру используют 47% из пролеченных больных.
На основании данных ЭЭГ у 15 (71,4%) пациентов регистрировалось снижение индекса эпилептичности (ИЭ) в среднем на 8,57% (р > 0,05). Отмечены быстрое падение ИЭ в первую неделю терапии, обычно — на 3–4-й день, реже — на 1-2-й день от начала применения препарата, затем его стабильный уровень и некоторый подъем на 2–3-й неделе лечения. При достижении клинического эффекта достигался стабильный уровень ИЭ.
У 6 (28,6%) пациентов, получавших кеппру, диагностически значимых изменений ЭЭГ не выявлено.
При анализе данных ОФЭКТ по зонам головного мозга в момент обострения определялось неравномерное повышенное накопление маркера перфузии в левой височной доле: на поперечных и фронтальных срезах выявлялись области с повышенным включением маркера мозгового кровотока в правой верхней лобной извилине (значение асимметрии накопления — 16%), в правой теменно-височной области (асимметрия — 30–35%); при секторальном анализе — с относительным снижением в области нижней лобной извилины (асимметрия — 11–21%).
Через 10 дней после начала лечения было отмечено, что контуры левого и правого полушария стали относительно симметричны. Распределение маркера перфузии неравномерное. По поперечным и фронтальным срезам максимальные значения асимметрии выявлены в затылочных областях (асимметрия — до 33%, больше справа), теменных областях (асимметрия — 18–23%, больше справа), в височных областях (асимметрия — 14–27%, больше справа). В лобных долях перфузия нормализовалась, значения асимметрии не превышали физиологических.
Топамакс назначали в режиме политерапии. До назначения топамакса пациенты принимали следующие сочетания АЭП: депакин хроно, кеппра — 6,4%; депакин хроно, финлепсин — 6,4%; финлепсин, ламиктал — 9,6%; депакин хроно, ламиктал — 6,4%; финлепсин — 9,6%, депакин хроно — 61,2%. Для решения вопроса об эффективности препаратов вальпроевой кислоты также применяли пробу с внутривенным введением депакина для инъекций [11, 12]. Принимая во внимание значительное ухудшение состояния больных (серии приступов, эпилептические статусы), а также учитывая, что различные комбинации используемых АЭП и увеличение их доз не оказывали сколько-нибудь положительного эффекта, мы начинали лечение топамаксом с «ударной дозы» на фоне ранее проводившейся терапии в режиме экстренной помощи. Первая доза составляла 25–75 мг (при средней суточной дозе от 1,5 до 12,5 мг/кг/сут), на вторые сутки дозу увеличивали до 50-100 мг в два приема. Эта тактика отличается от рекомендуемой другими авторами [1, 2, 4, 21] и основывается на таких фармакологических данных, как быстрое накопление (достижение пиковой концентрации в сыворотке крови в течение 1–4 ч), средний период полувыведения (21 ч), отсутствие активных метаболитов и влияния на другие АЭП [17, 22].
Клинический эффект в виде урежения припадков на 37% (р < 0,001) отмечался в течение первых 24 ч у всех пациентов. На 3-и сутки начинали уменьшать дозы применяемых ранее АЭП по 1/4 каждые 3 дня.
На 5-е сутки у 4 из 17 пациентов отмечалось небольшое недостоверное учащение приступов, но их количество не достигало исходного уровня (р > 0,05).
В течение первых 2 сут у больных происходило изменение качества припадков, упрощалась структура приступа: не отмечались генерализованные припадки, уменьшалось время приступа. Значительное урежение припадков происходило в период с 7-х по 10-е сутки и составило в среднем 73,92% (р < 0,01). В таблице 2 представлены данные об изменении частоты припадков у больных, использовавших топамакс.
Положительный эффект при назначении топамакса отмечен в 73,92% случаев. Различия по частоте припадков до и после лечения оказались достоверными (табл. 2) как в группах по возрасту, так и в группах, распределенных по характеру припадков и формам эпилепсии. В течение первых суток редуцировалась структура пароксизмального приступа: исчезла аура, уменьшились головные боли.
В отличие от кеппры при приеме топамакса отсутствовали проявления вегетативного и психологического дискомфорта. Генерализованные припадки урежались к 3-м суткам.
На 3-и сутки начинали уменьшать применяемые ранее АЭП по 1/4 дозы в сутки, каждые 3 дня. На 5-е сутки у 10 из 17 пациентов отмечалось небольшое недостоверное учащение приступов, но их количество не достигало исходного уровня (р > 0,05).
У 10 (58,82%) из 17 пациентов, получавших топамакс, регистрировалось снижение ИЭ в среднем на 70–80%. У 4 (23,53%) диагностически значимых изменений ЭЭГ не выявлено. У 3 (17,64%) пациентов регистрировалось увеличение ИЭ в среднем на 18–22%.
Что касается побочных эффектов, со стороны центральной нервной системы и периферической нервной системы, особенно в период подбора в первые 2 сут, были отмечены атаксия, нарушение концентрации внимания, спутанность сознания, головокружение. У 5 (29,41%) больных возникало чувство тошноты (успешно купировавшееся церукалом). В связи с тем что топамакс преимущественно использовался в составе комбинированной терапии, установить точную причину развития побочных эффектов было сложно.
При анализе ежедневных записей ЭЭГ отмечено быстрое падение ИЭ в первую неделю лечения (обычно это снижение ИЭ начиналось на 3–4-й день, реже — на 1– 2-й день применения препарата), затем — стабильный уровень ИЭ и небольшой подъем ИЭ во 2–3-ю неделю применения препарата. При достижении терапевтической дозы достигался стабильный уровень ИЭ, как правило, значительно более низкий, чем до лечения, либо было отмечено, что ИЭ приближается к 0. Такая динамика имела место у 10 (58,82%) пациентов из 17. При отсутствии терапевтического эффекта стадийность изменений ИЭ сглажена или не наблюдалась, ежедневные колебания ИЭ носили хаотичный характер.
В течение 16 мес терапия не менялась. Состояние оставалось стабильным. Эпилептические статусы и серии приступов не отмечены.
При анализе данных ОФЭКТ по зонам головного мозга в момент обострения определялось повышенное накопление маркера перфузии в височных, теменных и затылочных областях, что указывает на наличие в этих областях эпилептической активности. Через 10 дней после начала лечения было отмечено, что контуры левого и правого полушария стали относительно симметричны. Распределение маркера перфузии более равномерное. Данные результаты подтверждают улучшение мозговой перфузии под влиянием топамакса.
Сравнение эффективности кеппры и топамакса выявило, что в отношении уменьшения частоты эпилептических припадков эффективность обоих препаратов оказалась практически одинаковой. Отмечена тенденция к уменьшению выраженности прежде всего пароксизмальной симптоматики уже в ранние сроки (до 7 сут). Редуцируется структура пароксизмального синдрома: исчезает аура, сокращаются длительность и сила тонических и клонических судорог. Упрощается структура сложных пароксизмов с психомоторными компонентами. Уменьшается продолжительность приступов, видоизменяется и постприступный период: отсутствуют головные боли, легче переносятся явления вегетативного и психологического дискомфорта (чаще при применении топамакса), сокращаются и ослабевают астенические и вегетативные проявления после больших судорожных припадков (чаще при применении кеппры). У ряда больных купируются постприступные дистимии и дисфории. Не наблюдалось повторения эпилептических статусов, характерных для генерализованных форм эпилепсии. Регрессировали имевшиеся психические девиации (дистимии, дисфории) и невротические расстройства (депрессия, ипохондрия, сверхценные идеи).
По данным ОФЭКТ выявили положительную динамику в виде более равномерного распределения маркера мозгового кровотока в тканях мозга.
Не было отмечено какого-либо выраженного искажающего влияния на ЭЭГ препаратов топамакс и кеппра. Эти препараты быстро «санируют» ЭЭГ. Топамакс имеет более пологую и плавную кривую снижения ИЭ, но снижает его сильнее, чем кеппра. Этот вывод требует проверки на большем количестве случаев.
Положительная динамика ЭЭГ — показателей наблюдается спустя несколько недель после применения препаратов. Резкое падение ИЭ в первые 7–10 дней после назначения говорит о начале действия препаратов.
По вопросам литературы обращайтесь в редакцию.
А. С. Шершевер, доктор медицинских наук
С. А. Лаврова, А. В. Телегин, А. В. Гриб
Свердловский областной онкологический диспансер, Межрегиональный нейрохирургический центр им. проф. Д. Г. Шефера, Екатеринбург
Приложения
-
- Динамика показателей как критерий оценки качества лечения эпилепсии противосудорожными препаратами - Таблица 1
Сравнительные результаты лечения кеппрой больных с разными формами эпилепсии
-
- Динамика показателей как критерий оценки качества лечения эпилепсии противосудорожными препаратами - Таблица 2
Сравнительные результаты лечения топамаксом больных с разными формами эпилепсии