Согласно данным Всемирной организации здравоохранения, современный мир меняется в сторону глобального демографического старения населения в большинстве развитых стран, с сохранением превалирования доли женщин в средних и старших возрастных группах. Так, по современным данным Федеральной службы государственной статистики, число женщин в возрасте от 45 до 59 лет в РФ в 2018 г. составило более 38% от общего числа женщин всех возрастов [1]. Такая значимая доля женщин работоспособного возраста, включающего период развития пре-, пери- и постменопаузы, объясняет большой интерес разных специалистов к изучению возрастных изменений, происходящих в организме женщины старше 45 лет.
Менопауза, с одной стороны, по сути являясь естественным событием перехода женщины из репродуктивного периода жизни в нерепродуктивный, с другой стороны, может стать критическим периодом испытаний, в течение которого возможно развитие различных неблагоприятных симптомов. Учитывая тот факт, что к моменту начала менопаузы могут проявиться симптомами уже накопленные соматические заболевания, наряду с теми нейровегетативными, психологическими и соматическими расстройствами, связанными собственно с изменением уровня половых гормонов, влияющих на активность многих систем организма, включая центральную нервную (ЦНС) и сердечно-сосудистую системы (ССС), можно предполагать значительное ухудшение качества жизни женщины в данный период. По данным литературы, климактерический синдром (КС) значимой степени выраженности развивается как минимум у 48% женщин [2]. Падение уровня половых стероидов в крови проявляется несколькими группами клинических симптомов, связанных в том числе с изменением функционирования нейротрансмиттерных систем в ЦНС:
1) вегетативно-сосудистые нарушения: приливы жара, потливость, повышение уровня артериального давления (АД) и/или его частые колебания, головная боль, головокружение, сердцебиение, зябкость, ознобы, чувство онемения, симпатоадреналовые кризы;
2) обменно-эндокринные нарушения: ожирение, изменение функции щитовидной железы, дисгормональная гиперплазия молочных желез, атрофия половых органов;
3) психоэмоциональные нарушения: характеризуются в основном повышенной утомляемостью, резкими сменами настроения, снижением работоспособности и ухудшением памяти [1, 2].
Помимо этого, к моменту наступления менопаузы большинство женщин уже имеют сопутствующие соматические заболевания, ухудшающие течение климактерического периода. Наиболее часто встречающиеся патологии — сахарный диабет (СД), ожирение, артериальная гипертензия (АГ), ишемическая болезнь сердца (ИБС), фибрилляция предсердий и хроническая ишемия головного мозга (ХИМ) [3]. ХИМ — особая разновидность сосудистой церебральной патологии, обусловленная медленно прогрессирующим диффузным нарушением кровоснабжения головного мозга с постепенно нарастающими разнообразными дефектами его функционирования [4, 5]. Установлено, что у женщин в период менопаузы распространенность сосудистых заболеваний головного мозга — ХИМ атеросклеротического, гипертензионного или смешанного характера составляет около 43%. Тяжелое течение самого КС дополнительно приводит к раннему формированию поздних и тяжелых форм цереброваскулярной патологии [4, 5].
Лечение климактерических симптомов при наличии цереброваскулярной патологии — медленно и незаметно прогрессирующей ХИМ на фоне АГ — является сложной проблемой в практике врача первичного звена [6]. Эффективным методом коррекции вегетативно-эмоциональных проявлений КС считается назначение заместительной гормональной терапии, которая абсолютно противопоказана при наличии у женщины сердечно-сосудистого заболевания (ССЗ) или ХИМ [5]. Помимо этого известно, что многие ноотропные препараты обладают выраженным стимулирующим действием и не могут применяться при ССЗ, а у анксиолитиков и антидепрессантов есть побочные эффекты, затрудняющие активное функционирование больных (дневная сонливость, заторможенность).
Таким образом, АГ остается актуальной проблемой женщин с КС, поскольку является самым частым компонентом коморбидности, присутствуя в 90% случаев всех возможных сочетаний заболеваний в терапевтической практике, и является фактором риска развития ССЗ, а также цереброваскулярных заболеваний (ЦВЗ): ХИМ, гипертонической энцефалопатии, ишемического или геморрагического инсульта [6, 7, 9]. Ключевым моментом применения антигипертензивной терапии остается эффективный контроль АД и достижение оптимальных значений, определяемых индивидуально для каждого пациента, с учетом всех имеющихся факторов риска и сопутствующих состояний [8].
Сегодня для лечения АГ рекомендованы пять основных классов антигипертензивных препаратов: ингибиторы ангиотензинпревращающего фермента, блокаторы рецепторов к ангиотензину II, антагонисты кальция, β-адреноблокаторы и диуретики, для которых способность предупреждать развитие неблагоприятных сосудистых событий доказана в многочисленных рандомизированных клинических исследованиях [8, 9]. Все эти классы препаратов подходят для стартовой и поддерживающей терапии, как в виде монотерапии, так и в составе комбинаций. Ранний старт с рациональной комбинированной терапии является новым подходом, рекомендованным современными руководствами по лечению АГ [8, 9]. Примером такого старта может быть препарат Гипотэф, отечественный четырехкомпонентный антигипертензивный препарат с нейропротективным эффектом. В состав одной таблетки Гипотэфа входят: эналаприл 5 мг, индапамид 0,75 мг, метопролола тартрат 25 мг и винпоцетин 2,5 мг. Применение такой низкодозовой комбинации компонентов с различными механизмами действия позволяет уменьшать побочные эффекты отдельных компонентов, которые, как правило, имеют дозозависимый характер [10]. Гипотэф плавно снижает АД без риска гипотонии, благодаря низким дозам активных компонентов снижается вероятность возникновения побочных эффектов, что способствует хорошей переносимости препарата и увеличивают приверженность к терапии, что особенно важно у пациентов с ЦВЗ [11]. Эффективность входящего в состав Гипотэфа сосудистого ноотропного компонента — винпоцетина была неоднократно подтверждена в широкомасштабных исследованиях, терапия винпоцетином способствует уменьшению выраженности таких неврологических симптомов, как головная боль, головокружение, шум в ушах у пациентов с АГ, а также достоверное улучшение настроения и памяти. Особенно эффективно применение препарата Гипотэф может быть у женщин трудоспособного возраста с АГ 1–2 степени на фоне КС, сопровождающейся учащенным сердцебиением, головокружением, так как Гипотэф мягко снижает АД без риска гипотонии и улучшает микроциркуляцию в головном мозге благодаря наличию в составе винпоцетина [11].
Целью настоящего открытого контролируемого исследования являлось изучение эффективности и безопасности применения препарата Гипотэф в терапии АГ 1–2 степени тяжести у женщин с КС.
Материал и методы исследования
В открытом контролируемом рандомизированном исследовании приняли участие 60 женщин в возрасте от 40 до 60 лет (Ме возраста — 54 года [51; 58]) с впервые выявленной АГ 1–2 степени и проявлениями КС в период пре-, пери- и постменопаузы.
Все пациентки, включенные в исследование, прошли первичное клинико-лабораторное обследование и были рандомизированы в 2 группы.
В 1-й группе (n = 30) пациенткам к базовой терапии (гиполипидемической, сахароснижающей и т. д.) был добавлен препарат Гипотэф (эналаприл 5 мг, индапамид 0,75 мг, метопролола тартрат 25 мг и винпоцетин 2,5 мг) в суточной дозе 1 таблетка на период 4 недели с последующей титрацией, при необходимости. Во 2-й группе (n = 30) к прежней терапии (гиполипидемическая, сахароснижающая и т. д.) был добавлен комбинированный препарат, содержащий эналаприл 10 мг и гидрохлортиазид 12,5 мг, также с последующей титрацией через 4 недели.
Продолжительность терапии в обеих группах составила 12 недель. Оценка состояния пациенток с использованием всех методик проводилась на этапе включения в исследование, далее — через 12 недель. В комплексную терапию также входили немедикаментозные методы, направленные на коррекцию имеющихся у пациенток метаболических нарушений (отказ от курения, диетические ограничения животных жиров, рафинированных углеводов и соли в пище, увеличение физической активности за счет аэробных нагрузок (пешеходные прогулки на свежем воздухе по 30–45 мин ежедневно)).
Критерии включения пациенток в исследование:
- женщины в возрасте 40–60 лет;
- впервые выявленная АГ 1–2 степени, подтвержденная СМАД;
- изменения менструального цикла в возрасте от 40 лет, не связанные с заболеваниями, что подтверждено заключением врача-гинеколога (менопауза или нерегулярные менструации в период пре-, пери- и постменопаузы), сопровождающиеся КС.
Критерии исключения из исследования:
- склонность к аллергическим реакциям, в т. ч. гиперчувствительность к компонентам препарата Гипотэф в анамнезе;
- получение гормонозаместительной терапии половыми стероидами или применение психотропных препаратов, таких как ноотропы, анксиолитики, антидепрессанты (в т. ч. растительного происхождения), антиконвульсанты, нейролептики (типичные и атипичные), адаптогены (в т. ч. растительного происхождения);
- планирование беременности или отсутствие надежной контрацепции;
- зависимость от психоактивных веществ;
- состояния, угрожающие жизни пациента.
Всем пациенткам был проведен опрос по специально разработанной карте, включающей блоки медико-социального анамнеза (вопросы о социальном статусе, наследственности, статусе курения, потреблении алкоголя, диете, течении сопутствующих соматических и гинекологических заболеваний, контрацептивный анамнез). Оценку КС проводили по шкале менопаузального индекса Куппермана в модификации Е. В. Уваровой (1982) (ММИ), в основу которого положено определение нейровегетативного, обменно-эндокринного и психоэмоционального симптомокомплексов. Клинико-лабораторное исследование включало: измерение роста, веса, окружности талии (ОТ), окружности бедер (ОБ); расчет индекса массы тела (ИМТ) и соотношения ОТ/ОБ; измерение систолического АД, диастолического АД, ЧСС в покое; электрокардиография в 12 отведениях в покое в положении лежа, лабораторные исследования: клинический анализ крови и мочи. Исследование когнитивного статуса проводили по стандартному скрининговому нейропсихологическому тесту Мини-Ког (Mini-Cog).
Исследование выполнено в соответствии с Хельсинкской декларацией, принятой в июне 1964 г. и пересмотренной в октябре 2000 г. (Эдинбург, Шотландия). От каждой пациентки было получено информированное согласие на участие в исследовании.
Статистическая обработка полученных результатов осуществлялась с применением пакета анализа Microsoft Excel, а также при помощи пакета программ Statistica 6.0. Распределения количественных данных, отличные от нормального, описывались с указанием медианы (Ме) и интерквартильного размаха в виде 25% и 75% процентилей. Достоверность различий оценивалась по методу вариационной статистики с использованием критериев Манна–Уитни, Крускала–Уолиса и Данна для независимых выборок и критерия Уилкоксона для парных случаев непараметрических распределений. Различия считались достоверными при значениях p < 0,05.
Результаты и обсуждение
Сравниваемые группы пациенток были сопоставимы по социодемографическим характеристикам, сопутствующей патологии и получаемой базовой терапии (табл. 1–3).
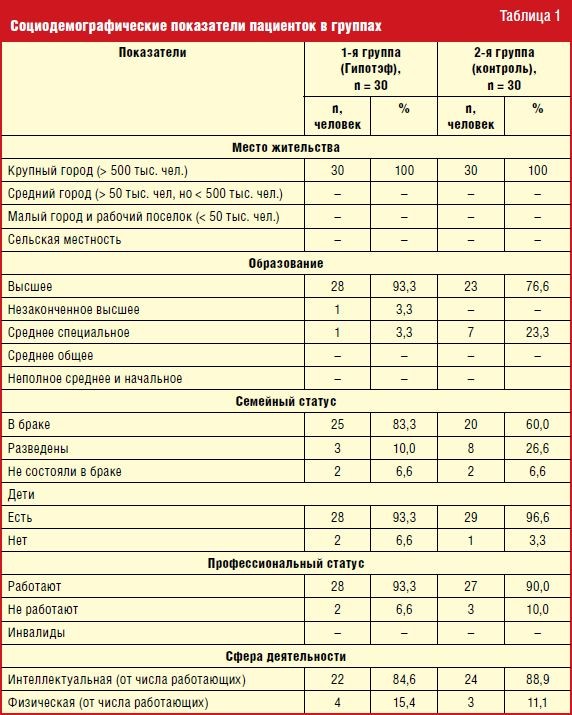
Следует отметить, что практически у всех женщин, включенных в исследование, ранее была выявлена дислипидимемия, также высокой оказалась распространенность нарушений углеводного и жирового обменов, что свидетельствует о рисках развития сердечно-сосудистой патологии у женщин в климактерическом периоде, значимо ухудшающей течение КС и влияющей на развитие когнитивных нарушений сосудистого генеза.
Динамика гемодинамических изменений
За весь период наблюдения (12 недель) в группах не было отмечено случаев смерти или развития неблагоприятных сосудистых событий, а также случаев непереносимости назначенных препаратов. Никто из наблюдаемых пациенток не отказался от участия в исследовании, и все 60 человек прошли финальное исследование через 12 недель.
За все время наблюдения в обеих группах было отмечено достоверное улучшение изучаемых гемодинамических показателей (табл. 4). Следует отметить, что в 1-й группе пациенток, получавших Гипотэф исходно по 1 таблетке в сутки, к 4-й неделе потребовалась титрация до 2 таблеток в сутки у 12 человек, что привело к достижению целевых значений АД к концу периода наблюдения. Во 2-й группе, исходно получившей комбинированный препарат, содержащий эналаприл 10 мг и гидрохлортиазид 12,5 мг, к 4-й неделе потребовалось увеличение дозы до 2 таблеток в сутки у большего количества пациенток — у 21, что также позволило достигнуть желаемого результата к концу наблюдательного периода. Однако достигнутая степень компенсации АГ в группе пациенток, получавших Гипотэф, оказалась достоверно более выраженной (табл. 4). Также были отмечены положительные изменения в показателях ЧСС, что в группе Гипотэфа отразилось в значимом уменьшении показателя ЧСС, в отличие от данных 2-й группы.
Динамика изменений менопаузального индекса
Проводился анализ нейровегетативных, обменно-эндокринных и психоэмоциональных нарушений путем оценки количества баллов в каждой группе симптомов, а также распределение степеней тяжести данных нарушений.
Показатели нейровегетативных, обменно-эндокринных и психоэмоциональных проявлений КС у женщин на этапе включения в исследование, ММИ представлены в табл. 5. Как видно из представленных в таблице данных, исходная тяжесть проявлений КС в обеих группах была сопоставима (р > 0,05). Следует отметить исходную более высокую степень тяжести КС по блокам нейровегетативных и сосудистых нарушений в обеих группах, видимо отражающих вклад АГ в патогенез данных нарушений на уровне ЦНС.
Все изменения в ММИ, произошедшие в группах за время наблюдения, отражены в табл. 5. Из полученных данных видно, что в обеих группах женщин произошло достоверное снижение степени тяжести проявлений КС (р < 0,02, р < 0,05). Необходимо также подчеркнуть, что в 1-й группе изменения носили ярко выраженный характер: через 12 недель ММИ составил Ме 30 (25; 32), в то время как во 2-й группе показатели изменились не столь эффектно и составили через 12 недель Ме 55 (53; 57). При сравнении результатов между группами с использованием критерия Манна–Уитни получено достоверное различие р < 0,02. Также из полученных результатов хорошо видно, что у большинства пациенток 1-й группы через 12 недель лечения отмечено снижение проявлений КС до легкой степени (общий ММИ снизился до 30 баллов). Основной вклад в изменение степени проявлений КС в 1-й группе внесло улучшение нейровегетативных и сосудистых нарушений, относящихся к жалобам на учащенное сердцебиение, головную боль, головокружение и повышение АГ.
Динамика когнитивных функций (память, внимание, работоспособность)
Тест Мини-Ког исходно был выполнен с ошибками у 30% пациенток 1-й и 2-й групп, что сопровождалось наличием жалоб у всех пациенток на снижение интеллектуальной работоспособности, сложность концентрации внимания, постоянную рассеянность и забывчивость наряду с неблагоприятным эмоциональным фоном (рис.). Через 12 недель после начала исследования в 1-й группе практически все пациентки отметили улучшение состояния как настроения, так и когнитивных функций: увеличилась умственная работоспособность, улучшилась память, уменьшились или практически исчезли эпизоды забывчивости и рассеянности, увеличилась концентрация внимания, что сопровождалось полным отсутствием ошибок при повторном проведении теста, в то время как во 2-й группе процент женщин, сделавших 1 ошибку в тесте, остался прежним. Очевидно, подобный результат может быть отчасти объяснен своевременным назначением терапии АГ и достижением целевых значений, но также и особенностью препарата Гипотэф, выбранного для данной терапии, обладающего нейропротективными свойствами, за счет включенного в состав винпоцетина.
Данные нашего исследования согласуются с результатами предыдущих наблюдений и дают возможность дополнить клиническую характеристику пациентов с АГ и различными сопутствующими состояниями, требующими индивидуализации терапии и комплексного, междисциплинарного подхода к лечению [10–15].
Заключение
Таким образом, у пациенток среднего возраста с АГ 1–2 степени и проявлениями КС, имеющих факторы риска развития ССЗ и их осложнений, такие как дислипидемия, ожирение, сахарный диабет, метаболический синдром и др., стартовая терапия препаратом Гипотэф (содержащим низкие дозы эналаприла, индапамида, метопролола тартрата и винпоцетина), в сравнении с комбинированным препаратом (содержащим полную терапевтическую дозу эналаприла и гидрохлортиазида), обеспечивает:
- эффективность антигипертензивной терапии, с достижением целевых значений через 12 недель, без эпизодов гипотонии и плохого самочувствия;
- нормализацию показателя ЧСС, в сочетании с коррекцией основных проявлений КС вегетативно-сосудистого характера, таких как головокружение, головная боль, сердцебиение, слабость;
- улучшение состояния когнитивной функции.
Литература
- Женщины и мужчины России 2018. Стат. сб. Росстат. М., 2018. 241 с.
- Cметник В. П. Медицина климактерия. Ярославль: Литера, 2006. 848 с.
- Шишкова В. Н. Сердечно-сосудистые заболевания в практике акушера-гинеколога // Российский вестник акушера-гинеколога. 2014; 4: 107–112.
- Синельникова М. Н. Цереброваскулярная патология в климактерическом периоде. Автореф. дис. к. м.н. Иркутск, 2004. 24 с.
- Шишкова В. Н. Проблемы старения и заместительная гормональная терапия у женщин в постменопаузе // Российский вестник акушера-гинеколога. 2013; 2: 42–47.
- Шишкова В. Н. Нейропротекция у пациентов с артериальной гипертонией: минимизация неблагоприятного прогноза // Терапевтический архив. 2014; 8: 113–118.
- Шишкова В. Н. Значение артериальной гипертензии в развитии поражения головного мозга — от легких когнитивных нарушений к деменции // Системные гипертензии. 2014; 11 (1): 45–51.
- Чазова И. Е., Жернакова Ю. В. от имени экспертов. Клинические рекомендации. Диагностика и лечение артериальной гипертонии // Системные гипертензии. 2019; 16 (1): 6–31.
- 2018 ЕОК/ЕОАГ Рекомендации по лечению больных с артериальной гипертензией // Российский кардиологический журнал. 2018; 23 (12): 143–228.
- Евдокимова А. Г. и др. Клиническая эффективность комбинированной антигипертензивной терапии в фиксированных дозах: фокус на Гипотэф // Терапия. 2016; 6 (10): 68–78.
- Скотников А. С., Хамурзова М. А. Органопротективные свойства гипотензивной терапии как профилактика развития «сосудистой» коморбидности // Лечащий Врач. 2017; 7: 16–24.
- Скотников А. С., Юдина Д. Ю., Стахнев Е. Ю. Гипотензивная терапия коморбидного больного: на что ориентироваться в выборе лекарственного средства // Лечащий Врач. 2018; 2: 24–30.
- Скотников А. С., Хамурзова М. А. Новые комбинации для комплексного лечения артериальной гипертензии в помощь врачу общей практики // Поликлиника. Кардиолог сегодня. Спецвыпуск. 2017/2018; 1: 47–55.
- Мамедов М. Н. Новый взгляд на стартовую терапию артериальной гипертонии у работающего пациента: практические аспекты концепции «полипилл» // Лечебное дело. 2017; 3: 26–30.
- Шишкова В. Н. Антигипертензивная терапия как основа нейропротекции в современной клинической практике // Лечащий Врач. 2019; 6: 2–6.
Л. А. Капустина**, кандидат медицинских наук
* ФГБОУ ВО МГМСУ им. А. И. Евдокимова Минздрава России, Москва
** ГБУЗ ГП 69 ДЗМ, Москва
1 Контатактная информация: Veronika-1306@mail.ru
DOI: 10.26295/OS.2019.66.50.002
Новые возможности в терапии артериальной гипертензии у женщин в менопаузе/ В. Н. Шишкова, Л. А. Капустина
Для цитирования: Лечащий врач № 7/2019; Номера страниц в выпуске: 12-16
Теги: женщины, климакс, антигипертензивные препараты
Купить номер с этой статьей в pdf