Колоректальный рак (КРР) является третьим по распространенности и вторым по летальности онкологическим заболеванием в мире: в 2020 г. диагноз КРР был установлен практически у 2 млн человек. Риск развития КРР в течение жизни составляет 4-5%. Высокие показатели смертности пациентов от КРР, до 50%, объясняются тем, что злокачественный процесс длительно протекает бессимптомно, а заболевание часто обнаруживается на IV стадии. Программы скрининга, которые сегодня реализуются на уровне общества, направленны на выявление злокачественного новообразования (ЗНО) на ранней стадии и определение предикторов и факторов риска развития патологического процесса (например, аденомы и зазубренные полипы, которые рекомендуется удалять при проведении колоноскопии до их малигнизации).
Каким бывает скрининг?
Программы скрининга КРР становятся частью рутинной врачебной практики. Они реализуются в двух основных формах.
- Оппортунистический скрининг предполагает выбор одного из нескольких доступных диагностических обследований, например, колоноскопии, КТ-колонографии или фекального иммунохимического теста (ФИТ).
- Организованные программы скрининга нацелены на определенные группы населения. В таких программах для формирования группы риска и отбора пациентов для последующей колоноскопии чаще всего применяют неинвазивный фекальный иммунохимический тест (ФИТ).
Наиболее эффективным с диагностической точки зрения подходом для снижения смертности пациентов с КРР сегодня является комбинация двух методов – теста на скрытую кровь в кале (гваяковая проба, gFOBT) с последующей колоноскопией.
Скрининг колоректального рака в рамках концепции персонализированной медицины
В рамках стратегий персонализированной медицины для повышения выявляемости КРР предлагается использовать оценку и суммирование имеющихся факторов риска и биомаркеров рака для создания общей «модели» или шкалы риска. Этот тип скрининга включает перекрестный (кросс-секционный) и продольный (лонгитюдный) скрининг. При кросс-секционном скрининге факторы риска и/или биомаркеры объединяют для определения вероятности развития прогрессирующих неоплазий на момент проведения теста и отбора пациентов для дальнейшей колоноскопии. При лонгитюдном скрининге модель суммарного риска используется для оценки вероятности развития неоплазий в будущем, например, в течение ближайших 10 лет, и выбора оптимальных стратегий для дальнейших обследований.
Кросс-секционный скрининг
- Модели на основе демографических и поведенческих факторов риска
Примером модели риска на основе демографических и поведенческих факторов является шкала Азиатско-Тихоокеанского колоректального скрининга. В рамках данной модели предикторами КРР являются возраст, пол, семейный анамнез (т.е. наличие КРР у прямых родственников первой линии родства) и статус курения. Для повышения чувствительности модели эти факторы риска можно комбинировать с результатами ФИТ.
- Модели риска на основе фекальных маркеров
Выявление фекальных биомаркеров может использоваться в качестве дополнения к ФИТ. Одним из примером является многоцелевой клинический тест на КРР на основе ДНК кала (мц-кДНК). Модель включает в себя комбинацию количественных результатов ФИТ и анализа генетических маркеров, обнаруженных в образцах кала, например, мутаций KRAS, аберрантного метилирования NDRG4 и BMP3 и ДНК маркера β-актина.
Другой биомаркер прогрессирующих неоплазий – белок кальпротектин. И хотя тест на кальпротектин малоэффективен в рамках массового скрининга в качестве единственного метода, исследования по его комбинации с ФИТ дают многообещающие результаты.
Результаты ФИТ также предлагается дополнять данными о состоянии кишечного микробиома. Например, ФИТ в комбинации с определением уровня Fusobacterium nucleatum значительно улучшает чувствительность теста в отношении к КРР и прогрессирующих неоплазий по сравнению с ФИТ.
Наконец, модели риска на основе фекальных биомаркеров могут включать летучие органические соединения (образующиеся из жидкостей или твердых тел (стул, моча) химические вещества, содержащиеся во вдыхаемом воздухе в виде газов). Так, изменения клеточного метаболизма, сопровождающие злокачественный процесс, можно выявлять с помощью «электронных сенсорных» («е-сенсорных») технологий, газовой хроматографии или масс-спектрометрии.
- Биомаркеры крови
Маркеры периферической крови или жидкостные биопсии набирают все большую популярность в скрининге КРР. Они включают ��атричную РНК (мРНК), микроРНК, внеклеточную ДНК (вкДНК), циркулирующую опухолевую ДНК (цоДНК), белки и внеклеточные везикулы. Одним из наиболее изученных маркеров периферический крови является циркулирующий метилированный ген SEPT9 (mSEPT9). Тест на этот ген уже одобрен FDA.
И хотя других генетических маркерах периферической крови известно гораздо меньше, сегодня ведутся активные разработки по их выявлению. Например, в недавнем исследовании ученые создали панель для определения маркеров вкДНК с использованием искусственного интеллекта.
Белковые маркеры, такие как карциноэмбриональный антиген (СЕА), также могут дополнить модели скрининга КРР.
Лонгитюдный анализ риска
Для разработки персонализированных стратегий скрининга КРР, обеспечении оптимальной профилактики при высоком онкологическом риске и, вместе с этим, минимизации ненужных обследований при низком риске развития заболевания, необходимо определение группы риска каждого пациента. Например, людям с высоким риском КРР рекомендуется чаще проходить и раньше начинать первый скрининг (ежегодное ФИТ вместо исследования один раз в два года). Вместе с этим, пользу от скрининга маловероятно получат люди с прогнозируемым 15-летним риском КРР <3%, а значит у лиц данной группы нет необходимости часто проходить скрининговые обследования. По сравнению с фиксированным подходом персонализированный подход позволяет дополнительно предотвратить 218 случаев и 156 смертей от КРР на 100 000 населения.
Для определения группы риска КРР могут использоваться калькуляторы и шкалы. Специальный калькулятор QCancer на основе данных о демографических (возраст, пол, этническая принадлежность) и поведенческих факторах (ИМТ, статус курения), а также личного и семейного анамнеза позволяет с высокой точностью оценить абсолютный риск развития КРР и семи других типов рака в течение следующих 10 лет.
Молекулярно-генетические данные также могут использоваться для долгосрочных прогнозов по риску КРР. В ряде работ предлагается ипользование однонуклеотидных полиморфизмов для создания полигенной шкалы риска (polygenic risk score, PRS) или шкалы генетического риска (genetic risk score, GRS).
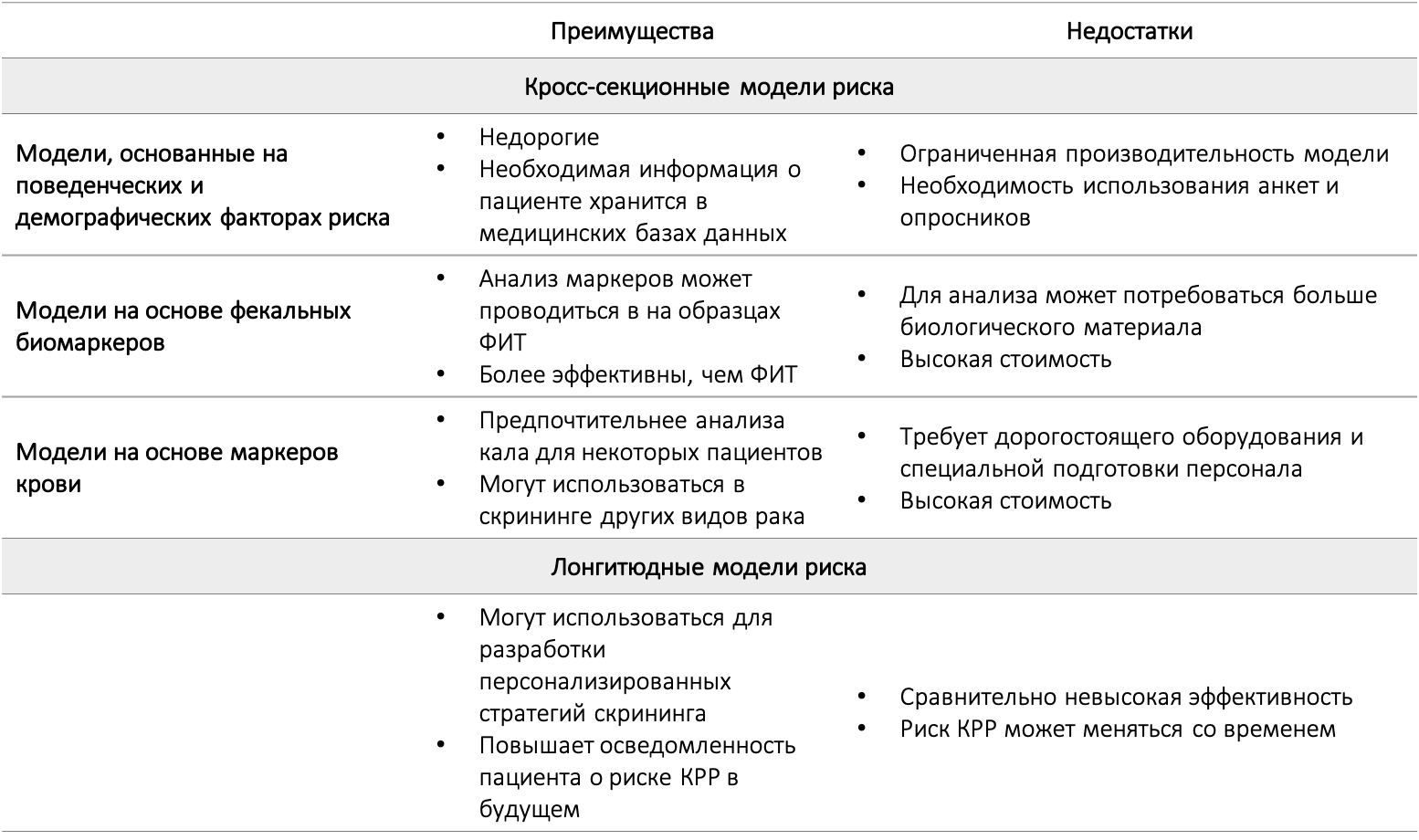
Потенциальные преимущества и недостатки современных моделей риска
Персонализированные подходы позволяют повысить выявляемость и снизить смертность от КРР. Однако для внедрения новых тестовых систем и моделей в широкую клиническую практику необходимы дальнейшие разработки в этой области, поскольку все еще остается много препятствий для внедрения новых моделей в программы массового скрининга. Требуется больше данных о влиянии оценки риска в рамках программ скрининга на реальный прогноз пациентов. Вместе с этим, даже если модель риска превосходит по эффективности текущие скрининговые тесты, ключевую роль в возможности ее реализации на уровне населения играет готовность целевых групп пройти обследование.
Материал подготовлен в рамках проекта «Медицина в точке бифуркации». Проект поддержан грантом Минобрнауки России в рамках федерального проекта «Популяризация науки и технологий»
Источник: Kortlever T, van der Vlugt M and Dekker E (2022) Future of Colorectal Cancer Screening: From One-Size-FITs-All to Tailor-Made. Front. Gastroenterol. 1:906052. DOI: 10.3389/fgstr.2022.906052