Григорьева Е.В., Хуторной Н.В., Солодов А.А., Крылов В.В.
Лучевая диагностика – неотъемлемый этап обследования пациента как на этапе диагностики, так и при подготовке к хирургическому вмешательству, а также при оценке эффективности назначенного лечения. Современные диагностические методики позволяют за короткое время получить достоверные данные о структуре и функции практически любого органа человека.
Поскольку все использующиеся сегодня радиологические методики задействуют волновое излучение, для их описания используется термин «лучевая диагностика». Началом эры лучевой диагностики можно считать 8 ноября 1895 года. В этот день произошло открытие рентгеновских лучей – позже, в 1901 г., за это Рентгену будет присуждена первая в истории Нобелевская премия по физике.
Первые рентгеновские изображения напоминали фотографии, и общественность восприняла их с энтузиазмом. Спустя полгода после публикации Рентгена уже появились изображения египетских мумий из музеев Вены и снимки костей конечностей, а авторитетные врачи советовали всем желающим увидеть изображение своего мозга. Современные Рентгену хирурги быстро нашли применение новому излучению для обнаружения инородных тел в организме пациента и в диагностике конкрементов мочевыделительных путей. В 1896 году доктор Henry W.Cattel из Университета Пенсильвании писал: «Хирургическое воображение может легко потеряться в бесконечных возможностях применения этого замечательного метода».
В России Х-лучи уже в 1896 году были названы рентгеновскими, возможно, по инициативе одного из учеников Рентгена – А.Ф. Иоффе. Первый рентгеновский аппарат был сконструирован А.С. Поповым в 1896 г., а в марте того же года профессор Н.В. Склифосовский начал регулярно использовать Х-лучи для диагностики переломов костей скелета.
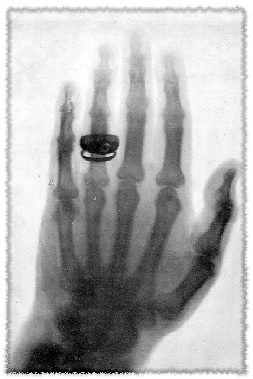
Рис.1. Рентгеновский снимок руки анатома Альберта фон Кёликера, сделанный Рентгеном во время доклада об открытии 28 декабря 1895 года в Физическом институте Вюрцбургского Университета
В 1897 году появились первые сообщения о заболеваниях, связанных с неконтролируемым использованием рентгеновского излучения. Просвинцованные защитные костюмы из свинца со временем стали неотъемлемой частью оборудования любого рентгеновского кабинета.
Согласно нормативам, сегодня суммарная эффективная доза облучения для здорового человека, проходящего профилактические обследования, не должна превышать 1мЗв в год.
Рис.2. Защитный костюм фельдшера рентгеновского кабинета, около 1918г.
Как и во времена Рентгена, сегодня по данным рентгеног��афии верифицируют переломы костей черепа, позвоночника и скелета, расхождение черепных швов, инородные тела, первично обызвествленные образования, скопление воздуха в полости черепа, в плевральной и брюшной полостях, патологию придаточных пазух носа, конкременты мочевыводящих путей и многие другие заболевания. Однако, несмотря на небольшую себестоимость и доступность рентгенологического метода, он отступает на второй план из-за низкой контрастности и невозможности визуализировать изменения мягких тканей. На смену классической рентгенографии приходит рентгеновская компьютерная томография.
Рентгеновская компьютерная томография (КТ) вошла в клиническую практику в 70-х годах прошлого века. Метод основан на послойном поперечном сканировании объекта тонким пучком рентгеновских лучей. Ткани организма по-разному абсорбируют излучение, и на основе этих различий можно построить изображение.
Теоретическую основу компьютерной томографии разработал A. MсCormak в 1956-1973гг, а сотрудник центральной научной лаборатории EMI Ltd G.N.Hounsfield сконструировал первый работающий вариант сканера. В 1979г. оба ученых были удостоены Нобелевской премии в области физиологии и медицины.
Рис.3. Первый рентгеновский компьютерный томограф EMI Mark I и первый аксиальный срез вещества головного мозга у женщины с внутимозговой опухолью, полученный 1 октября 1971г. (опухоль указана стрелкой)
Сегодня насчитывается 5 поколений компьютерных томографов, которые отличаются по характеру движения сканирующего устройства, виду пучка излучения и числу детекторов. Начиная с III поколения в КТ используется спиральная технология сканирования, при которой во время движения стола рентгеновская трубка и детекторы (либо только трубка) вращаются вокруг тела пациента на 360°. За одно вращение трубки можно получить от 16 до 360 срезов, что позволяет сканировать большие объемы за короткое время и с высоким пространственным разрешением. Например, можно получить одновременное изображение брахиоцефальных и интракраниальных артерий на фоне внутривенного болюсного контрастного усиления с высоким качеством визуализации сосудов диаметром до 1-2мм, что используется для оценки функционирования сосудистых анастомозов либо при распространённых стенозах внутренней сонной артерии и ее ветвей.
При спиральном сканировании в зависимости от области исследования доза эффективного облучения уменьшается до 88%, а максимальный объем сканирования увеличивается до 80-160см. Это позволяет производить onco check-up – сканирование головного мозга, шеи, органов грудной клетки, брюшной полости и малого таза за одно исследование у пациентов с опухолями и подозрением на метастатическое поражение. Внутривенное болюсное введение контрастного вещества с высокой скоростью помогает получить раздельное изображение артериальной, венозной и отсроченной фазы контрастирования и определить питающие сосуды опухоли, дифференцировать различные типы опухолевых образований, оценить распространенность и объем инвазии. По итогам исследования в клинике можно получить консультацию онколога для определения тактики лечения, назначения и проведения химиотерапии.
Рис. 4. КТ исследование (onco check-up) пациентки с рабдомиосаркомой плечевого пояса слева. Слева направо, сверху вниз: 2D реконструкция помогает определить объем опухолевых узлов (стрелки) и метастазов в регионарные лимфатические узлы (короткая стрелка); 3D реконструкция этого же объема позволяет оценить просвет брахиоцефальных и подключичной артерий на уровне опухоли; 3D реконструкция по программе onco check-up нужна для выявления очагов деструкции костей скелета; сканирование большого объема с контрастом позволяет диагностировать отдаленные метастазы в течение одного исследования (короткие стрелки)
Современной методикой исследования сосудистого русла является КТ-ангиография. Этот метод позволяет получать качественные изображения артерий и вен на уровне исследования за счет предварительного контрастирования. По данным российских и зарубежных клинических рекомендаций КТ-ангиография – один из обязательных предоперационных методов обследования у пациентов со стенозами и окклюзиями сонных и позвоночных артерий, патологической деформацией артерий головы и шеи, при болезни Такаясу и моямоя, стил-синдроме и диссекции артерий. Показаниями к операции служит не только определение степени стеноза артерии, но и протяженность стеноза, которую бывает трудно определить при дуплексном сканировании, особенно при стенозах и извитостях на уровне краниовертебрального перехода.
Рис. 5. КТ-ангиография, различные способы постобработки. Слева направо: MPR, реформация в сагиттальной плоскости, в ампулярном отделе внутренней сонной артерии частично кальцинированная бляшка (стрелка); тот же пациент, 3D реконструкция в программе transparent vessel; 3D реконструкция КТ-ангиографии у пациента с окклюзией внутренней сонной артерии (указана длинной стрелкой)
Одна из областей применения КТ-ангиографии – диагностика интракраниальных сосудистых образований, прежде всего аневризм и артериовенозных мальформаций, в том числе на фоне нетравматических внутричерепных кровоизлияний. По данным разных авторов, возможности КТ-ангиографии в диагностике интракраниальных аневризм практически равны дигитальной субтракционной церебральной ангиографии, а чувствительность и специфичность составляет 97,1% и 98, 5% соответственно. Мультипланарная реформация (MPR) и проекция максимальной интенсивности (MIP) достоверно передают взаимоотношения между аневризмой и несущим сосудом, а объемные (3D) реконструкции служат для отображения общего анатомического строения артериального круга и взаимоотношений аневризмы с костями основания черепа.
Современные томографы предоставляют возможность создания объемных реконструкций. Это выводит предоперационную подготовку на качественно новый уровень. Особенную ценность это предоставляет у пациентов с опухолями головы и шеи, интракраниальными образованиями, так как позволяют наглядно показать взаимное расположение опухоли и магистральных сосудов, костных структур, что облегчает планирование доступа и снижает риск осложнений.
Рис.6. КТ-ангиография у пациентов с интракраниальными аневризмами. Слева направо: аневризма кавернозного отдела внутренней сонной артерии, 3D реконструкция с костями черепа; аневризма бифуркации внутренней сонной артерии, 3D реконструкция после субтракции костей черепа (аневризмы указаны стрелками)
Технологии компьютерной томографии с успехом применяются в отделении лучевой диагностики КМЦ МГМСУ им.А.И.Евдокимова. В клинике установлен компьютерный томограф Aquillion (Toshiba), позволяющий получать 64 среза за одно вращение трубки с минимальной толщиной среза 0.5мм и программой снижения дозы облучения. В результате тесной работы с нейрохирургическим подразделением клиники, возглавляемым главным внештатным специалистом Минздрава РФ академиком В.В. Крыловым, рутинным исследованием в отделении стала КТ-ангиография интра-и экстракраниальных артерий и вен.
Активная работа в клинике челюстно-лицевых хирургов позволила развивать редкие для рутинной работы методики. КТ активно применяется для диагностики заболеваний слюнных желез. При КТ-сиалографии помимо визуализации протоков пораженной слюнной железы можно оценить состояние паренхимы самой железы, регионарных лимфатических узлов, а также диагностировать патологию и других слюнных желез на уровне исследования.
Лучевые методы активно применяются и в офтальмохирургии. За период 2017-2018гг. офтальмологами и нейрохирургами клиники было проведено более 20 операций по декомпрессии орбиты у пациентов с эндокринной офтальмопатией и экзофтальмом. Цель такой операции – уменьшить компрессию зрительного нерва за счет увеличенных экстраокулярных мышц и объема клетчатки. При подготовке к операции исследование орбит с внутривенным контрастным усилением позволяет оценить объем экстраокулярных мышц и ретробульбарной клетчатки, визуализировать состояние глазничных артерий и вен и степень компрессии зрительного нерва.
Рис.7. КТ исследование орбит у пациента с эндокринной офтальмопатией. Сверху вниз: 2D реконструкция в коронарной плоскости с оценкой толщины и формы экстраокулярных мышц и степени компрессии зрительного нерва; аксиальный срез с оценкой экзофтальма; сагиттальная 3D реконструкция позволяет определить ход глазничной артерии и состояние костных структур
Помимо описанных методик в отделении широко используют стандартные исследования головного мозга, позвоночника, крупных и мелких суставов. Основными показаниями для первичного проведения КТ являются сложные переломы, артрозы и опухоли, как при первичных костных образованиях, так и при метастатических поражениях.
Применение компьютерной томографии в многопрофильной клинике позволяет получить консультацию специалиста в день исследования и сразу определить тактику дальнейшего лечения.