Открытие роли Helicobacter pylori в патологии желудка полностью изменило терапевтические подходы к ведению пациентов с хроническим гастритом и снизило степень риска развития его осложнений. Наиболее актуальной задачей, реализуемой эрадикацией инфекции H. pylori на современном этапе развития медицины, является профилактика гастродуоденальных кровотечений и канцеропревенция рака желудка. На основе принципов доказательной медицины установлено, что инфекция
Эпидемиология
Результаты изучения распространенности инфекции H. pylori демонстрируют ее текущий положительный статус у каждого второго человека в мире [2, 3]. В экономически развитых странах указанный показатель составляет 15–35%, а в странах с низким социально-экономическим статусом достигает 80% [4, 5]. Данные об эпидемиологической ситуации с инфекцией H. pylori в Российской Федерации представлены локальными исследованиями и указывают на ее широкую распространенность, достигающую в некоторых регионах 90% [6].
Современные исследования указывают на длительную историю сосуществования рассматриваемой инфекции и Homo sapiens — по меньшей мере 60 000 лет [7, 8]. Распространение H. pylori происходит орально-оральным, фекально-оральным, ятрогенным путем от человека человеку, и особую роль играют механизмы внутрисемейной передачи [9].
Заражение
Современные стандарты диагностики и лечения
К референсным методам диагностики рассматриваемой инфекции относят дыхательный тест с 13С-меченой мочевиной и определение антигена H. pylori в кале. Также в качестве дополнительных методов первичной диагностики возможно использование быстрого уреазного теста в биоптате из антрального отдела и тела желудка, требующего проведения фиброгастроэзофагоскопии, и серологических методов определения антител к H. pylori, имеющих в свою очередь широкий спектр ограничений в интерпретации [12, 13].
Современное лечение больных с инфекцией H. pylori в качестве терапии первой линии включает стандартную тройную терапию: ингибитор протонной помпы (ИПП) в стандартной дозе 2 раза в сутки, кларитромицин (500 мг 2 раза в сутки) и амоксициллин (1000 мг 2 раза в сутки); также, как альтернативу, классическую четырехкомпонентную терапию на основе висмута трикалия дицитрата (120 мг 4 раза в сутки) в сочетании с ИПП (в стандартной дозе 2 раза в сутки), тетрациклином (500 мг 4 раза в сутки) и метронидазолом (500 мг 3 раза в сутки) [13, 14].
Актуальной терапией второй линии является классическая четырехкомпонентная терапия на основе висмута трикалия дицитрата при неэффективности стандартной тройной терапии или терапия, включающая ИПП в стандартной дозе 2 раза в сутки, левофлоксацин (500 мг 2 раза в сутки) и амоксициллин (1000 мг 2 раза в сутки). Терапию третьей линии подбирают на основании определения чувствительности H. pylori к антибиотикам, в том числе важно учитывать применение предшествующих схем лечения [13, 15].
В реальной клинической практике стандартная тройная терапия была и остается самой популярной схемой лечения пациентов с H. pylori-ассоциированными заболеваниями. В первую очередь это связано с ее относительной простотой, изученной эффективностью и безопасностью. Вместе с тем уровень эффективности указанной схемы последнее десятилетие снижался и схема требовала улучшения [16–18].
Меры по оптимизации эрадикационной терапии
Оптимизация стандартной тройной терапии, повышающая результат лечения, достигается увеличением продолжительности терапии: с 7 до 10 дней (ОР 0,80, 95% ДИ 0,70–0,91) и с 10 до 14 дней (ОР 0,69, 95% ДИ 0,52–0,91) [19].
Метаанализ A. G. McNicholl и соавт. продемонстрировал определенный вклад в увеличение результатов лечения при применении эзомепразола и рабепразола по сравнению с ингибиторами протонной помпы первых генераций [20].
Образовательная работа врача с пациентом, предоставляющая информацию о целях терапии, ее эффективности и безопасности, — основополагающая методика, определяющая приверженность к любому лечению, в том числе и эрадикации H. pylori. В частности, обучающая информация о патологических процессах и меры контроля за выполнением рекомендаций позволили повысить эффективность результатов лечения на 21%, а комплаентность на 68% [21].
Включение висмута трикалия дицитрата в эрадикационную терапию H. рylori приводит к повышению ее эффективности за счет прямого бактерицидного действия препарата, в том числе позволяющего преодолеть резистентность к кларитромицину [22, 23].
Исходя из вышеописанного «в идеале» тройная эрадикационная терапия в реальной клинической практике может выглядеть следующим образом: рабепразол или эзомепразол (20 мг 2 раза в сутки), кларитромицин (500 мг 2 раза в сутки), амоксициллин (1000 мг 2 раза в сутки) и висмута трикалия дицитрат (120 мг 4 раза в сутки) в течение 14 дней. Вместе с тем есть еще одно самое молодое и перспективное направление в борьбе с инфекцией H. рylori и разработке дополнительных мер повышения эффективности и безопасности эрадикационной терапии — применение пробиотиков.
Современные стратегии использования пробиотического антагонизма против H. pylori включают три перспективных направления: пробиотики как дополнение к эрадикации
Экспериментальной основой указанной стратегии являются результаты опытов in vivo. В частности, в 2 группах мышей, которые получали суспензию H. pylori в течение 7 дней, уровень инфицирования H. pylori составил 40% и 67%. При анализе состава желудочного микробиома между первой и второй группами обнаружены значимые отличия. В группе мышей с большей резистентностью к H. pylori преобладали Lactobacillus reuteri, L. murinus, L. johnsonii, демонстрирующие различную антихеликобактерную активность [25].
Установлено, что большинство лактобацилл производят молочную кислоту, которая ингибирует активность уреазы, и тем самым повреждают H. pylori [26]. Mukai и соавт. выявили, что L. reuteri влияет на колонизацию H. pylori путем секреции ганглиозидов сиаловой кислоты и тиолатов, которые ингибируют гликолипидную связь H. pylori с эпителиальными клетками желудка, а также конкурируют с H. pylori за адгезию азиало-ганглио-N-тетраозилцерамида и сульфатида [27]. В результате изучения более чем 700 штаммов L. reuteri был выделен уникальный штамм Lactobacillus reuteri DSMZ 17648 (Pylopass™), который содержит на своей поверхности адгезивные молекулы, распознающие поверхностные рецепторы
Экспертный совет Российской гастроэнтерологической ассоциации (РГА) под председательством академика РАН В. Т. Ивашкина провел 28 февраля 2018 г. заседание, целью которого был критический анализ значения L. reuteri DSMZ 17648 в эрадикационной терапии инфекции H. pylori. По результатам работы был принят ряд положений, в том числе: L. reuteri DSMZ 17648, благодаря адгезивным молекулам, распознающим поверхностные рецепторы H. pylori, способствует элиминации H. pylori со слизистой оболочки желудка; это свойство метабиотика на основе L. reuteri DSMZ 17648 позволяет рекомендовать использовать его при различных режимах эрадикационной терапии инфекции H. pylori в качестве биологически активной добавки к пище. В резолюции также отмечено, что необходимо дальнейшее изучение эффективности комбинирования Pylopass™ с различными режимами эрадикационной терапии H. pylori, для оценки оптимальных сочетаний с антибиотиками, продолжительности терапии и частоты возникновения нежелательных явлений [29].
Материал и методы исследования
В городе Екатеринбурге в 2018 г. стартовала программа по формированию территориального регистра эрадикационной терапии H. pylori у взрослых пациентов, в которой приняли участие врачи-гастроэнтерологи 7 медицинских учреждений. Показания для эрадикационной терапии у пациентов определялись в соответствии с национальными клиническими рекомендациями РГА [12].
В рамках регистра получены результаты эффективности и безопасности эрадикационной терапии H. pylori у 220 пациентов, принимавших в течение 14 дней ингибитор протонной помпы (рабепразол или эзомепразол) 20 мг 2 раза в день, кларитромицин 500 мг 2 раза в сутки и амоксициллин 1000 мг 2 раза в сутки, а также висмута трикалия дицитрат 120 мг 4 раза в сутки. Возраст больных данной группы (медиана, 25-й, 75-й процентили): 43 (34 ± 51) года. Женщины составили 62,3% от общего числа пациентов. Эрадикация H. pylori, оцениваемая с помощью уреазного дыхательного теста с 13С-меченой мочевиной, была достигнута у 199 (90,4%) пациентов. Нежелательные явления указанной схемы лечения зафиксированы в 58,6% случаев.
Значительную группу (217 человек) составили пациенты, получившие ингибитор протонной помпы (рабепразол или эзомепразол) 20 мг 2 раза в день, кларитромицин 500 мг 2 раза в сутки и амоксициллин 1000 мг 2 раза в сутки, а также висмута трикалия дицитрат 120 мг 4 раза в сутки в сочетании с Lactobacillus reuteri DSMZ17648 (Pylopass™) (1 капсула 2 раза) в течение 14 дней, с дальнейшим продолжением приема Lactobacillus reuteri DSMZ17648 (1 капсула 2 раза) на 4 недели. Возраст больных указанной группы: 41,0 (33 ± 51,5) год. Женщины составили 64% от общего числа данной группы пациентов. Эрадикация H. pylori, оцениваемая с помощью уреазного дыхательного теста с
Статистическая обработка результатов проводилась с использованием пакета прикладных статистических программ Statistica 7, Microsoft Exсel 2000. Отличия считали статистически значимыми при р < 0,05.
Сравнительные результаты
Статистический анализ сравнения эффективности схемы терапии без L. reuteri DSMZ 17648 и схемы терапии с данным метабиотиком продемонстрировал прирост положительных результатов эрадикации H. pylori на 5,9%. Примененный критерий χ2 Пирсона (с поправкой Иейтса), как непараметрический метод, который позволяет оценить статистическую значимость различий двух относительных показателей, установил статистическую достоверность полученных различий: χ2 = 5,14 (р = 0,024). Отношение шансов, как статистический показатель (на русском его название принято сокращать как ОШ, а на английском — OR от «odds ratio»), описывающий в численном выражении то, насколько отсутствие или наличие определенного исхода связано с присутствием или отсутствием определенного фактора в конкретной статистической группе, также выявило снижение риска неэффективности эрадикационной терапии при применении L. reuteri
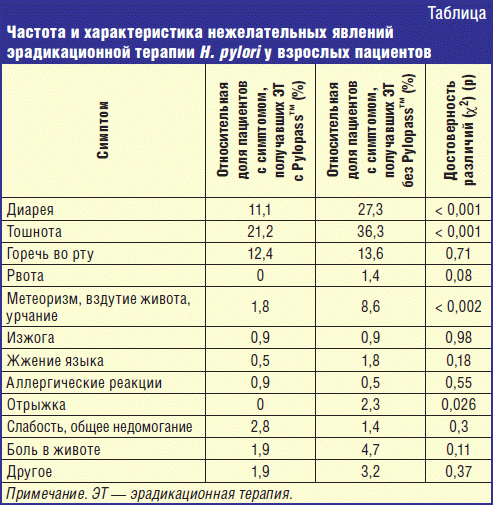
Статистический анализ сравнения безопасности схемы терапии с L. reuteri DSMZ 17648 и схемы терапии без данного метабиотика продемонстрировал снижение нежелательных явлений эрадикационной терапии на 18,1%. Примененный критерий χ2 Пирсона установил достоверность различий: χ2 = 14,29 (р < 0,001). Расчет отношения шансов выявил значительное снижение риска нежелательных явлений: ОШ 0,48 (0,33–0,71). В таблице представлен спектр, частота и характеристика нежелательных явлений схем эрадикационной терапии. Из данных таблицы видно, что такие симптомы желудочной диспепсии, как тошнота, рвота и отрыжка, встречались на 47% реже у пациентов, которые принимали L. reuteri DSMZ17648. Также в группе пациентов, которые получали эрадикационную терапию без метабиотика, у каждого третьего наблюдались симптомы кишечной дисфункции: диарея, метеоризм, вздутие живота и урчание. Прием L. reuteri DSMZ 17648 в комплексной терапии снизил частоту данного симптома более чем в 2,5 раза.
Обсуждение
Повышение эффективности терапии хеликобактерной инфекции у взрослых пациентов в реальной клинической практике при добавлении L. reuteri DSMZ 17648 объясняется, вероятно, как видоспецифическим для Lactobacillus воздействием молочной кислоты на активность уреазы, так и штаммспецифической способностью L. reuteri DSMZ17648 образовывать с H. pylori коагрегаты и тем самым нарушать колонизацию данной инфекции [26–28]. Указанный механизм, возможно, приводит к разрушению биопленки колонии микроорганизмов и обеспечивает повышение эффективности антибиотиков.
Эффективное снижение нежелательных явлений эрадикационной терапии, в основном связанных с применением двух антибактериальных препаратов, вероятно, объясняется регуляторным эффектом активных метаболитов L. reuteri DSMZ17648 на микробиом пациентов [30].
Заключение
В заключение представленных результатов важно отметить:
- Схема эрадикационной терапии: ингибитор протонной помпы (рабепразол или эзомепразол) 20 мг 2 раза в день, кларитромицин 500 мг 2 раза в сутки и амоксициллин 1000 мг 2 раза в сутки, а также висмут трикалия дицитрат 120 мг 4 раза в сутки в течение 14 дней является актуальной для реальной клинической практики, так как обеспечивает ее эффективность у 90,4%.
- Стандартная тройная терапия с висмутом длительностью 14 дней в 58,6% случаев сопровождается нежелательными явлениями.
- Дополнительное введение в стандартную тройную терапию с висмутом метабиотика Lactobacillus reuteri DSMZ17648 (Pylopass™) (1 капсула 2 раза) в течение 14 дней, с его дальнейшим приемом L. reuteri DSMZ17648 (1 капсула 2 раза) до 4 недель, увеличивает эффективность терапии на 5,9%, а частоту нежелательных явлений снижает на 18,1%.
- Mentis A., Lehours P., Megraud F. Epidemiology and Diagnosis of Helicobacter pylori infection // Helicobacter. 2015; 20 (1): 1–7.
- Salih B. A. Helicobacter pylori infection in developing countries: the burden for how long? // Saudi Journal of Gastroenterology. 2009; 15 (3): 201–207. DOI: 10.4103/1319-3767.54743.
- Go M. F. Natural history and epidemiology of Helicobacter pylori infection // Alimentary Pharmacology & Therapeutics. 2002; 16: 3–15. DOI: 10.1046/j.1365-2036.2002.0160s1003.
- Tonkic A., Tonkic M., Lehours P. et al. Epidemiology and Diagnosis of Helicobacter pylori Infection // Helicobacter. 2012; 17: 1–8. DOI: 10.1111/j.1523-5378.2012.00975.
- Mahadeva S., Raman M. C., Ford A. C. et al. Gastro-oesophageal reflux is more prevalent in Western dyspeptics: a prospective comparison of British and South-East Asian patients with dyspepsia // Alimentary Pharmacology & Therapeutics. 2005; 21: 1483–1490. DOI: 10.1111/j.1365-2036.2005.02455.
- Рахманин Ю. А., Герман С. В. Распространенность и пути трансмиссии пилорической хеликобактерной инфекции (обзор литературы) // Гигиена и санитария. 2014; 93 (4): 10-13.
- Wirth T., Wang X., Linz B. et al. Distinguishing human ethnic groups by means of sequences from Helicobacter pylori: Lessons from Ladakh // Proceedings of the National Academy of Sciences. 2004; 101: 4746–4751.
- Moodley Y., Linz B. Helicobacter pylori Sequences Reflect Past Human Migrations Genome // DYN. 2009; 6: 62–74. DOI: 10.1159/000235763.
- Kivi M., Tindberg Y. Helicobacter pylori occurrence and transmission: A family affair? // Scandinavian Journal of Infectious Diseases. 2006; 38: 407–417. DOI: 10.1080/00365540600585131.
- Salih B. A. Helicobacter pylori infection in developing countries: the burden for how long? // Saudi Journal of Gastroenterology. 2009; 15 (3): 201–207. DOI: 10.4103/1319-3767.54743.
- Logan R. P. H., Walker M. M. Epidemiology and diagnosis of Helicobacter pylori infection // British Medical Journal. 2001; 323: 9–20.
- Ивашкин В. Т., Маев И. В., Лапина Т. Л. и др. Рекомендации Российской гастроэнтерологической ассоциации по диагностике и лечению инфекции Helicobacter pylori у взрослых // Российский журнал гастроэнтерологии гепатологии и колопроктологии. 2012; 22 (1): 87–89.
- Malfertheiner P., Megraud F., O’Morain C. A. et al. Management of Helicobacter pylori infection — the Maastricht V Florence Consensus Report // Gut. 2017; 66: 6–30.
- Ивашкин В. Т., Маев И. В., Лапина Т. Л. и др. Лечение инфекции Helicobacter pylori: мейнстрим и новации (Обзор литературы и резолюция Экспертного совета Российской гастроэнтерологической ассоциации 19 мая 2017 г.) // Российский журнал гастроэнтерологии, гепатологии, колопроктологии. 2017; 27 (4): 4–21.
- Ивашкин В. Т., Маев И. В., Лапина Т. Л. и др. Клинические рекомендации Российской гастроэнтерологической ассоциации по диагностике и лечению инфекции Helicobacter pylori у взрослых // Российский журнал гастроэнтерологии, гепатологии, колопроктологии. 2018; 28 (1): 55–70.
- Graham D.Y. Efficient identification and evaluation of effective Helicobacter pylori therapies. Clinical Gastroenterology and Hepatology. 2009; 7: 145–148. DOI: 10.1016/j.cgh.2008.10.024.
- Graham D. Y., Fischbach L. Helicobacter pylori treatment in the era of increasing antibiotic resistance // Gut. 2010; 59: 1143–1153. DOI: 10.1136/gut.2009.192757.
- McNicholl A. G., Gasbarrini A., Tepes B. et al. Pan-European Registry on H. pylori Management (HP-EuReg): First-Line Treatments and Interim Analysis of 11272 patients // Helicobacter. 2015; 20 (1): 91.
- Yuan Y., Ford A. C., Khan K. J. et al. Optimum duration of regimens for Helicobacter pylori eradication // Cochrane Database of Systematic Reviews. 2013; 12. Art. №: CD008337. DOI: 10.1002/14651858.CD008337.
- McNicholl A. G., Linares P. M., Nyssen O. P. Metaanalysis: esomeprazole or rabeprazole vs. first-generation pump inhibitors in the treatment of Helicobacter pylori infection // Alimentary Pharmacology & Therapeutics. 2012; 36 (5): 414–425. DOI: 10.1111/j.1365-2036.2012.05211.
- Al-Eidan F. A., McElnay J. C., Scott M. G. et al. Management of Helicobacter pylori eradication — the influence of structured counselling and follow-up // British Journal of Clinical Pharmacology. 2002; 53: 163–171. DOI: 10.1046/j.0306-5251.2001.01531.
- Sun Q., Liang X., Zheng Q. et al. High efficacy of 14-day triple therapy-based, bismuth-containing quadruple therapy for initial Helicobacter pylori eradication // Helicobacter. 2010; 15: 233–238. DOI: 10.1111/j.1523-5378.2010.00758.
- Zhang W., Chen Q., Liang X. et al. Bismuth, lansoprazole, amoxicillin and metronidazole or clarithromycin as first-line Helicobacter pylori therapy // Gut. 2015; 64: 1715–1720. DOI: 10.1136/gutjnl-2015-309900.
- Qureshi N., Li P., Gu Q. Probiotic therapy in Helicobacter pylori infection: a potential strategy against a serious pathogen? // Applied Microbiology and Biotechnology. 2019; 103 (4): 1573–1588. DOI: 10.1007/s00253-018-09580-3.
- Zaman C., Osaki T., Hanawa T. et al. Analysis of the microbial ecology between Helicobacter pylori and the gastric microbiota of Mongolian gerbils // Journal of Medical Microbiology. 2014; 63: 129–137. DOI: 10.1099/jmm.0.061135-0.
- Hsieh P. S., Tsai Y. C., Chen Y. C. et al. Eradication of Helicobacter pylori infection by the probiotic strains Lactobacillus johnsonii MH-68 and L. salivarius ssp. salicinius AP-32 // Helicobacter. 2012; 17 (6): 466–477. DOI: 10.1111/j.1523-5378.2012.00992.
- Mukai T., Asasaka T., Sato E. et al. Inhibition of binding of Helicobacter pylori to the glycolipid receptors by probiotic Lactobacillus reuteri // FEMS Immunology and Medical Microbiology. 2002; 32 (2): 105–110. DOI: 10.1111/j.1574-695X.2002.tb00541.
- Holz C., Busjahn A., Mehling H. et al. Significant Reduction in Helicobacter pylori Load in Humans with Non-viable Lactobacillus reuteri DSM17648: A Pilot Study // Probiotics and Antimicrobial Proteins. 2015; 7: 91–100. DOI: 10.1007/s12602-014-9181-3.
- Ивашкин В. Т., Алексеева О. П., Барановский А. Ю. и др. Значение Lactobacillus reuteri DSMZ17648 в эрадикационной терапии инфекции H. pylori (обзор литературы и резолюция Экспертного совета, 28 февраля 2018 г.) // Российский журнал гастроэнтерологии гепатологии и колопроктологии. 2018; 28(3): 33–38.
- Li B. Z., Threapleton D. E., Wang J. Y. et al. Comparative effectiveness and tolerance of treatments for Helicobacter pylori: systematic review and network meta-analysis // British Medical Journal. 2015; 351: h4052. DOI: 10.1136/bmj.h4052.
Р. И. Акименко*
Е. И. Воронова**
Е. В. Гаранина**, кандидат медицинских наук
И. А. Гурикова**, кандидат медицинских наук
М. Э. Лосева***
О. Г. Марченко***
С. В. Одинец****
П. Ю. Пинигина**
О. А. Рябинина#
Е. Б. Фрезе##, кандидат медицинских наук
* ФГБОУ ВО УГМУ Минздрава России, Екатеринбург
** Европейский медицинский центр «УГМК-Здоровье», Екатеринбург
*** Медицинское объединение «Новая больница», Екатеринбург
**** Медицинский центр «Парацельс», Екатеринбург
# МАУЗ ГКБ № 40, Екатеринбург
## Многопрофильная клиника «Здоровье-365», Екатеринбург
1 Контактная информация: hlinov.doc@yandex.ru
DOI: 10.26295/OS.2020.45.81.004
Роль Lactobacillus reuteri DSMZ 17648 в эрадикационной терапии инфекции Helicobacter pylori у взрослых в реальной клинической практике/ И. Б. Хлынов, Р. И. Акименко, Е. И. Воронова, Е. В. Гаранина, И. А. Гурикова, М. Э. Лосева, О. Г. Марченко, С. В. Одинец, П. Ю. Пинигина, О. А. Рябинина, Е. Б. Фрезе
Для цитирования: Лечащий врач № 2/2020; Номера страниц в выпуске: 19-22
Теги: патология желудка, тройная терапия, висмут, антибиотики
Купить номер с этой статьей в pdf