Официальная презентация Римских критериев IV состоялась 22 мая 2016 г. на 52-й Американской гастроэнтерологической неделе (г. Сан-Диего, США).
Согласно определению Римских критериев IV, функциональные расстройства желудочно-кишечного тракта (ЖКТ) представляют собой нарушение кишечно-мозгового взаимодействия. Это группа расстройств, классификация которых основана на клинических симптомах, связанных между собой в любых сочетаниях: нарушение моторики, висцеральная гиперчувствительность, иммунная дисфункция, изменение функции слизистой кишечника, изменение микрофлоры кишечника, нарушение работы центральной нервной системы.
В Римских критериях IV (2016) сформулирована парадигма патогенеза функциональных гастроинтестинальных расстройств (ФГИР) как следствие стрессового воздействия с нарушением связей по оси «мозг — кишечник», в том числе на уровне иммунной регуляции, регуляции чувствительности, кишечной флоры и других компонентов, входящих в определение в зависимости от ведущего (ведущих) в данной (конкретной) клинической ситуации.
Ось «головной мозг — кишечник» представляет собой двунаправленную разветвленную коммуникационную сеть (табл. 1), которая посредством нейроиммунно-эндокринных медиаторов осуществляет мониторинг и интеграцию функций ЖКТ, реализует связь эмоциональных и когнитивных центров с ЖКТ (в плане его функциональной активности), координирует местные адаптивные реакции к стрессовым факторам любого рода. В свою очередь висцеротопические афферентные воздействия воспринимаются головным мозгом и оказывают влияние на ощущения боли, настроение и поведение человека.
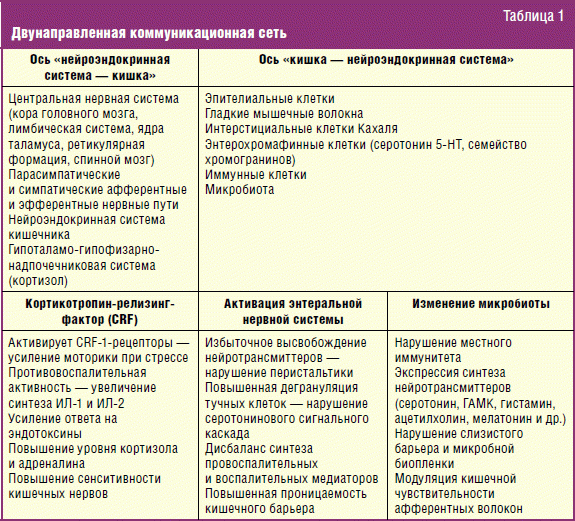
Под контролем этой разнонаправленной оси протекают все основные процессы, происходящие в ЖКТ: моторика, секреция, активность размножения кишечной флоры, всасывание, миграция флоры, микроциркуляция, местная иммунная защита, пролиферация клеток. Патологическая (нарушенная) активность этой системы и нарушение функциональных связей между ее структурами составляют патофизиологическую основу ФГИР. В зависимости от ведущего патофизиологического механизма (механизмов) составляет основу фармакологического, диетического и других лечебных воздействий.
В определение ФГИР, данное Римскими критериями IV, добавили раздел «Интестинальное микроокружение и функциональные гастроинтестинальные расстройства», которые объединяют наши знания о микробиоме, еде, питании и которые важны не только для понимания процессов, происходящих в ЖКТ, но и для воздействия на эту компоненту ФГИР.
Микробиота ЖКТ представляет собой тесное биологическое сообщество, включающее примерно 1014 бактерий, массой более 1 кг, которое можно рассматривать как самостоятельный экстракорпоральный орган человека (микробиом), участвующий в метаболических, иммунологических, защитных и пищеварительных процессах и влияющий на состояние других органов и систем и в целом на здоровье человека.
Микробиота кишечника включает около 400 различающихся между собой типов бактерий, объединенных в три энтеротипа:
- с преобладанием Bacteroides;
- с преобладанием Prevotella;
- с преобладанием Ruminococcus.
Большая часть микробиоты фиксирована к рецепторам слизистой, небольшая часть находится в свободном состоянии.
Микробиота ЖКТ очень важна в функциональном отношении. С ее участием синтезируются некоторые витамины (преимущественно группы В), метаболизируются желчные кислоты, происходит деградация ксенобиотиков, поддерживается энергетический гомеостаз, поддерживается местный и общий иммунный статус: трансформация лимфоцитов, активация противовоспалительных цитокинов, супрессия провоспалительных цитокинов, активируется продукция IgA, повышается толерантность слизистой к микробной агрессии и токсинам.
Кишечный микробиоценоз представляет собой высокоорганизованную экосистему, реагирующую качественными и количественными сдвигами на динамическое состояние организма человека в различных условиях жизнедеятельности. Он различен по своему составу в различных отделах ЖКТ. Так, в норме в проксимальных отделах тонкой кишки содержание бактерий не превышает 104–105 КОЕ в 1 мл аспирата. Содержание анаэробных бактерий в ЖКТ последовательно увеличивается по направлению к дистальному отделу. Нарушение баланса кишечной микробиоты, как количественное, так и качественное, может влиять на состояние ЖКТ. Одним из таких нарушений является синдром избыточного бактериального роста (СИБР) [2].
Микробиологическим критерием избыточного роста бактерий в тонкой кишке является наличие микроорганизмов (кишечная палочка и штаммы облигатных анаэробов: бактероидов, клостридий и иной), в концентрации более 105 КОЕ в 1 мл аспирата из тощей кишки [1].
Причин развития СИБР много, но если говорить о ФГИР, то следует отметить, что их развитию способствуют моторные расстройства ЖКТ, стаз кишечного содержимого, нарушение функции илеоцекального клапана, угнетение функциональной активности желудка и иммунных нарушений (лучевое воздействие, иммуносупрессивная терапия) [3–7].
Диагностика СИБР
Золотым стандартом диагностики СИБР является посев аспирата тонкой кишки, однако этот метод в исполнении имеет значительные издержки и в практической медицине не используется.
На сегодняшний день наиболее простыми и доступными и пригодными для практики являются водородные дыхательные тесты (ВДТ). Они позволяют высказать суждение о наличии СИБР по определению концентрации водорода в выдыхаемом воздухе.
В проведении ВДТ используется либо глюкоза, либо лактулоза, которая разлагается и утилизируется микробной флорой с образованием водорода, который всасывается в кровь и выделяется с выдыхаемым воздухом. При СИБР в тонкой кишке концентрация водорода возрастает, и по его уровню высказывается предположение о наличии СИБР и его выраженности.
Клинические проявления формируются местными (кишечными) симптомами и системными нарушениями, обусловленными транслокацией бактерий и их токсинов во внутренние среды организма (нарушением всасывания, иммунологическими расстройствами, потерей электролитов и др.). Так, при контаминации верхних отделов ЖКТ развивается клиническая картина дуоденита с дуоденальной гипертензией, затрудняющей пассаж секрета из печени, поджелудочной железы и расстройством пищеварения, реактивным мезаденитом, билиарными расстройствами. При контаминации нижних отделов тонкой кишки развивается вздутие живота, болезненность, снижается активность пищеварительных ферментов, возникает расстройство пищеварения, снижается масса тела.
Результаты собственных исследований
Мы оценили нарушение кишечного микробиоценоза вследствие избыточной колонизации кишечника у больных хроническим панкреатитом с внешнесекреторной недостаточностью поджелудочной железы: в лечение кроме ферментных препаратов включали препараты, устраняющие нарушение микробиоценоза кишечника (т. е. препараты про- и пребиотического ряда) [8, 9]. Предпочтение отдавали препаратам с пребиотическими свойствами, стимулирующими, в отличие от пробиотиков, изменение собственной микрофлоры, чтобы не вызывать лишней антигенной нагрузки [10].
В этом отношении преимущество имеют метабиотики — т. е. препараты, содержащие продукты метаболизма или структурные компоненты пробиотических микроорганизмов. Одним из известных представителей этой группы препаратов является комплексный метабиотик Бактистатин, который содержит продукты жизнедеятельности Bacillus subtilis (сенная палочка, грамположительная, спорообразующая аэробная бактерия), которая является антагонистом микроорганизмов: сальмонеллы, протея, стафилококков, стрептококков, дрожжевых грибков. Она продуцирует несколько видов метаболитов: метаболиты с антибактериальной активностью против названных микроорганизмов; метаболиты с ферментной активностью, которые участвуют в пищеварении. Вторым компонентом Бактистатина является сорбит «цеолит», который, проявляя сорбционные свойства к соединениям с низкой молекулярной массой (метан, сероводород, аммиак и другие токсические вещества), уменьшает различные виды интоксикации. Третьим является гидролизат соевой муки — источник аминокислот и олигосахаров. В целом препарат рассматривается как стимулятор роста и размножения собственной нормальной микрофлоры кишечника (в первую очередь «облигатной»).
Настоящее исследование посвящено оценке эффективности Бактистатина у больных с СИБР тонкой кишки, развившимся на фоне внешнесекреторной недостаточности поджелудочной железы (ПЖ). Лечение носило сочетанный характер: применялись Бактистатин и Эрмиталь.
Материалы и методы исследования
Изучено 78 больных, страдавших хроническим панкреатитом. 48 из них имели недостаточность внешнесекреторной функции поджелудочной железы, установленную по изучению эластазы 1 в кале (31 — имели умеренную и 17 — тяжелую степень).
У 30 больных микробная флора была изучена проведением бактериологического исследования кала исходно и в динамике лечения, а также изучены короткоцепочечные жирные кислоты (КЖК) (С2-С6) в биосубстратах методом газожидкостного хроматографического анализа — также исходно и в динамике лечения.
Микробная флора тонкой кишки была изучена у 48 больных с целью установления СИБР дыхательным водородным тестом с лактулозой. Оценивались также клинические проявления, данные биохимического исследования, общий анализ крови, карболеновая проба — исходно и в динамике.
Больные были разделены на группы.
- 1-ю группу составили 15 больных, которые получали Эрмиталь в адекватной дозе и Бактистатин.
- 2-ю группу составили 15 больных, которые получали Эрмиталь (при тяжелой степени функциональной недостаточности ПЖ — 144 ЕД по липазной активности — 6 больных и 108 ЕД при умеренной недостаточности поджелудочной железы — 9 больных).
В группах преобладали мужчины — 2:1, средний возраст больных составил 48 ± 3,07 года. Хронический алкогольный панкреатит имели 20 больных, билиарнозависимый — 6 и идиопатический — 4 человека. Группы были сопоставимы по полу, возрасту, этиологии и течению хронического панкреатита (ХП). Критериями оценки служили: динамика клиники, моторики кишечника (по карболеновой пробе), состояние дисбиоза.
- 3-ю группу составили 16 больных ХП и СИБР, которые получали Бактистатин и Эрмиталь.
- 4-ю группу составили 16 больных ХП и СИБР, которые получали Эрмиталь.
- 5-ю группу составили 16 больных ХП, которые были подобраны из архива, не получали терапию изучаемыми препаратами, но имели исходно СИБР и были оценены в динамике.
Бактистатин (кроме больных 5 группы) больные получали в стабильной дозе 2 капсулы 2 раза в сутки, 21 день. Эрмиталь получали в дозе, зависящий от степени внешнесекреторной недостаточности ПЖ в постоянном режиме, 5-я группа — «контрольная» — исходно терапию не получала.
Статистическую обработку изучаемых показателей производили с помощью пакета программ статистического анализа Statistica 7.0 for Windows 7 и Microsoft Office 2010. Для определения значимости средних значений рассчитывались t-критерии Стьюдента. Для оценки достоверности различий применялся альтернативный двусторонний анализ Фишера и χ2 с поправкой Йетса для малых чисел. Различия считались значимыми при величине р < 0,05.
Результаты исследования
1-я и 2-я группы, всего 30 больных (по 15 в каждой группе). По бактериологическому исследованию установлен дисбактериоз I–II ст. Кроме того, изучены метаболиты (по КЖК) кишечной микрофлоры. Исходные данные и результаты лечения представлены в табл. 2, 3.
Из представленных таблиц видно, что лечение было эффективным: основная симптоматика была купирована к 7–11 дням с четкой тенденцией восстановления моторики (укорочение времени транзита при запоре и удлинение при диарее); по данным КЖК — отмечена четкая тенденция к восстановлению дисбиоза, более того, и с нормализацией профиля КЖК у больных, получавших комбинированную терапию (Эрмиталь + Бактистатин). По мере восстановления эубиоза у больных с умеренной ферментативной недостаточностью удалось уменьшить дозу Эрмиталя, что сопровождалось повышением уровня фекальной эластазы 1.
Общее заключение по этому разделу исследования сводится к следующему:
- Бактистатин эффективно влияет на восстановление микробиоценоза кишечника у больных с внешнесекреторной недостаточностью ПЖ (при сочетанном лечении с ферментными препаратами).
- Сочетанная терапия (Бактистатин и Эрмиталь) позволяет уменьшить дозу ферментных препаратов. Это подтверждается повышением уровня эластазы кала, восстановлением моторики и купированием клинических проявлений.
3-я группа — 16 больных хроническим панкреатитом с развившимся СИБР.
Преобладали мужчины — 10/6, средний возраст составил 46 ± 4,03 года, продолжительность заболевания — 8 лет, у мужчин преобладала алкогольная форма — 9, у женщин билиарнозависимый панкреатит — 5; 2 больных имели идиопатическую форму.
Продолжительность лечения составила 3 недели, получали Бактистатин (2 капсулы 2 раза в день в сутки), Эрмиталь 72 тыс ЕД (в качестве препарата, участвующего в формировании функционального покоя ПЖ, восстанавливающего внутрибрюшное давление и пассаж секрета по протокам ПЖ).
4-я группа — 16 больных хроническим панкреатитом в стадии ремиссии, но с наличием СИБР, который и формировал клинические проявления: быстрое насыщение, тяжесть после еды, неустойчивый стул (с преобладанием запоров).
Возраст больных 48 ± 7 лет, преобладали мужчины — 11/5 и алкогольные и билиарнозависимые формы — 10/4, продолжительность болезни — 8 лет. СИБР имел умеренную форму выраженности.
Больные получали Эрмиталь в суточной дозе 72 ЕД по липазе. Продолжительность лечения составила 21 день.
5-я группа (контрольная), 16 больных ХП, которые были набраны из архива. В качестве критерия отбора был СИБР умеренной и легкой выраженности. Лечение по этому поводу, до отбора больных, не предпринималось. Больные были оценены в динамике с разницей в сроках обследования — 21 день. Так как больные находились в стадии ремиссии, то фармакотерапию по поводу ХП не получали.
Почему хронический панкреатит сопровождается развитием СИБР? Этому способсвуют два обстоятельства. Во-первых, в период обострений развивается та или иная степень ферментной недостаточности. Во-вторых, в лечении ХП используются блокаторы желудочной секреции, которые снимают кислотный барьер желудка, открывая доступ в нижележащие отделы микрофлоре из ротоглотки, желудка и дыхательных путей.
Состав микрофлоры, которая мигрирует в двенадцатиперстную кишку, представлен в табл. 4 и 5.
Этот спектр не противоречит влиянию — ферментному и антимикробному — Бактистатина.
В результате проведенного лечения у пациентов 3-й группы, получавших Бактистатин и Эрмиталь, на 7–10 день боли были полностью, либо в основном купированы. Клиническая симптоматика: восстановился стул, либо значительно уредился с тенденцией к оформлению, удлинилось время транзита у больных с наклонностью к диарее и уменьшилось время транзита у больных с преобладанием запоров (9–26 часов, 48–16 часов).
СИБР был купирован у 87% больных. В 4-й группе больных, получавших только Эрмиталь, клиническая симптоматика формировалась за счет нарушенного микробного спектра, который приводил к дуоденостазу, нарушению пассажа желчи и панкреатического секрета. Купирование симптоматики происходило в более отдаленные сроки — 14–15 дней. У части больных симптоматика уменьшилась, но полностью не купирована, максимально уменьшилась кишечная диспепсия (вздутие, урчание, частота стула). СИБР был купирован у 50% больных; у 25% уменьшилась интенсивность симптомов и у 25% больных — сохранился в исходной степени.
Больные 5-й контрольной группы, которые не получали никакой фармакотерапии, сохранили СИБР в исходном состоянии.
Таким образом, у больных, страдающих хроническим панкреатитом, развивается СИБР, в возникновении которого участвуют два патогенетических фактора:
- Использование блокаторов желудочной секреции в период обострения.
- Преходящее нарушение функциональной активности ПЖ (ферментная недостаточность), развивающееся в период обострения ХП.
Развитие СИБР у больных ХП сопровождается клиническими проявлениями (усугубление основной клиники, более медленное ее купирование или появление клинических проявлений в виде желудочной и/или кишечной диспепсии).
Использование в лечении нарушенного микробиоценоза Бактистатина в сочетании с ферментными препаратами (Эрмиталь) приводит к восстановлению микробиоценоза у 87% больных, только ферментная терапия купирует СИБР у 50% больных. Отсутствие лекарственного воздействия сохраняет СИБР, ведет к его прогрессированию и способствует обострению хронического панкреатита.
Из представленных данных можно сделать следующее заключение:
- Бактистатин эффективно влияет на восстановление микробиоценоза толстой кишки у больных с внешнесекреторной недостаточностью поджелудочной железы.
- Сочетанное применение Бактистатина и Эрмиталя позволяет уменьшить дозу ферментных препаратов. Это сопровождается восстановлением микробиоценоза, моторики и ускоряет купирование кишечных проявлений.
- Ферментные препараты (Эрмиталь) эффективно купируют СИБР у 50% больных хроническим панкреатитом.
- Сочетанная терапия (Бактистатин + Эрмиталь) устраняет СИБР у 87% больных хроническим панкреатитом, что сопровождается купированием клиники, восстановлением моторики и укорачивает период активного лечения.
- Ардатская М. Д., Минушкин О. Н. Синдром избыточного бактериального роста: определение, современные подходы к диагностике и лечебной коррекции // Consillium medicum. 2012, № 2, с. 45–49.
- Miazda A., Osinki M., Cichy W., Zaba R. Current views on the ethiopathogenesis, clinical, manifestation, diagnostics, treatment and correlation with other nosological entities of SIBO // Advences in Medical Sciences. 2015, March. Vol. 60, issue 1. P. 118–124.
- Sachdev A. H., Pimentel M. Gastrointestinal Bacterial Overgrowth Pathogenesis and clinical significance // Ther. Adv. Chron Dis. 2013. Sep. Vol. 4, № 5. P. 223–231.
- Quigley E. M. Small Intenstinal Bacterial Overgrowth: What it is and what it is not // Current Opinion in Gastroenterology. 2014, Mar. Vol. 30, № 2. P. 141–146.
- Compare D. et al. Effect of long-term PPI treatment on producing bowel symptoms and SIBO // Eur. J. Clin. Invest. 2011, Apr. Vol. 41, № 4. P. 380–386.
- Логинов В. А., Минушкин О. Н. Синдром избыточного бактериального роста у больных гастроэзофагеальной рефлюксной болезнью, длительно принимающих ингибиторы протонной помпы // Кремлевская медицина. Клинический вестник. 2014; 2: 30–33.
- Минушкин О. Н., Кручинина М. А. Синдром избыточного бактериального роста у больных дивертикулярной болезнью толстой кишки // Кремлевская медицина. Клинический вестник. 2014; 1: 99–104.
- Madseu J. et al. Bile acid malabsorbcion or disturled intestinal permeability in patients treated with enzyme substitution for exocrine pancreatic insulfcieacy is not caused by bacterial overgrowth // J Pancreas. 2003, vol. 65. P. 175–179.
- Старостин Б. Д. Комбинированная терапия хронического панкреатита (двойное, слепое, плацебо-контролируемое пилотное исследование) // Эксперементальная и клиническая гастроэнтерология. 2003, № 3, с. 58–65.
- Маев И. В., Кучерявый Ю. А. Заместительная ферментная терапия при панкреатической недостаточности // Клинические перспективы гастроэнтерологии, гепатологии // 2005, № 5.
Т. Б. Топчий1, кандидат медицинских наук
ФГБУ ДПО ЦГМА УДП РФ, Москва
1 Контактная информация: tantop@mail.ru
Функциональные гастроинтестинальные расстройства в определении Римских киртериев IV и некоторые лечебные подходы, зависящие от этого/ О. Н. Минушкин, Т. Б. Топчий
Для цитирования: Лечащий врач № 5/2018; Номера страниц в выпуске: 84-88
Теги: внешнесекреторная недостаточность, функциональные расстройства, желудочно-кишечный тракт
Купить номер с этой статьей в pdf