Язвенный колит (ЯК) — распространенное заболевание, с наблюдаемой тенденцией к ежегодному увеличению случаев выявления. Преимущественно поражаются лица молодого и трудоспособного возраста [1]. Пик заболеваемости приходится на возрастной период 20–29 и 50–55 лет [2, 3]. При неэффективности консервативной терапии или развитии осложнений заболевания, оперативные вмешательства при ЯК выполняются у 10–20% пациентов, с летальностью 12–50%. Этиология ЯК до сих пор неизвестна [1, 4]. Одним из важных факторов, осложняющих его течение, является микрофлора толстой кишки, которая может влиять на процесс обострения заболевания. При воспалительных заболеваниях кишечника у больных нарушена иммунологическая толерантность к бактериям, населяющим желудочно-кишечный тракт [5, 6]. При развитии ЯК нарушается барьерная функция слизистой толстой кишки, при этом бактериальные агенты могут проникать в глубокие ткани кишки, запуская каскад воспалительных и иммунных реакций [5–8]. Нарушение целостности слизистой оболочки создает благоприятные условия для обсеменения транзиторной микрофлорой пораженного участка [9].
Микроорганизмы, находящиеся в слизистой оболочке и на поверхности язвенно-некротических образований, принимают непосредственное участие в развитии обострений ЯК. С целью уменьшения бактериального воспаления назначают антибактериальные препараты [1–4]. В настоящее время отсутствует единое мнение о применении антибактериальной терапии у пациентов с ЯК.
Целью настоящего исследования было улучшение результатов лечения пациентов с язвенным колитом путем коррекции антибактериальной терапии на основании данных микробиологического исследования микрофлоры подслизистого слоя толстой кишки.
Материалы и методы исследования
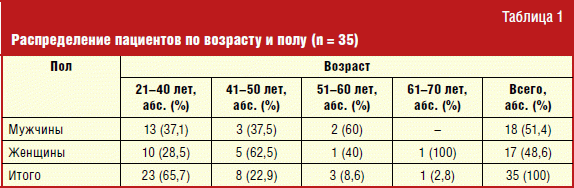
Обследовано 35 пациентов с ЯК в возрасте от 28 до 61 года, средний возраст пациентов 37,6 года, которые находились на амбулаторном и стационарном лечении в отделениях колопроктологии и гастроэнтерологии Клиник СамГМУ с января по май 2017 г. Мужчин было 18 (51,4%), женщин 17 (48,6%) (табл. 1). Критерии включения в исследование: пациенты обоих полов в возрасте от 20 до 70 лет включительно, подписавшие информированное согласие, с впервые выявленным ЯК или перенесшие не более двух атак заболевания; левосторонний или тотальный уровни поражения; отсутствие в лечении биологической терапии. Критерии исключения из исследования: возраст меньше 20 лет или старше 70 лет; сахарный диабет, симптомы декомпенсации хронической сердечной недостаточности, наличие системных аутоиммунных заболеваний или онкопатологии, психические заболевания, препятствующие проведению обследования, беременность или кормление грудью, недееспособность пациента, хронические специфические инфекции — туберкулез, ВИЧ-инфицирование (СПИД) и др., судимость либо нахождение под следствием на момент начала исследования, отказ от сотрудничества и несоблюдение медицинских рекомендаций.
Всем больным выполнялись стандартные клинические и лабораторные исследования, ирригоскопия, ректороманоскопия, фиброколоноскопия с биопсией.
Тяжесть ЯК оценивали по критериям J. G. Truelove и L. I. Witts (1955) с дополнениями Е. А. Белоусовой [4, 10]. Легкая форма ЯК была у 4 (11,4%), среднетяжелая у 18 (51,5%), тяжелая у 13 (37,1%) пациентов (табл. 2).
Проктит выявлен у 16 (45,7%), левосторонний колит у 11 (31,4%), тотальное поражение у 8 (22,9%) больных.
Терапия включала базисные препараты, содержащие 5-аминосалициловую кислоту (месалазин), фолиевую кислоту, стероидные гормоны (преднизолон, гидрокортизон) и симптоматические средства (спазмолитики — папаверин, Но-шпа).
Препараты месалазина являются средством базового лечения ЯК легкого и среднетяжелого течения. Помимо противовоспалительного действия, заключающегося в ингибировании липооксигеназного пути метаболизма арахидоновой кислоты, торможения синтеза и освобождения простагландинов и лейкотриенов, ингибировании провоспалительных цитокинов, антиоксидантном действии и др., месалазин обладает и антимикробным эффектом. Показано, что месалазин ингибирует бактериальный рост, подавляя активность генов, ответственных за метаболизм, рост и ответ кишечных бактерий (Kaufman et al., 2009). Антимикробные свойства 5-аминосалициловой кислоты в отношении различных бактериальных штаммов (C. perfringens, C. difficile, C. botulinum и C. tetani) защищены патентом США в 2001 г. (US Patent 6326364).
В качестве лекарственного препарата месалазина мы применяли Салофальк в различных лекарственных формах (для перорального приема — гранулы и таблетки, для ректального введения — свечи, клизмы, пена). Выбор именно Салофалька в нашем исследовании обусловлен, во-первых, многообразием лекарственных форм месалазина, что позволило подобрать оптимальный режим терапии в зависимости от локализации воспаления. Так, при проктитах мы применяли свечи Салофальк в дозе 1–1,5 г/сут или ректальную пену в дозе 1 г/сут. В некоторых случаях проктосигмоидита применялась комбинация из местных и пероральных форм препарата; учитывая более высокую эффективность гранул по сравнению с таблетками в терапии дистальных форм колита (L. Leifeld et al., 2011), предпочтение отдавалось гранулам Салофалька. Терапия левостороннего и тотального колита состояла в основном из комбинации клизм (2–4 г/сутки) или пены (1–2 г/сут) и гранул Салофалька (в дозе 3 г/сутки) или таблеток (доза 3–4 г/сут). Согласно современным европейским и российским рекомендациям комбинированная терапия, за счет гораздо более высокого (чем при монотерапии) уровня месалазина в слизистой оболочке кишечника, более эффективна по сравнению с монотерапией только пероральными препаратами. Во-вторых, было показано, что, несмотря на то, что все препараты месалазина позволяют достичь ремиссии, время до наступления улучшения может существенно отличаться. Максимально быстрое разрешение симптомов (стул ≤ 3 сут) с полным прекращением ректального кровотечения достигается при использовании гранул Салофалька — уже на 11–12 день (рис.) (W. Kruis и соавт., 2009; V. Gross и соавт., 2011). С клинической точки зрения эти данные являются крайне важными для оценки терапевтического ответа на терапию месалазином и определения дальнейшей тактики лечения (продолжение терапии месалазином или назначение системных стероидов), поскольку, согласно современным рекомендациям, данный ответ следует оценивать на 14-й день. Разница в скорости наступления эффекта обусловлена различным профилем высвобождения месалазина у разных препаратов.
При среднетяжелой и тяжелой формах ЯК пациентам назначали инфузионную терапию, аминокислоты, хлористый калий, витамины группы B, гемостатические препараты, парентеральное питание, антибактериальную терапию в соответствии с данными микробиологического исследования микрофлоры биоптата стенки кишки.
Собирался биопсийный материал язвенных поражений слизистой оболочки толстой кишки во время проведения фиброколоноскопии или ректороманоскопии до начала лечения и после выполнения колопроктэктомии (n = 7).
Сбор материала проводили в соответствии с методическими указаниями МУ 4.2.2039–05 «Техника сбора и транспортирования биоматералов в микробиологические лаборатории» и клиническими рекомендациями. Собирался биопсийный материал язвенных поражений слизистой оболочки толстой кишки во время проведения фиброколоноскопии или ректороманоскопии. Выделенные культуры идентифицировали с использованием MALDI-TOF масс-спектрометрии. У всех выделенных культур определяли антибиотикорезистентность диско-диффузионным методом в соответствии с клиническими рекомендациями и методическими указаниями МУК 4.2.1890–04 «Определение чувствительности микроорганизмов к антибактериальным препаратам». У всех энтеробактерий дополнительно определяли фенотипы продукции β-лактамаз расширенного спектра действия методом двойных дисков с цефалоспоринами III поколения и амоксициллином/клавулановой кислотой [6, 8].
Результаты и их обсуждение
Из биопсийного материала 35 пациентов было выделено и идентифицировано 65 штаммов микроорганизмов. Видовой состав выделенных микроорганизмов представлен в табл. 3.
У 6 пациентов (20%) микроорганизмы были выделены в монокультуре, у 24 пациентов (68%) было выделено от 2 до 4 штаммов, у 3 (4%) пациентов определено 5 штаммов микроорганизмов. Роста микрофлоры не было выделено из двух проб биопсийного материала (8%) пациентов.
Выделено 34 штамма в титре 105 КОЕ в биоптате, 4 штамма — в титре 106 КОЕ в биоптате, 15 штаммов — в титре 104 КОЕ в биоптате, 7 штаммов — в титре 103 КОЕ в биоптате.
С учетом видовых особенностей, факторов патогенности и данных по участию микроорганизмов в воспалительных процессах в толстой кишке выделенную микрофлору можно разделить на три группы:
1) представители нормальной микрофлоры толстой кишки — 16 штаммов;
2) микроорганизмы, участие которых в процессе воспаления неизвестно, — 9 штаммов;
3) микроорганизмы, имеющие высокий потенциал в поддержании антимикробного воспаления, — 40 штаммов.
При анализе чувствительности к антибиотикам выделенных штаммов было выявлено, что 45% из них имеют признаки резистентности к 1–2 группам лекарственных препаратов, у 33% отмечены признаки поливалентной резистентности к трем и более группам. Эрадикация такой флоры представляет сложности и, с нашей точки зрения, требует назначения комбинированной терапии после исследования биоптата [11].
При оценке количественного состава выделенной микрофлоры у пациентов с легкой степенью заболевания микрофлора в стенке толстой кишки отсутствовала либо определялись низкие титры высеянных штаммов (102–103 КОЕ на биоптат). У пациентов со средней степенью тяжести и тяжелым течением заболевания в 50,0% и 53,8% соответственно выявлена выраженная микробная контаминация подслизистого слоя (количество микроорганизмов 105–106 КОЕ на биоптат), большое разнообразие видов (более 3). Согласно клиническим рекомендациям, антибактериальная терапия показана пациентам с тяжелой атакой заболевания при наличии лихорадки или подозрении на кишечную инфекцию, но, по нашему мнению, при этом необходимо учитывать видовой состав микрофлоры и ее чувствительность к антибактериальным препаратам. В 50% при течении средней степени тяжести и в 46,2% при тяжелой атаке заболевания микробная контаминация стенки толстой кишки отсутствует либо выражена слабо (количество микроорганизмов 10
При сравнительном анализе результатов микробиологических исследований биоптатов, взятых при фиброколоноскопии, до выполнения оперативного вмешательства (n = 28) и после выполнения колопроктэктомии (n = 7) из биоптатов удаленной части толстой кишки были получены идентичные данные.
По нашему мнению, важность детального исследования видового состава энтерококков у пациентов с ЯК обусловлена высокими рисками распространения их во внутрибольничной среде и формированием множественной лекарственной устойчивости, что согласуется с литературными данными [8, 12].
Выводы
- Всем пациентам с язвенным колитом необходимо исследовать микробный состав кишечной стенки с целью оптимизации тактики проводимого лечения.
- Микроорганизмы в титре 105–106 КОЕ, их большое видовое разнообразие поддерживают воспаление в толстой кишке и препятствуют его купированию.
- Результаты микробиологического исследования стенки толстой кишки у пациентов с обострением язвенного колита могут служить критерием для назначения антибактериальной терапии, а также являться прогностическим признаком при определении показаний к хирургическому лечению.
- Воробьев Г. И., Халиф И. Л. Неспецифические воспалительные заболевания кишечника. М.: Миклош, 2008. 400 с.
- Ивашкин В. Т., Лапина Т. Л. Гастроэнтерология: национальное руководство. М.: ГЭОТАР-Медиа, 2008. 700 с.
- Комаров Ф. И., Осадчук А. М., Осадчук М. А. и др. Неспецифический язвенный колит. М.: ООО Медицинское информационное агентство, 2008. 256 с.
- Белоусова Е. А. Язвенный колит и болезнь Крона. Тверь: ООО «Изд-во Триада», 2002. 128 с.
- Лягина И. А., Корнева Т. К., Головенко О. В. и др. Характеристика кишечной микрофлоры у больных язвенным колитом // Рос. журн. гастроэнтерол., гепатол. и колопроктол. 2008. № 2. С. 48–54.
- Sandler R. S., Eisen G. M. Epidemiology of inflammatory bowel disease. Inflammatory bowel disease / Ed. J. B. Kirshner. Fifth edition. Saunders, 2000. P. 89–113.
- Жуков Б. Н., Исаев В. Р., Андреев П. С., Каторкин С. Е., Чернов А. А. Комплексное лечение неспецифического язвенного колита с применением эндолимфатической терапии // Новости хирургии. 2012. Т. 20, № 2. С. 49–54.
- Reid K. C., Cockerill F. R. III, Robin Patel. Clinical and Epidemiological Features of Enterococcus casseliflavus/flavescens and Enterococcus gallinarum Bacteremia: A Report of 20 Cases // Clin Infect Dis. 2001, Jun 1; 32 (11): 1540–1546. Epub 2001 Apr 30.
- Лямин А. В., Андреев П. С., Жестков А. В., Жуков Б. Н. Антибиотикорезистентность грамотрицательной микрофлоры, выделенной из биопсийного материала у больных неспецифическим язвенным колитом // Клиническая микробиология и антимикробная химиотерапия. 2010. Т. 12, № 4. С. 342–346.
- Truelove S. C. et al. Cortisone in ulcerative colitis; final report on a therapeutic trial // Br Med J. 1955; 2: 1041–1048.
- Давыдова О. Е., Андреев П. С., Каторкин С. Е. Язвенный колит — особенности диагностики и лечения // Научно-практический журнал гастроэнтерология Санкт-Петербурга. 2017. № 1. С. 76–77.
- Давыдова О. Е., Каторкин С. Е., Лямин А. В., Андреев П. С. Улучшение результатов лечения пациентов с язвенным колитом с использованием индивидуальных схем эрадикационной терапии условно-патогенной микрофлоры, основанных на микробиологическом мониторинге // Врач-аспирант. 2016. Т. 77, № 4. С. 49–55.
О. Е. Давыдова1
П. С. Андреев, кандидат медицинских наук
С. Е. Каторкин, кандидат медицинских наук
А. В. Лямин, кандидат медицинских наук
А. А. Горюнов
И. В. Киселева, кандидат медицинских наук
ФГБОУ ВО СамГМУ МЗ РФ, Самара
1 Контактная информация: doctorproct@mail.ru
Купить номер с этой статьей в pdf