Черепно-мозговая травма (ЧМТ) занимает первое место в современном мире по суммарному экономическому и медико-социальному ущербу, опережая цереброваскулярную патологию и сердечно-сосудистые заболевания, что определяется временной и стойкой нетрудоспособностью, инвалидизацией и летальностью среди наиболее активной части общества — у лиц молодого и среднего возраста [1, 2].
В различных странах мира предпринимаются значительные и схожие по характеру усилия, направленные на профилактику травматизма и преодоление его последствий, в основе которых лежат социально-общественные, организационно-методические и медицинские мероприятия [3–5].
В настоящее время с позиций доказательной медицины установлено, что существует два основных механизма повреждения мозга при травме: первый обусловлен разрушительным воздействием механической энергии на мозговое вещество в момент получения травмы; второй — дополнительным повреждением мозга после травмы, вызываемым факторами вторичного его повреждения [6].
Меры по совершенствованию средств защиты людей от травматизма, проведение различных профилактических мероприятий, принятие превентивных мер административного и процессуального характера позволяют уменьшить число случаев травматизма, т. е. обстоятельств, при которых реализуется разрушающее воздействие на мозг фактора первичного его повреждения — механической энергии [7].
Но все эти меры не эффективны по отношению к факторам вторичного повреждения, дополнительно поражающим уже пострадавший мозг, действие которых реализуется сразу после травмы и непосредственно определяет результаты лечения и исход острого периода травмы.
Известно, что у больных с легкой травмой головы (более 12 баллов по шкале ком Глазго (ШКГ)), которые составляют абсолютное большинство (90% пострадавших), цифра летальности приближается к 0%. У пациентов со средней тяжестью ЧМТ (9–12 баллов по ШКГ) цифры летальности колеблются от 5% до 20%. У больных с тяжелой ЧМТ (менее 8 баллов по ШКГ), составляющих всего 10% пострадавших, летальность достигает по данным разных авторов от 38% до 80% [8].
Анализ многоцентровых клинических исследований, проведенный ведущими специалистами мира, занимающимися проблемой церебральной травмы, с применением методов доказательной медицины позволил разработать и внедрить международные рекомендации по лечению пострадавших с тяжелой травмой мозга [9]. Применение этих рекомендаций, основанных на доказательных медицинских исследованиях в клинической практике, обусловило снижение летальности при тяжелой травме мозга более чем в 2 раза [10, 11]. За этим последовало создание подобных рекомендаций для больных с легкой и среднетяжелой травмой мозга [12]. Важным итогом этих исследований стало представление об универсальности механизмов вторичного повреждения травмированного мозга, реализующихся вне зависимости от тяжести первичной травмы, поскольку, как оказалось, в основе этих механизмов лежит развитие ишемии и гипоксии мозга [13]. Условно весь комплекс терапевтических мероприятий, доказательно применяемых для предупреждения вторичного повреждения мозга, может быть разделен на три составляющих: физиологическую, хирургическую и медикаментозную [14]. Предупреждение эпизодов артериальной гипотензии, коррекция нарушений газообмена, поддержание нормотермии, борьба с внутричерепной гипертензией, нормализация нутритивного статуса больного и многое другое — все это может быть объединено как физиологическая составляющая лечебного комплекса по предупреждению вторичной ишемии мозга, объединяемой международным термином «secondary brain insults» [9]. Этому же служит и хирургическая составляющая — хирургическое пособие, применяемое по строгим показаниям в рамках протоколов по эвакуации патологического внутричерепного содержимого (гематомы, геморрагические очаги ушибов) и декомпрессии черепа путем краниотомии, что также опционально представлено в современных рекомендациях по ведению пострадавших с травмой мозга.
Обращает на себя внимание то, что с позиций доказательной медицины в современных рекомендациях отсутствуют какие-либо указания относительно медикаментозной составляющей терапии вторичной ишемии мозга при его травме. В то же время изучение патофизиологии ЧМТ выявило чрезвычайную чувствительность поврежденного мозга прежде всего к ишемии и гипоксии. Именно поэтому развитие церебральных повреждений происходит не только в момент травмы (первично), но и в течение продолжительного времени после нее в связи с действием факторов вторичного (ишемическо-гипоксического) повреждения мозга. С учетом остроты развития вторичной ишемии мозга в острейшем периоде травмы и ее значения для исхода острого периода травмы, актуальным является применение достижений доказательной медицины в области фармакологической нейропротекции [15]. Причем наибольший интерес на сегодняшний день представляют препараты, обладающие как нейропротективными, так и нейрорепаративными свойствами, усиливающие эндогенные механизмы нейропластичности.
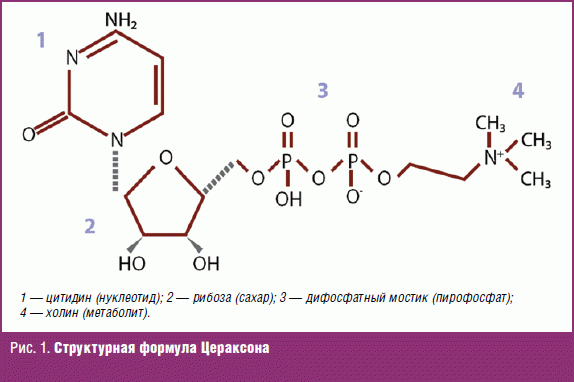
В этой связи большой интерес вызывает цитиколин (Цераксон) — эндогенное промежуточное соединение в цикле Кеннеди (синтез мембранных фосфолипидов и сфингомиелина), играющее важную роль в восстановлении и поддержании структурной целостности нейрональных мембран, внутриклеточных органелл (микросом, митохондрий), миелиновых оболочек нервных стволов [16]. Помимо этого препарат уменьшает накопление свободных жирных кислот, препятствует процессам окислительного стресса и апоптоза, позитивно влияет на холинергическую передачу, стимулируя образование ацетилхолина, модулирует дофамин-, глутаматергическую нейротрансмиссию [17]. В ряде экспериментальных работ показано также, что цитиколин обладает выраженным нейрорепаративным эффектом, стимулируя процессы нейропластичности, нейро- и ангиогенеза [18–20]. Мультипотентность Цераксона как лекарственного средства обусловлена его уникальной формулой (рис. 1), в структуру которой входит цитидин, дифосфат, рибоза и холин, что позволяет не просто доставить метаболит (холин) к месту его потребления (в нервную ткань), но и запустить процессы его метаболизации (восстановления мембранных комплексов нейрональных клеток и миелиновой оболочки нервных стволов) [21–24].
Биологическая доступность Цераксона приближается к 100%, причем она практически одинакова как при парентеральном, так и при пероральном приеме; будучи аналогом эндогенного цитиколина, препарат на 84% включается в обменные процессы, прежде всего в нервной ткани. Это объясняет отсутствие каких-либо описаний побочных эффектов препарата при его клиническом применении, в том числе у больных с острым инсультом, в критических состояниях с острыми церебральными повреждениями при остром отеке мозга, при внутричерепной гипертензии [25–27]. Положительные эффекты препарата были продемонстрированы в многочисленных исследованиях при инсульте, черепно-мозговой травме различной степени тяжести, а также у пожилых пациентов с когнитивными расстройствами сосудистого и нейродегенеративного генеза [16].
Ряд ранее проведенных клинических исследований по применению Цераксона у больных с травматическим повреждением мозга продемонстрировал благоприятный профиль безопасности препарата вне зависимости от дозировки и длительности применения, тяжести больных и дозировок, а также положительные клинические эффекты в виде ускорения реабсорбции отека головного мозга и восстановления как сознания, так и неврологических функций, что приводило к сокращению длительности госпитализации и улучшению качества реабилитации. Более того, в случаях ЧМТ легкой или умеренной степени Цераксон достоверно снижал длительность и тяжесть так называемого постконтузионного синдрома и уменьшал выраженность когнитивных расстройств [28–30].
Все это позволило в 2009 году инициировать многоцентровое, двойное слепое, плацебо-контролируемое исследование (CORBIT) по применению Цераксона у более чем 1200 больных с ЧМТ различной тяжести. Уже на уровне дизайна исследования был допущен ряд противоречий, а именно: только пероральная форма приема препарата (2000 мг в течение 90 дней); разнородность групп больных по тяжести и характеру травмы; малая приверженность больных к лечению (только 44,4% больных приняли 75% препарата на курс лечения). Все эти недостатки дизайна исследования обусловили получение в конечном итоге положительного, но не достаточного по доказательной силе результата [31].
Учитывая противоречия, возникшие после публикации исследования COBRIT, было интересным оценить реальное влияние цитиколина на восстановление пациентов после ЧМТ. Проведенный метаанализ рандомизированных исследований применения препарата при травмах мозга, включая COBRIT (рис. 2), показал достоверный положительный эффект Цераксона, что заключалось в улучшении функционального восстановления, уменьшении продолжительности пребывания в стационаре, сокращении периода дальнейшей реабилитации [32].
Стоит отметить, однако, что результаты, полученные на основе принципов доказательной медицины, следует использовать как ориентир в ежедневной врачебной практике и, сочетая их с личным опытом использования, стараться улучшать исходы пациентов. Цитиколин (Цераксон) уже вошел в рекомендуемый протокол лечения больных с травмой мозга в ряде стран [33]. Его применение в лечебных учреждениях и амбулаторно в нашей стране при травме мозга обосновывается позитивными эффектами препарата, а также превосходным профилем безопасности, который явно продемонстрирован не только в клинических исследованиях, но и в ежедневной практике.
При терапии ЧМТ важно подчеркнуть необходимость рационального использования всех составляющих лечения: базовой терапии, применения протоколов хирургического лечения при травме мозга и медикаментозного лечения с включением в терапию препаратов нейропротективного профиля. Так, исходя из личного клинического опыта, целесообразным является прием Цераксона с началом терапии в острейшем периоде и ее продолжением в последующем не менее 45–90 дней; причем у пациентов без нарушений глотания оптимальным является прием пероральной формы в виде саше, содержащего суточную дозировку 1000 мг [34].
Таким образом, ЧМТ является одной из наиболее важных социально-экономических и медицинских проблем современности. Первичное повреждение мозга механической энергией при травме, вне зависимости от причины травмы, ее характера и вида является основой оценки тяжести и состояния больного при его догоспитальном осмотре, определяя первичный клинический диагноз, формируя стратегию и тактику неотложных мероприятий лечебно-диагностического характера. Вторичное повреждение мозга начинает формироваться сразу после его травмы и обусловлено действием факторов вторичного повреждения мозга (внутричерепных и внечерепных). В основе вторичного повреждения мозга лежит универсальный (биологический) механизм ишемическо-гипоксического поражения, что сближает механизмы повреждения мозга после травмы с ишемией вещества мозга при церебральном инсульте и его последствиях, определяя единые подходы к цито- и нейропротективной терапии. Медикаментозная составляющая терапии при травме мозга до последнего времени была ограничена отсутствием доказательных клинических исследований по применению лекарственных препаратов, направленных на защиту нервных клеток и мозга в целом. Особое место в ряду лекарственных средств с нейропротективным действием занимает Цераксон. Совокупность фармакологических эффектов препарата и результатов клинических исследований при острой и хронической ишемии мозга позволяет рекомендовать практическое применение Цераксона при травме мозга различной степени тяжести начиная с острейшего периода травматического процесса.
Литература
- Waxweiler R. J., Thurman D., Sniezek J. et. al. Monitoring the impact of traumatic brain injury: A review and update // J. Neurotrauma. 1995; 2: 509–516.
- Corrigan J. D., Selassie A. W., Orman J. A. The epidemiology of traumatic brain injury // J. Head Trauma Rehabil. 2010; 25: 72–80.
- Розенфельд Л. Г., Тесленко В. Р., Сорокун Н. В. Некоторые аспекты организации медицинской помощи пострадавшим от травм, отравлений и несчастных случаев на догоспитальном этапе в современных условиях. Бюллетень НИИ соц. гигиены, экономики и управлением здравоохранения им. Н. А. Семашко. М., 1997. C. 209–214.
- Теодоридис К. А. О состоянии дорожной безопасности в странах Европейского Союза // Вестник травматологии и ортопедии им. Н. Н. Приорова. 1998; 3: 48–53.
- Всемирный доклад о предупреждении дорожно-транспортного травматизма. Всемирная организация здравоохранения и Всемирный Банк Развития, 2004. С. 257
- Bullock M. R., Pavlishock J. T. Guidelines for management of severe traumatic brain injury // J. of Neurotrauma. 2007; 24 (1): 1–106.
- Leibson C. L., Brown A. W., Ransom J. E. et al. Incidence of traumatic brain injury across the full disease spectrum: a population-based medical record review study // Epidemiology. 2011; 22 (6): 836–844.
- Narayan R. K., Miechel M. E., Ansel B. et al. Clinical trials in head injury // J. Neurotrauma. 2002; 19: 223–236.
- Bullock R., Chesnut R. M., Clifton G. et al. Guidelines for management of severe head injury. Brain Trauma Foundation // J. of Neurotrauma. 2000; 17: 451–533.
- Andrews P. J., Sleeman D. H., Statham P. F. et al. Predicting recovery in patients suffering from traumatic brain injury by using admission variables and physiological data: a comparison between decision tree analysis and logistic regression // J Neurosurgery. 2002; 97 (2): 326–336.
- Lu J., Marmarou A., Choi S. et al. Mortality from traumatic brain injury // Acta Neurochir. 2005; 95: 281–285.
- NICE. Head Injury: triage, assessment, investigation and early management of head injury in infants, children and adults. National Collaborating Centre for Acute Care. Guideline commissioned by the National Institute for Clinical Excellence, 2003. 248.
- Maas A. I., Stocchetti N., Bullock R. Moderate and severe traumatic brain injury in adults // Lancet Neurol. 2008; 7: 728–741.
- Амчеславский В. Г., Генералов В. О., Амчеславская Е. В. Черепно-мозговая травма. Изд. МАИ-ПРИНТ, 2011; 48 с.
- Leker R. R., Shohami E. Cerebral ischemia and trauma-different etiologies yet similar mechanisms: neuroprotective opportunities // Brain Res Brain Res Rev. 2002; 39: 55–73.
- Secades J. Citicoline: pharmacological and clinical review, 2010 update // Rev Neurol. 2011; 52 (Suppl 2): S1-S62.
- Hurtado O., Moro M. A., Cardenas A. et al. Neuroprotection afforded by prior citicoline administration in experimental brain ischemia: effects on glutamate transport // Neurobiol Dis. 2005; 18 (2): 336–345.
- Gutierrez-Fernandez M. et al. CDP-choline treatment induces brain plasticity markers expression in experimental animal stroke // Neurochemistry International. 2012; 60: 310–317.
- Hurtado O., Hernandez-Jimenez M., Zarruk J. G. et al. CDP-choline increases Sirtuin1 expression concomitant to neuroprotection in experimental stroke // J. Neurochem. 2013; 126 (6): 819–826.
- Diederich K. et al. Citicoline Enhances Neuroregenerative Processes After Experimental Stroke in Rats // Stroke. 2012; 43 (7): 1931–1940.
- Chida N., Shimizu Y. Biosynthesis of myelin lipids of cultured nervous tissues. Incorporation of choline and CDP-choline into myelin phospholipids // Tohoku J. Exp. Med. 1973; 111: 41–49.
- Baburina I., Jackowski S. Apoptosis triggered by 1-O-octadecyl-2-O-methyl-rac-glycero-3-phosphocholine is prevented by increased expression of CTP: phosphocholine cytidylyltransferase // J. Biol. Chem. 1998; 273: 2169–2173.
- Klein J. Membrane breakdown in acute and chronic neurodegeneration: Focus on choline-containing phospholipids // J. Neural. Transm. 2000; 107: 1027–1063.
- Farooqui A. A., Horrocks L. A., Farooqui T. Glycerophospholipids in brain: their metabolism, incorporation to membranes, functions, and involvement in neurological disorders // Chem Phys Lipids. 2000; 106: 1–29.
- Cho H. J., Kim Y. J. Efficacy and safety of oral citicoline in acute ischemic stroke: drug surveillance study in 4191 cases // Methods Find Exp Clin Pharmacol. 2009; 31 (3): 171–176.
- D’ Orlando K. J., Sandage B. W. Citicoline (CDP-choline): mechanisms of action and effects in ischemic brain injury // Neurol. Res. 1995, 17: p. 281–284.
- Adibhatla R. M. Citicoline in stroke and TBI clinical trials // Nat Rev Neurol. 2013, 9: 173.
- Calatayud M. V., Calatayud P., Aso E. J. Effects of CDP-choline on the recovery of patients with head injury // J. Neurol Sci. 1991; 103: 15–18.
- Tanovich A., Alfaro V., Secades J. J. Citicoline in treatment of traumatic brain damage // Drugs of Today. 2004, 40 (Suppl. B), p. 1–18.
- Lozano R. CDP-choline in the treatment of cranio-encephalic traumata // J. Neurol Sci. 1991; 103: 43–47.
- Zafonte R., Bagiella E., Ansel B. M. et al. Effect of citicoline on functional and cognitive status among patients with traumatic brain injury: Citicoline Brain Injury Treatment Trial (COBRIT) // JAMA. 2012; 308 (19): 1993–2000.
- Secades J. J. Citicoline for the Treatment of Head Injury: A Systematic Review and Meta-analysis of Controlled Clinical Trials // J. Trauma Treat. 2014; 4 (1): 2–4.
- Maejima S., Katayama Y. Neurosurgical trauma in Japan // World J. Surg. 2001; 25 (9): 1205–1209.
- Амчеславский В. Г. Нейропротективная терапия в остром периоде церебральных поражений. Методическое пособие (для специалистов здравоохранения), М., 2009, с. 29.
В. Г. Амчеславский*, 1, доктор медицинских наук, профессор
В. О. Генералов**, доктор медицинских наук
Е. В. Амчеславская**, кандидат медицинских наук
* НИИ НДХиТ ДЗМ, Москва
** Центр диагностики и лечения эпилепсии, Москва
1 Контактная информация: vamches@mail.ru
Купить номер с этой статьей в pdf