Рожа лица и рожа нижних конечностей как острое стрептококковое заболевание встречается повсеместно, без тенденции к снижению в обозримом будущем. Чаще всего воспалительный процесс развивается на нижних конечностях (67%), реже — на лице (24%). Многие авторы указывают на связь рожи нижних конечностей с наличием соматических заболеваний, таких как ожирение, сахарный диабет 2-го типа и фоновая грибковая инфекция стоп и ногтей. Не менее часто фактором, предрасполагающим к развитию рожи, являются хроническая венозная недостаточность (ХВН) и хроническая лимфовенозная недостаточность (ХЛВН) [1–6].
В последние годы частота выявления геморрагических форм рожи заметно нарастает, что заставляет исследователей особое внимание уделять состоянию сосудистой стенки и системы свертывания крови в целом [7–10].
Протеин С, витамин К-зависимая протеаза, синтезируется в печени, откуда поступает в кровоток. В норме он находится в неактивном состоянии. При инфекционно-воспалительных процессах в крови наблюдается связывание протеина С с кофактором (протеином С) и дальнейшее его взаимодействие с тромбомодулином и эндотелиальным рецептором протеина С. Активированный протеин С (АПС) ингибирует каскадный механизм свертывания на ранней стадии тромбинообразования (за счет инактивации Va и VШа факторов свертывания). Другой важной его функцией является способность ускорять плазминоген-зависимый лизис тромба, что является прямым проявлением его ангиопротекторных свойств. Снижение протеина С коррелирует с уровнем плазминогена в крови при инфекционно-септических состояниях [11–19].
Различные исследования показали, что подавление реакций активации протеина С вызывает резкое увеличение продукции интерлейкина-6 и интерлейкина-8, фактора некроза опухоли и других цитокинов и снижает толерантность организма к различным эндотоксинам. Получены до��азательства того, что протеин С не только блокирует активацию лейкоцитов, но и регулирует активность матричных металлопротеиназ, вызывающих деградацию экстрацеллюлярного матрикса и локальное изъязвление [18, 19, 22–26].
Предотвращение эндотелиальной дисфункции микроциркуляторного русла эффективно используется для профилактики и лечения многих заболеваний [18, 19]. На этом фоне роль протеина С (одного из ключевых эндотелий-зависимых антикоагулянтов) в формировании дисфункции сосудистой стенки при роже изучена слабо.
Мы попытались восполнить имеющийся пробел, изучив динамику протеина С у больных рожей нижних конечностей (с наличием и без наличия хронической венозной недостаточности) в сравнении с больными рожей лица и здоровыми добровольцами для уточнения патогенеза и определения целесообразности проведения заместительной (антитромботической) терапии.
Пациенты и методы исследования
Обследовано 60 человек в возрасте от 25 до 71 года с диагнозом «рожа нижних конечностей II степени тяжести» (36) и «рожа лица II степени тяжести» (24). Эритематозная форма рожи была установлена в 33% всех наблюдений (в 52% при роже лица), эритематозно-буллезная в 15%, эритематозно-геморрагическая в 22% и буллезно-геморрагическая в 30% случаев. Эритематозно-геморрагическая (11 случаев) и буллезно-геморрагическая (15 случаев) рожа развивались на нижних конечностях чаще, чем на лице (2 и 3 случая соответственно). Частота геморрагических нарушений была достоверно выше при местном воспалительном процессе (78%) на нижних конечностях по сравнению с лицом (20%); отношение шансов (ОШ) = 9,9 [2,8; 34,7].
Первичная рожа лица (16 женщин, 8 мужчин) диагностирована в 92% случаев и преобладала у женщин. При роже нижних конечностей случаи первичной рожи регистрировались в 50%, повторной в 31% и рецидивирующей в 19%; в отличие рожи лица: первичной (92%), повторной (4%) и рецидивирующей (4%). Риск рецидива рожи был статистически достоверно выше при локализации воспалительного очага на ногах по сравнению с лицом (ОШ) = 5,55 [1; 51,2], p = 0,009.
При роже нижних конечностей гендерное соотношение было сопоставимым (мужчин — 17, женщин — 19). Среди сопутствующих заболеваний обращала на себя внимание высокая (88%) частота микозов стоп и онихомикозов. У 11 больных было ожирение от 2-й до 4-й степени, у 5 больных субкомпенсированный сахарный диабет 2-го типа.
У больных рожей лица фоновая патология в 37,5% была представлена кожными заболеваниями (заушный дерматит, стрептодермия, псориаз) и в 29% — хронической ЛОР-патологией (отит, тонзиллит, ринит). Сахарный диабет 2-го типа — у четырех человек.
Пациенты находились на стационарном лечении в отделении рожи ИКБ № 2 г. Москвы. 32 больным назначена антибактериальная монотерапия: бензилпенициллина новокаиновая соль внутримышечно по 0,6 млн МЕ два раза в сутки (7–10 дней) и еще двум больным — цефалоспорины (цефазолин) внутримышечно по 1 г 3 раза в сутки (5 дней). Комбинированная терапия из двух антибиотиков (бензилпенициллина новокаиновая соль внутримышечно по 0,6 млн МЕ два раза в сутки (7–10 дней) и Ципролет per os по 0,5 г два раза в сутки (10 дней)) проведена 14 больным. 12 человек пролечены комбинацией из трех антибиотиков (бензилпенициллина новокаиновая соль внутримышечно по 0,6 млн МЕ два раза в сутки (7 дней) + ципрофлоксацин внутривенно по 800 мг в сутки (3 дня) с последующим переводом на 1 г в сутки per os (10 дней) + цефазолин внутримышечно по 1 г 3 раза в сутки (5 дней)). Дополнительно пациенты получали: антигистаминные препараты (Зодак, диазолин), местную физиотерапию и регулярную обработку рожистого очага нижних конечностях дубящим раствором перманганата калия. Пациенты, участвующие в исследовании, не получали лекарственные средства с направленным действием на состояние системы гемостаза. Средний срок пребывания больных в стационаре с рожей нижних конечностей составил 11,9 ± 4,1 дня; с рожей лица — 8,4 ± 1,6 дня.
Исследование ключевых показателей системы гемостаза проводили в начале заболевания (1–3 день — 1-я точка), в динамике (4–6 и 7–10 день — соответственно точки 2, 3) и в периоде реконвалесценции (11–15 дни болезни — 4-я точка исследования). Каждому третьему больному рожей нижних конечностей проводилось катамнестическое исследование (через 5 месяцев после выписки из стационара), позволяющее разграничить изменения, вызванные рожей, от фона сопутствующих заболеваний.
Контрольная группа состояла из 32 здоровых лиц в возрасте от 24 до 50 лет в равном соотношении мужчин и женщин.
Содержание протеина С в плазме крови определяли на автоматическом коагулометре SYSMEX CA-500 (Siemens Healthcare, США, реагенты Siemens AG, Германия) в экспресс-лаборатории детской городской клинической больницы № 13 им. Н. Ф. Филатова ДЗ г. Москвы совместно с врачом клинической лабораторной диагностики Н. К. Лагутиной. Всего обработано 90 образцов плазмы.
Статистическая обработка полученных результатов проводилась с помощью программы Statistica 10.0 for Windows 7.0. Критический уровень значимости (достоверности) был принят как p < 0,05. В таблице результаты приведены как Mе + s (медиана и стандартное отклонение). В случае статистически значимых различий между группами вычислялось отношение шансов (ОШ) и 95% доверительный интервал (ДИ) (ОШ [-95%ДИ; +95%ДИ]).
Полученные результаты
Исходные значения протеина С на 1–3 дни болезни (при поступлении) в группе больных рожей нижних конечностей были ниже (81,9 ± 4,9%), чем у больных рожей лица (94,1 ± 6,0%) и достоверно ниже контрольных значений (100 ± 5%, р < 0,05) (табл. 1).
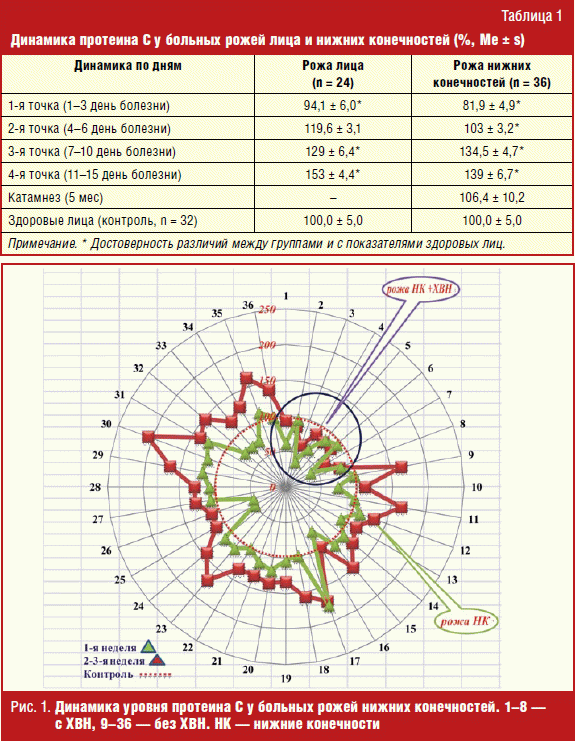
По мере угасания рожистого очага уровень протеина С постепенно восстанавливался в обеих группах: 119,6 ± 3,1 на 4–6 день болезни, 129 ± 6,4% на 7–10 день болезни, 153 ± 4,4% на 11–15 день болезни — при роже лица (р < 0,05 между 1/4, 2/4 и 3/4 точками исследования) и 103 ± 3,2%, 134,5 ± 4,7%, 139 ± 6,7% при роже нижних конечностей (р < 0,05 между 1/4, 2/4 точками исследования).
Полученные значения протеина С логично укладывались в общую картину эндотелиальной дисфункции микроциркуляторного русла, ранее описанную нами у больных рожей [20, 21]. В то же время динамика протеина С у отдельных больных: с 49,7% (1-я точка исследования) до 112% (4-я точка) — прирост 125%; с 48,9% (1-я точка) до 110,7% (4-я точка) — прирост 126%; с 65,5% (1-я точка) до 119,7% (4-я точка) — прирост 86%, заслуживает внимания как эффективный механизм работы факторов саногенеза в кровеносном русле в периоде реконвалесценции (рис. 2, табл. 2).
У больных рожей нижних конечностей с сопутствующей хронической венозной недостаточностью активность протеина С оставалась ниже нормы в течение всего периода наблюдений (рис. 1).
Так, у больных рожей нижних конечностей без ХВН (n = 28) уровень протеина С был 99,8 ± 4,7% в остром периоде болезни и увеличился до 140 ± 4,5% в стадии реконвалесценции (р < 0,001) (табл. 2). При роже нижних конечностей с ХВН исходно низкий уровень протеина С — 69,8 ± 8,1% статистически значимо не менялся в периоде реконвалесценции — 79,15 ± 4,0%, р = 0,21 (табл. 3). Различия были настолько выразительными, что в публикацию включены все абсолютные значения протеина С, полученные у больных рожей нижних конечностей с наличием (табл. 2) и без наличия признаков ХВН (табл. 3).
Кроме того, период реконвалесценции у больных рожей нижних конечностей без признаков ХВН (и положительной динамикой протеина С) протекал более благоприятно, чем у больных рожей нижних конечностей с сопутствующей ХВН, что демонстрируют два клинических наблюдения.
Пациент К. (71 год), диагноз «буллезно-геморрагическая рожа правой нижней конечности, II степени тяжести, 2-й поздний рецидив, сопутствующая хроническая лимфовенозная недостаточность». Уровень протеина С при исследовании: 37,6% на 3-й, 39,9% на 4-й, 61,7% на 9-й, 85,8% на 15-й, 93,4% на 19-й день болезни. Даже после выписки, в катамнезе через 5 месяцев, уровень С-протеина оставался ниже уровня здоровых лиц — 82,1%. Status localis при поступлении представлен на рис. 2, status localis в динамике выздоровления — на рис. 3.
Аналогичный по тяжести клинический случай рожи (но без признаков ХВН) демонстрирует более благоприятное течение болезни в сочетании с восстановлением уровня протеина С на 11-й день болезни.
Пациент К. (40 лет), диагноз «эритематозно-геморрагическая рожа левой нижней конечности, II степени тяжести, повторная». Уровень протеина С: 74,5% на 2-й, 74,5% на 3-й, 119,7% на 11-й, 130,2% на 12-й день болезни. Клинические признаки лимфовенозной недостаточности отсутствуют (рис. 4–5).
Восстановление протеина С до нормы наблюдалось на третьей неделе болезни при роже лица (108,2 ± 5,1% при поступлении и 144 ± 4,6% при выписке; 1/4 точка — р < 0,001); на 4-й неделе болезни — при роже нижних конечностей без ХВН (99,8 ± 4,7% при поступлении и 140 ± 4,4% при выписке, 1/4 точка — р < 0,001) и отсутствовало у пациентов с рожей нижних конечностей и ХВН (69,8 ± 8,1% при поступлении, 79,15 ± 4,07% при выписке; 1/4 точка — р = 0,21) (рис. 6).
Проведенное исследование позволило доказать, что при нормальных значениях протеина С (100,0 ± 5,0%) шансы благоприятного течения рожи нижних конечностей достоверно выше (ОШ = 2,89, [0,15; 55]), чем при роже нижних конечностей с хронической венозной недостаточностью и низким уровнем протеина С.
Обсуждение и заключение
Как показали проведенные нами ранее исследования [20, 21], рожа сопровождается развитием скрытого внутрисосудистого гемолиза и ДВС-подобного синдрома. Исследование протеина С дополнило общую картину изменений системы гемостаза при роже, выявив дефицит одного из важнейших естественных антикоагулянтов.
Уровень протеина С при поступлении в группе больных рожей нижних конечностей был ниже, чем в группе больных рожей лица, и ниже значений, полученных в группе здоровых лиц. В периоде реконвалесценции активность эндотелий-зависимого антикоагулянта восстанавливалась у больных рожей лица и рожей нижних конечностей, за исключением пациентов с наличием хронической венозной недостаточности.
Было установлено, что уровень протеина С отличается рефрактерностью к стандартной терапии рожи у таких больных, а документально подтвержденный дефицит протеина С сопровождается затягиванием периода реконвалесценции и удлинением сроков стационарного лечения больных рожей нижних конечностей с признаками ХВН. Значения протеина С только у 7 из 8 больных с ХВН возвращались к норме через 5 месяцев после перенесенной рожи.
Отсутствие положительной динамики протеина С в процессе лечения рожи и затяжной период реконвалесценции у больных рожей нижних конечностей с сопутствующей ХВН требуют пересмотра существующей тактики лечебных мероприятий. Документально подтвержденный дефицит протеина С может служить показанием для проведения заместительной терапии, начинать которую целесообразно в остром периоде болезни [12, 13]. Согласно литературным данным эффективность заместительной терапии зависит от уровня снижения протеина С (не ниже 50–60% от нормы) [18, 19, 26].
Возмещение документированного дефицита протеина С при роже может быть перспективным направлением терапии, направленной на лечение хронической венозной недостаточности и уменьшение системного воспалительного ответа.
Литература
- Фазылов В. Х. Состояние сосудисто-тромбоцитарного гемостаза и коррекция его нарушений при роже. Автореф. дис. … к.м.н. Л., 1990.
- Фролов В. М. Клиника и патогенетические механизмы рецидивирующей рожи. Автореф. дис. … к.м.н. Киев, 1986.
- Храмцов М. М. Патогенетическая и прогностическая роль факторов межклеточных взаимоотношений при рожистом воспалении. Автореф. дис. … д.м.н. М., 2000.
- Еровиченков А. А. Клинико-патогенетическое значение нарушений гемостаза и их коррекция у больных геморрагической рожей. Автореф. дис. д.м.н. М., 2003.
- Черкасов В. Л. Патогенез и лечение различных клинических форм рожи и бициллинопрофилактика ее рецидивов. Автореф. дис. … д.м.н. М., 1977.
- Denis F., Martin C., Ploy M. C. Erysipelas: microbiological and pathogenic data // Annales de Dermatologie et de Venereologie. 2001, v. 128; № 3, C2; 317–326.
- Фазылов В. Х. Нарушение гемостаза и иммунитета при формировании рецидивов рожи, их терапевтическая коррекция. Автореф. дис. … д.м.н. СПб, 1996.
- Митрофанова М. Ю. Нарушения гемостаза и функции эндотелия сосудов у больных рожей. Автореф. дис. к.м.н. М., 2010.
- Дубовикова Т. А. Нитроксидергический профиль и состояние свертывающей системы крови при геморрагических формах рожи. Автореф. дис. к.м.н. М., 2012.
- Ратникова Л. И., Дубовикова Т. А. Оценка состояния сосудисто-тромбоцитарного гемостаза у больных геморрагическими формами рожи // Журнал инфектологии. 2012. Т. 4, № 1, 53–57.
- Егорова В. В., Титова М. И., Демидова В. С. Современные методологические аспекты лабораторной диагностики системы протеина С и значение ее исследования в хирургии // Медицинский алфавит. Современная лаборатория. 2013. № 3, 12–17.
- Liaw P. C. Y., Neuennschwander P. F., Smirnov M. D. Mechanisms by wich soluble endothelial cell protein C receptor modulates protein C and activated protein C function // J. Biol. Che. 2000, vol. 275, № 8; 5447–5452.
- Dahlback B. Resistance to activated protein C as risk factor for thrombosis: molecular mechanism, laboratory investigation and clinical managements // Semin in hematol. 1997, 34 (№ 3); 217–234.
- Суханов В. А. Воспалительный коагуляционный ответ как часть синдрома системной воспалительной реакции (SIRS) // Интенсивная терапия. 2006, № 1; 21–23.
- Светухин А. М., Амирасланов Ю. А., Земляной А. Б. и др. Особенности нарушений системы гемокоагуляции и их коррекция у больных с гнойно-некротическими формами синдрома диабетической стопы // Хирургия. 2006. № 10; 30–34.
- Ерин Д. Н. Роль снижения уровня протеинов C, S и антитромбина III при инфекционно-септическом ДВС-синдроме и коррекция их дефицита криосупернатантом. Автореф. дис. к.м.н. Барнаул, 1999.
- Ена Я. М., Платонова Т. Н., Сушко Е. А. и др. Биологическая роль и клиническое значение протеина С // Врачебное дело. 1992. № 6; 20–25.
- Климович Л. Г., Козар Е. Ф., Крайнюченко Т. В. и др. Противовоспалительные и антикоагулянтные эффекты рекомбинантного активированного протеина С в комплексной интенсивной терапии сепсиса у новорожденных и грудных детей после операции на сердце / 3-я Всероссийская конференция Клиническая гемостазиология и гемореология в сердечно-сосудистой хирургии: материалы конференции. 2007. С. 101.
- Бокерия Л. А., Лобачева Г. В., Харькин А. В., Очаковская Е. Ю., Самсонова Н. Н., Климович Л. Г. Первый опыт применения рекомбинантного активированного протеина С в комплексной интенсивной терапии сепсиса у новорожденных и грудных детей после кардиохирургических вмешательств // Детские болезни сердца и сосудов. 2006. № 35. С. 60–64.
- Фокина Е. Г., Рослый И. М. Лабораторная оценка рожистого воспаления // Эпидемиология и инфекционные болезни. Актуальные вопросы. 2014. № 1; 28–32.
- Фокина Е. Г. Некоторые особенности первичной рожи лица в современных условиях // Терапевтический архив. 2014. № 11; 70–77.
- White B., Schmidt M. // Activated protein C inhibits lipopolysacchartde-induced nuclear translocation of NFkB and TNF-alpha production in THP-1 monocytic cell line // Br J Haematol. 2000. V. 110. P. 130–134.
- Esmon C. T., Taylor F. B. Inflammation and coagulation: Linked processes potentialliregulated through a common pathway mediated by protein C // Thromb Haemost. 1991. V. 66. P. 160–165.
- Esmon C. T. Role of coagulation inhibitors in inflammation // Thromb. 2001. V. 86. P. 51–56.
- Coughlin S. R. Protease-activated receptors in vascular biology // Thromb Haemost. 2001. V. 86. P. 298–307.
- Bernard G. R., Vincent J. L. Efficacy and safety of recombinant human activated pritein C for severe sepsis // N Engl J Med. 2001. V. 344. P. 699–709.
Е. Г. Фокина, кандидат медицинских наук
ФБУН ЦНИИЭ Роспотребнадзора, Москва
Контактная информация: e-fokina@yandex.ru
Купить номер с этой статьей в pdf