Гастроэзофагеальная рефлюксная болезнь (ГЭРБ) — хроническое рецидивирующее заболевание, характеризующееся забросами (рефлюксом) в пищевод желудочного или дуоденального содержимого, возникающими вследствие нарушений моторно-эвакуаторной функции эзофагогастродуоденальной зоны с развитием клинических проявлений и/или осложнений. Наиболее характерными симптомами ГЭРБ являются изжога и регургитация, а наиболее распространенным осложнением — рефлюкс-эзофагит.
ГЭРБ является одним из наиболее распространенных заболеваний верхних отделов желудочно-кишечного тракта и по праву считается болезнью XXI века [1]. Клинические проявления и осложнения ГЭРБ снижают качество жизни, а также трудоспособность больных и ставят данное заболевание в ряд социально значимых. Так, изжога, являющаяся наиболее характерным симптомом заболевания, ухудшает качество жизни у 60% европейских респондентов [2]. По результатам российских эпидемиологических исследований, проведенных в Новосибирске, Санкт-Петербурге и Красноярске (1700, 1898 и 508 опрошенных соответственно), отмечено, что изжога имеет место у 46–60% жителей данных городов [2]. В среднем по России распространенность ГЭРБ составляет 13,3%, что незначительно отличается от данных, полученных в европейских странах и США [1]. При несвоевременной диагностике и отсутствии эффективного лечения у значительного числа больных отмечается склонность заболевания к прогрессированию и развитию таких опасных для жизни осложнений, как кровотечения, пищевод Барретта и аденокарцинома пищевода, частота и смертность от которых значительно выросли [3], что делает проблему лечения ГЭРБ актуальной.
Согласно современным представлениям ГЭРБ, с патофизиологической точки зрения, является преимущественно кислотозависимым заболеванием, развивающимся на фоне нарушения двигательной функции верхних отделов пищеварительного тракта [4]. У большинства пациентов ГЭРБ доминантным механизмом формирования симптомов является контакт слизистой оболочки (СО) пищевода с желудочной кислотой и пепсином, что приводит к нарушению защитных барьеров и развитию повреждений [5]. У пациентов с ГЭРБ в большинстве случаев степень тяжести эзофагита коррелирует не только с продолжительностью воздействия кислоты на пищевод, но и с повышением кислотности рефлюктата [6]. Повышенный уровень секреции соляной кислоты, который, по некоторым данным, отмечается у 80–95% пациентов, является одним из существенных факторов риска развития ГЭРБ [7]. Роль кислотно-пептического фактора в развитии ГЭРБ подтверждается и высокой эффективностью антисекреторных препаратов в лечении данной категории больных [4]. Таким образом, одной из приоритетных задач патогенетической терапии ГЭРБ является эффективное подавление желудочной секреции.
Несмотря на ряд проведенных исследований, все еще остается неразрешенным вопрос о механизмах формирования симптомов, связанных с кислотным рефлюксом. Некоторые авторы полагают, что за их развитие ответственна измененная чувствительность хеморецепторов пищевода в результате действия на них кислоты или медиаторов воспаления [8]. Анализ результатов электронно-микроскопических исследований показал, что в СО пищевода под влиянием соляной кислоты отмечается расширение межклеточных пространств, что позволяет ионам водорода достигать чувствительных нервных окончаний [9]. Укорочение времени экспозиции соляной кислоты в пищеводе способно нормализовать структуру и снизить чувствительность СО к факторам агрессии. Вместе с тем установлено, что не более 5% всех эпизодов кислотных рефлюксов вызывают появление симптомов как у пациентов с эзофагитом, так и при эндоскопически негативной ГЭРБ [10].
Наряду с соляной кислотой существенную роль в генезе развития клинических проявлений ГЭРБ играет ряд других некислотных факторов. Отмечено, что наиболее частым триггером симптомов ГЭРБ является пища, особенно повышенной жирности [11]. Известно, что инфузия жира в просвет двенадцатиперстной кишки больным ГЭРБ существенно сокращает латентный период до появления изжоги и увеличивает ее интенсивность, что может быть связано с вовлечением в механизмы формирования клинических проявлений эффектов холецистокинина или других кишечных нейротрансмиттеров. Кроме того, причинами появления симптомов могут быть воздействие на пищевод объема рефлюктата (жидкого или газообразного) и расстройства перистальтики пищевода. Так, растяжение пищевода воздушным баллоном индуцировало появление изжоги у значительного числа здоровых добровольцев и больных ГЭРБ [8]. Помимо этого, по данным высокочастотной внутрипросветной ультрасонографии выявлена существенная корреляция между эпизодами изжоги и патологически длительными сокращениями продольной мускулатуры пищевода. Желчные рефлюксы могут быть другой возможной причиной симптомов изжоги, а сочетание желчных с кислотными рефлюксами существенно коррелирует с выраженностью ГЭРБ [12]. Определенную роль в восприятии внутрипищеводных стимулов играют психологические факторы. Так, психологическая коморбидность (беспокойство, напряжение, депрессия и т. д.) может вносить свой вклад в модулирование восприятия импульсов из пищевода, когда пищеводные физиологические стимулы низкой интенсивности воспринимаются как болезненные.
Большое число исследований, посвященных вопросам ведения ГЭРБ, свидетельствуют о том, что лечение данной патологии все еще остается не до конца разрешенной и сложной проблемой. Наряду с диетическими рекомендациями, изменением образа жизни (отказ от курения, снижение массы тела, подъем головного конца кровати и т. д.) антациды и алгинаты могут быть успешно использованы пациентами в целях самопомощи для купирования слабо выраженных клинических проявлений ГЭРБ. Вместе с тем в итоговом соглашении конференции по ГЭРБ в Генвале (1999) отмечается, что меры по изменению образа жизни и прием антацидов являются малоэффективными и не могут быть рекомендованы в качестве начальной терапии данной категории больных [5].
Общепризнано, что купирование симптомов ГЭРБ и разрешение рефлюкс-эзофагита (РЭ) прямо коррелирует с продолжительностью и скоростью блокирования желудочной секреции, которая является важным фактором агрессии для СО пищевода [6]. Эффективный контроль внутрижелудочного, а следовательно, и внутрипищеводного уровня рН принципиально важен для быстрого и длительного купирования симптомов ГЭРБ, а также репарации повреждений СО пищевода, независимо от степени тяжести эзофагита.
Установлено, что при 6–8-недельном курсе лечения стандартными дозами ранитидина купирование симптомов ГЭРБ и уменьшение воспалительных изменений СО пищевода отмечалось в 48–88% случаев, однако при наличии эрозий и язв СО пищевода — лишь в 27–45% случаев [6]. Также выявлено, что поддерживающая терапия стандартными дозами антагонистов Н2-рецепторов гистамина не предотвращает рецидивов заболевания. Это может быть обусловлено целым рядом причин. Так, недостаточное блокирование постпрандиальной желудочной кислотности антагонистами Н
В итоговом соглашении по ГЭРБ в Генвале указано, что ингибиторы протонной помпы (ИПП) являются оптимальным вариантом лечения ГЭРБ даже на ранней стадии, поскольку обладают наибольшей эффективностью, которая выражается в быстром достижении желаемых результатов при наименьшей общей стоимости лечения [5].
Метаанализ 43 исследований, проводившихся у пациентов с умеренным и тяжелым эзофагитом, подтвердил преимущество ИПП в сравнении с антагонистами Н2-рецепторов гистамина [14]. Так, имеются данные, что антисекреторная активность ИПП не лимитируется приемами пищи, несмотря на снижение абсорбции. Кроме того, в отличие от антагонистов Н2-рецепторов гистамина, ИПП блокируют конечный этап секреции соляной кислоты, не зависящий от природы стимуляции — вагусной, гистаминовой или гастриновой. Известно, что ИПП подавляют секрецию соляной кислоты селективно и не конкурентно, необратимо инактивируя молекулы Н+/К+ АТФазы париетальных клеток. Активация секреции соляной кислоты обеспечивается за счет морфологических изменений париетальной клетки: заранее синтезированные и хранящиеся в цитоплазме клетки везикулы с расположенными в их мембране молекулами протонной помпы в ответ на функциональную стимуляцию встраиваются в апикальную мембрану клетки, увеличивая ее поверхность. В период стимуляции секреции на апикальной поверхности париетальных клеток образуется большое количество направленных внутрь клетки инвагинаций, называемых секреторными канальцами. Формирование секреторных канальцев в десятки раз увеличивает поверхность, через которую осуществляется секреция соляной кислоты. Концентрирующиеся в секреторных канальцах париетальных клеток молекулы ИПП активируются под действием секретируемой соляной кислоты и, ковалентно связываясь с SH-группами Н+/К+ АТФазы, необратимо ингибируют этот фермент. При этом скорость активации молекул ИПП, а следовательно, и выраженность их антисекреторного эффекта тем выше, чем ниже рН среды в секреторных канальцах, т. е. чем выше уровень секреции соляной кислоты париетальной клеткой. ИПП могут блокировать молекулы Н+/К+ АТФазы, только встроенные в апикальную поверхность клеточных мембран, в то время как внутриклеточные не ингибируются. Таким образом, существование огромного пула не активированных молекул Н+/К+ АТФазы в париетальных клетках может быть ответственно за снижение выраженности и продолжительности антисекреторного эффекта ИПП. Оптимальный антисекреторный эффект может достигаться при предварительной максимальной активации протонных помп с помощью пищевой стимуляции. Преобладание у больных ГЭРБ дневных постпрандиальных кислотных рефлюксов ставит первоочередной задачей блокировать кислотную продукцию преимущественно в дневные часы, что наиболее эффективно достигается при использовании ИПП [6].
В России представители первого поколения ИПП (омепразолы) под различными торговыми названиями используются с начала 1990-х гг. Наиболее назначаемым в нашей стране ИПП стал препарат Омез (омепразол). Данный генерик за долгие годы подтвердил свою высокую эффективность при лечении кислотозависимых заболеваний. Одним из положительных свойств Омеза является сочетание высокого качества препарата, производимого по международным стандартам GMP (Good Manufacturing Practice), и доступность широким слоям населения. При лечении рефлюкс-эзофагита Омез назначается 20 мг 2 раза в день, что позволяет более эффективно тормозить кислотообразование в течение суток. Продолжительность курса лечения, а также последующая суточная доза препарата зависит от степени выраженности рефлюкс-эзофагита и составляет от 20 до 40 мг/сутки на протяжении 6–8 недель.
Независимо от выбора первоначальной терапии, ГЭРБ с эзофагитом или без него может рецидивировать при отсутствии эффективного контроля рН пищевода. Приблизительно у 60–90% пациентов с рефлюкс-эзофагитом при эндоскопическом исследовании отмечается рецидив болезни в течение 6 месяцев после достижения ремиссии заболевания [15]. Следовательно, большинство пациентов с ГЭРБ нуждается в долгосрочном поддерживающем лечении. В итоговом соглашении конференции в Генвале [5] рекомендуется вслед за первоначальной терапией максимально снижать дозировку препаратов до уровня, при котором возможен контроль симптомов. Ряд исследований продемонстрировал хорошие результаты в купировании симптомов и улучшении качества жизни больных при поддерживающей терапии, предусматривающей прием 20 мг омепразола в день «по требованию». Однако в 15–20% случаях для получения положительного эффекта необходимо увеличение дозировок ИПП [16].
Вместе с тем использование для лечения ГЭРБ ИПП в виде монотерапии не всегда устраняет симптомы заболевания, что может быть обусловлено наличием некислотных механизмов развития клинических проявлений заболевания. У ряда больных ГЭРБ рефлюкс возникает вследствие замедления моторики верхних отделов желудочно-кишечного тракта (и особенно желудка), что также сопровождается появлением симптомов функциональной диспепсии (чувство раннего насыщения, тяжести и переполнения в эпигастрии после приема пищи, тошнота и др.). Для разрешения постпрандиального дистресс-синдрома используются прокинетики (метоклопрамид, домперидон, итоприд), которые одновременно повышают и клиренсную функцию пищевода, и тонус нижнего пищеводного сфинктера. Проведенные исследования подтвердили, что сочетанное использование прокинетиков и препаратов с антисекреторным действием существенно повышают эффективность терапии больных ГЭРБ с наличием симптомов функциональной диспепсии. С учетом результатов данных исследований был разработан новый комбинированный препарат Омез Д, в одной капсуле которого содержатся два действующих вещества — 10 мг омепразола и 10 мг домперидона. Данное сочетание позволяет осуществлять двунаправленное кислотосупрессивное и прокинетическое действие препарата, что значительно повышает эффективность лечения и комплаентность пациентов. Омез Д может назначаться по 1 капсуле 2 раза день в течение 2–4 недель больным ГЭРБ с наличием симптомов функциональной диспепсии в период поддерживающей терапии заболевания.
Существенное значение в лечении ГЭРБ имеет скорость наступления антисекреторного эффекта при приеме кислотодепрессивных препаратов, которая прямо коррелирует с качеством жизни и скоростью репарации структурных изменений СО пищевода у данной категории больных. До настоящего времени все оральные ИПП (омепразол, лансопразол, пантопразол, эзомепразол и рабепразол) были в лекарственной форме с отсроченным высвобождением, в которых активные субстанции для защиты от деградации в кислой среде желудка покрыты кишечно-растворимыми оболочками, что приводит к замедлению абсорбции действующего вещества и следующего за ней подавления секреции соляной кислоты. Омепразол немедленного высвобождения Зегерид (в РФ препарат в настоящее время не зарегистрирован), одобренный для применения в США, является первым поступившим в продажу препаратом группы ИПП в оральной лекарственной форме с немедленным высвобождением и состоит из омепразола в свободном виде и бикарбоната натрия.
В настоящий момент единственным ИПП с немедленным высвобождением, одобренным для применения в России, является препарат Омез Инста. Принимаемый в виде оральной суспензии он обладает исключительными свойствами с точки зрения фармакокинетики и фармакодинамики. Омепразол немедленного высвобождения, входящий в состав препарата Омез Инста, отличается от ИПП отсроченного высвобождения тем, что он не имеет энтеросолюбильного покрытия, а для защиты активного вещества от деградации в кислой среде желудка применяется бикарбонат натрия. Бикарбонат натрия, вызывая подъем уровня внутрижелудочного рН, оказывает протективное действие на не покрытый кишечно-растворимой оболочкой омепразол, который быстро эвакуируется и всасывается в тонкой кишке. Кроме того, быстрая нейтрализация соляной кислоты желудка бикарбонатом натрия приводит к выбросу гастрина, активирующего протонные помпы париетальных клеток желудка. Последнее способствует блокированию омепразолом максимального числа активированных протонных помп и, следовательно, поддержанию продолжительного и стабильного кислотодепрессивного эффекта. Результаты исследований по применению омепразола немедленного высвобождения у пациентов с ночными симптомами ГЭРБ и ночными «кислотными прорывами» подтверждают его высокую эффективность при данной патологии, что, по-видимому, связано с описанными выше особенностями действия бикарбоната натрия на гастриновые механизмы стимуляции желудочной секреции [17].
Нами было проведено открытое сравнительное исследование скорости наступления антисекреторного эффекта при однократном приеме ИПП с отсроченным и немедленным высвобождением с использованием длительного мониторирования интрагастрального и интрапищеводного уровня рН. В настоящее исследование было включено 27 амбулаторных пациентов с клиническими симптомами ГЭРБ и различной степенью выраженности (A-C по Лос-Анджелесской классификации) рефлюкс-эзофагита по результатам эндоскопического исследования. Пациенты не получали антисекреторные препараты в течение 30 дней до проведения рН-метрии. Фармакологическая проба проводилась в первой половине дня (до 14 часов) и включала в себя однократный прием ИПП с отсроченным (омепразол 20 мг, пантопразол 40 мг, эзомепразол 20 мг, рабепразол 20 мг) и немедленным (Омез Инста 20 мг) высвобождением. У всех больных изучались базальный интрагастральный уровень рН (средний рН за первый час измерений утром, натощак) и латентный период препарата (интервал времени от момента приема препарата до подъема интрагастрального уровня рН до 4).
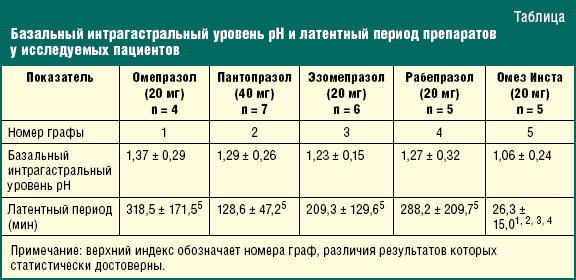
Результаты исследования, представленные в таблице, показали, что повышение базальной интрагастральной кислотности выявлялось у большинства пациентов в исследуемых группах, подтверждая ведущую роль гиперпродукции соляной кислоты в патогенезе ГЭРБ [6]. При этом базальный интрагастральный уровень рН в исследуемых группах пациентов не имел значимых различий.
Латентный период препарата в группе пациентов, принимавших Омез Инста, составил 26,3 ± 15,0 мин (от 2 до 40 мин) и был значительно короче, чем у пациентов других групп (рис.). Окончание кислотодепрессивного действия препарата в группе пациентов, принимавших Омез Инста, в течение трехчасового мониторирования интрагастрального уровня рН не отмечалось.
Примечательно, что у трех пациентов из группы, получавших Омез Инста, с наличием до начала исследования клинических симптомов (боли в эпигастрии, изжога, тошнота), последние быстро купировались во время проведения фармакологической пробы.
Таким образом, ИПП с немедленным высвобождением Омез Инста выгодно отличается по скорости наступления кислотодепрессивного действия от ИПП с отсроченным высвобождением. Данное уникальное свойство Омез Инста способствует быстрому купированию симптомов ГЭРБ, что позволяет рекомендовать данный препарат для использования в ступенчатой терапии ГЭРБ. Последняя предусматривает назначение с 1-го по 5-й день лечения ИПП с немедленным высвобождением — Омез Инста по 20 мг 2 раза в сутки с интервалом в 12 часов и с 6 дня — прием ИПП с отсроченным высвобождением — Омез по 20–40 мг в сутки на протяжении 6–8 недель, в зависимости от степени выраженности рефлюкс-эзофагита.
Препарат целесообразно использовать также в режиме «по требованию» в качестве «скорой помощи» пациентам при поддерживающей терапии заболевания. Такой подход предотвращает необходимость повторных курсов лечения комбинациями препаратов и позволяет пациенту самостоятельно контролировать свои симптомы, что может привести к улучшению качества жизни и уменьшению использования медицинских ресурсов.
Литература
- Маев И. В., Вьючнова Е. С., Щекина М. И. Гастроэзофагеальная рефлюксная болезнь — болезнь XXI века // Лечащий Врач. 2004; 4: 10–14.
- Лазебник Л. Б., Машарова А. А., Бордин Д. С. и др. Результаты многоцентрового исследования «Эпидемиология гастроэзофагеальной рефлюксной болезни в России» (МЭГРЕ) // Тер. Архив. 2011; 1: 45–50.
- Falk G. W., Richter J. E. Gastroesophageal Reflux Disease and Barrett’s Esophagus // Endoscopy. 1998; 30: 61–72.
- Ивашкин В. Т., Трухманов А. С. Болезни пищевода. М.: Триада, 2000.
- Dent J., Brun J., Fendrick A. M. et al. An evidence-based appraisal of reflux disease management the Genval Workshop Report // Gut. 1998; 44: 1–6.
- Bell N. J. V., Burget D., Howden C. W. et al. Appropriate acid suppression for the management of gastroesophageal reflux disease // Digestion. 1992; 51: 59–67.
- Van Herwaarden M. A., Samsom M., Smout A. J. P. M. Excess Gastroesophageal Reflux in Patients With Hiatal Hernia is Caused by Mechanisms Other Than Transient LES Relaxation // Gastroenterology. 2000; 119: 1439–1446.
- Fass R., Naliboff B., Higa L. et al. Differential effect of long-term esophageal acid exposure on mechanosensitivity and chemosensitivity in humans // Gastroenterology. 1998; 115: 1363–1373.
- Hopwood D., Milne G., Logan K. R. Electron microscopic changes in human oesophageal epithelium in oesophagitis // J. Pathol. 1979; 129: 161.
- Fass R., Tougas G. Functional heartburn — the stimulus, the pain and the brain // Gut. 2002; 51: 885–892.
- Robertson D. A. F., Aldersley M. A., Shepherd H. et al. Patterns of acid reflux in complicated oesophagitis // Gut. 1987; 28: 1484–1488.
- Vaezi M. F., Richter J. E. Role of acid and duodenogastroesophageal reflux in gastroesophageal reflux disease // Gastroenterology. 1996; 111 (5): 1192–1199.
- Wilder-Smith C. H., Merki H. S. Tolerance during dosing with H2-receptor antagonists // Scand. J. Gastroenterol. 1992; 27: 14–19.
- Chiba N., De Cara C. J., Wilkinson J. M., Hunt R. H. Speed of healing and symptom relief in grade II to IV gastro-oesophageal reflux disease: a meta-analysis // Gastroenterology.1997; 112: 1798–1810.
- Sontag S. J. Rolling review: gastro-oesophageal reflux disease // Aliment. Pharmacol. Ther. 1993; 7: 293–312.
- Carlsson R., Dent J., Watts R. et al. Gastro-oesophageal reflux disease in primary care: an international study of different treatment strategies with omeprazole // Eur. J. Gastroenterol. Hepatol. 1998; 10: 119–124.
- Castell D. Review of immediate-release omeprazole for the treatment of gastric acidrelated disorders // Expert Opin. Pharmacother. 2005; 6 (4): 2501–2510.
А. Н. Иванов*, кандидат медицинских наук, доцент
А. В. Яковенко*, кандидат медицинских наук, доцент
Н. А. Агафонова*, кандидат медицинских наук, доцент
А. С. Прянишникова*, кандидат медицинских наук, доцент
Л. П. Краснолобова**
О. И. Костюкович**
С. В. Белякова***
*ГБОУ ВПО РНИМУ им. Н. И. Пирогова Минздравсоцразвития России,
**ДКЦ № 1, Москва
***МУЗ ГП, Орехово-Зуево
Контактная информация об авторах для переписки: kafgastro@mail.ru
Купить номер с этой статьей в pdf