Пыльцевая аллергия по данным исследователей отмечается у 3,0–40% населения земного шара и является одним из самых распространенных аллергических заболеваний [1–3].
В Саратовской области при популяционном исследовании с помощью стандартизированных вопросников (ECRHS) распространенность симптомов пыльцевого аллергического ринита составила 28,3%, у 40–80% лиц с симптомами ринита одновременно присутствовали симптомы конъюнктивита [3, 4].
Пыльцевой аллергический риноконъюнктивит в Саратовской области характеризуется целым рядом особенностей, связанных с климато-географическими условиями, видовым составом растений, календарем их цветения, аллергенностью пыльцы. Причинами аллергического риноконъюнктивита в регионе является преимущественно пыльца сорных трав: маревых, конопли, циклахены [4], которые присутствуют в воздухе в высокой концентрации в т��чение длительного периода (более трех месяцев) и приводят к появлению тяжелых персистирующих форм заболевания с вовлечением различных органов и систем, требующих одновременного использования многих препаратов. Для уменьшения лекарственной нагрузки необходим подбор препаратов, подавляющих аллергическое воспаление на слизистой носа и конъюнктив. Эффективными средствами как для предупреждения, так и для облегчения симптомов, обусловленных ранней и поздней фазами аллергического ответа при аллергическом рините, зарекомендовали себя интраназальные кортикостероиды (ИНГКС) [1–3].
Большинство исследований ИНГКС, проводившихся в последние десятилетия, были сосредоточены в основном на эффективности купирования носовых симптомов аллергического ринита (АР), а глазные симптомы упоминались либо как вторичная конечная точка, либо чаще совсем не оценивались. С появлением нового класса препаратов (например, флутиказона фуроата, оказывающего существенное влияние на глазные симптомы) [5] возобновился интерес к исследованию влияния «старых» ИНГКС в отношении подобного феномена при риноконъюнктивитах.
Целью настоящего исследования была оценка влияния флутиказона пропионата (Фликсоназе®) на глазные симптомы у больных с персистирующими пыльцевыми риноконъюнктивитами среднетяжелого/тяжелого течения.
Дизайн исследования
Рандомизированное, двойное слепое плацебо-контролируемое исследование в параллельных группах.
Монотерапия с применением препарата Фликсоназе® исследовалась в контексте облегчения назальных и глазных симптомов у пациентов с аллергическим риноконъюнктивитом. Эффективность монотерапии препаратом Фликсоназе®, применяемого 2 раза в сутки, сравнивали с комбинированной терапией (интраназальный ГКС в сочетании с глазными каплями топического антигистамина азеластина). Комбинированная терапия рассматривалась как стандартный подход к лечению сочетанных риноконъюнктивальных симптомов, поскольку топический блокатор гистаминовых H
Критерии включения: пациенты в возрасте ≥ 18 лет с клиническими симптомами аллергического риноконъюнктивита с документированным анамнезом сезонного заболевания (сезонное наступление и прекращение симптомов в течение каждого из двух последних сезонов цветения трав) и положительными результатами кожных проб на аллергены пыльцы.
Критерии исключения: пациенты с физической травмой или анатомической обструкцией носовой полости, пациенты с астмой, медикаментозным ринитом, хроническими заболеваниями, которые могли помешать проведению исследования.
Исключаемые медикаменты: интраназальные кортикостероиды за 4 недели до первого посещения или любые иные кортикостероиды за 8 недель до первого посещения; любые иные медикаменты, которые могут оказать воздействие на симптомы сезонного аллергического ринита или эффективность исследуемого лекарственного средства.
Пациенты по группам распределялись в отношении 4:1 (4 пациента с азеластином/1 пациент с плацебо) по таблице случайных чисел. Продолжительность лечебного периода составила 56 дней (8 недель).
Первая группа получала для лечения флутиказона пропионат (назальный спрей 50 мкг в одной дозе, режим дозирования — по 1 дозе в каждый носовой ход 2 раза в день) в сочетании с глазными каплями топического антигистаминного препарата азеластина 0,05% водный раствор (Аллергодил®) по 1 капле в каждый глаз 3–4 раза в день. Вторая группа пациентов получала флутиказона пропионат в сочетании с плацебо (в виде глазных капель, составленных идентично азеластину, но без активной субстанции, режим дозирования такой же, как и в группе азеластина).
Эффективность фармакотерапии оценивалась по динамике глазных и назальных симптомов заболевания в обеих группах. Динамику клинических симптомов оценивали по дневникам самонаблюдения для определения степени тяжести аллергической симптоматики, которые пациенты вели на протяжении всего курса лечения, оценки шкалы тяжести симптомов исходно (0-й день), а также на 3-й, 14-й, 35-й и 56-й день от начала лечения. В индивидуальных регистрационных картах регистрировались выраженность основных и вторичных глазных симптомов, а также назальных симптомов; обязательной была регистрация о нежелательных явлениях (наблюдение за основными показателями состояния организма, контроль электрокардиограммы и клинические лабораторные пробы) и потребности в дополнительных препаратах.
Характеристика больных, включенных в исследование
В исследование было рандомизировано 68 больных аллергическим риноконъюнктивитом (АРК), в возрасте от 18 до 64 лет, находящихся на диспансерном учете в аллергологическом центре Саратовского государственного университета им. В. И. Разумовского. Среди обследованных пациентов 25 человек (36,76%) — лица мужского и 43 (63,24%) — женского пола. Средний возраст (М ± s) для всей группы — 35,44 ± 11,68 года, средний возраст мужчин — 32,92 ± 12,59, женщин — 36,91 ± 11,0 лет. Длительность заболевания АРК для всей группы составила — 10,04 ± 5,25 года, для мужчин — 10,0 ± 4,95 года, для женщин — 10,06 ± 5,47 года.
В группу получающих комбинацию флутиказона пропионата и азеластина рандомизировано 49 пациентов. Досрочно прекратили свое участие в исследовании шесть пациентов, из них два — вследствие недостаточного эффекта от проводимой терапии, два — в результате проявления побочных эффектов от приема глазных капель (жжение глаз), один пациент выбыл из исследуемой группы по причине возникновения острого интеркуррентного заболевания (ОРВИ) и один прекратил участие по личным причинам (деловая поездка).
В группу, получающую флутиказона пропионат и плацебо (монотерапия ИНГКС), вошли 19 пациентов, один из которых вынужден был прекратить терапию из-за недостаточного эффекта.
Таким образом, лечебный период до конца прошли 43 пациента из группы «флутиказона пропионат + азеластин» и 18 пациентов из группы «флутиказона пропионат + плацебо».
В исходной точке демографические и клинические характеристики в обеих группах были сходными.
Критериями эффективности лечения были изменения интенсивности регистрируемых на визитах глазных и назальных симптомов заболевания.
Материалы и методы
Стандартная процедура аллергологического обследования включала сбор семейного и индивидуального аллергологического анамнеза (наследственная отягощенность по аллергическим заболеваниям, аллергические реакции на профилактические прививки, лекарственные препараты), данные комплексного клинического обследования (сопутствующие аллергические заболевания), кожные аллергические пробы.
Для специфической диагностики использовали скарификационные кожные тесты со стандартизованными аллергенами пыльцы. Использовались отечественные пыльцевые аллергены (деревья, злаковые, сорные травы). Результаты кожной пробы оценивали на пике реакции на основании измерения диаметра волдыря и эритемы через 20 минут после начала теста.
На каждом визите пациенты заполняли бланк контроля, где регистрировались назальные и глазные (основные и вторичные) и симптомы. Каждый из симптомов оценивали по принятой шкале от 0 до 3 баллов на каждый из перечисленных признаков:
- 0 баллов — отсутствие симптомов;
- 1 балл — легкие симптомы, явно чувствуемые, но легко переносимые;
- 2 балла — умеренно выраженные симптомы — обращают на себя внимание, влияют на дневную активность;
- 3 балла — выраженные симптомы — тяжело переносятся, препятствуют дневной активности.
Из назальных симптомов оценивались зуд в носу, чихание, ринорея, заложенность. Общий показатель тяжести назальных симптомов состоял из суммы отдельных показателей по этим четырем симптомам.
Основные глазные симптомы включали зуд глаз, слезотечение, покраснение конъюнктивы. В исследование вошли только пациенты, у которых сумма оценки основных глазных симптомов составляла не менее 6 баллов.
Вторичные глазные симптомы включали жжение глаз, светобоязнь, отек век, выделение/склеивание век, чувство инородного тела в глазах.
В день 0 симптомы оценивались до начала противоаллергической терапии, все последующие визиты оценка глазной и назальной симптоматики производилась на фоне получаемой терапии.
Результаты и обсуждение
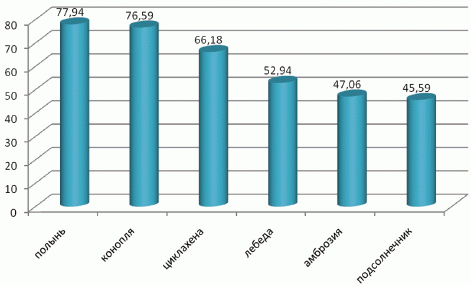
Среди участников исследования «intent-to-treat» все пациенты были с персистирующим течением АРК, обусловленным сенсибилизацией к пыльце сорных трав (100% обследуемых). Наибольшее число пациентов с аллергией на сорные травы имели сенсибилизацию к пыльце полыни (77,94%), конопли (76,59%), циклахены (66,18%), лебеды (52,94%), далее следует сенсибилизация к пыльце амброзии и подсолнечника (рис. 1).
Кроме того, у части пациентов отмечалась сенсибилизация к другим группам аллергенов (у 11,76% к пыльце деревьев, у 23,52% — к пыльце злаковых трав) (рис. 2).
До начала лечения среднее значение (М ± s) в баллах назальных (зуд в носу, чихание, ринорея, заложенность), основных глазных (зуда глаз, слезотечения и покраснения конъюнктивы) и вторичных глазных (жжение глаз, светобоязнь, отек век, выделение/склеивание век, чувство инородного тела) симптомов в первой группе («флутиказона пропионат + азеластин») и второй группе («флутиказона пропионат + плацебо») было практически одинаковым (рис. 3).
| |
| Рис. 2. Распределение больных, сенсибилизированных к пыльце других растений (%) |
| |
| Рис. 3. Оценка основных глазных (по порядку — зуд, слезотечение, покраснение), вторичных глазных (по порядку — жжение глаз, светобоязнь, отек век, выделение/склеивание век, чувство инородного тела в глазах) и назальных (зуд в носу, чихание, ринорея, заложенность) симптомов в группах 1 («флутиказона пропионат + азеластин» — интенсивно голубой столбик) и 2 («флутиказона пропионат + плацебо» — светло-голубой столбик) Реклама |
Влияние на назальные симптомы
Среднее балльное значение (М ± s) назальных симптомов (зуд носа, чихание, ринорея, заложенность) до начала изучаемой терапии в первой группе («флутиказона пропионат + азеластин») составляло 2,49 ± 0,59, 2,23 ± 0,81, 2,23 ± 0,75 и 2,3 ± 0,71 балла соответственно. В группе 2, получающей флутиказона пропионат + плацебо, оценка назальных симптомов была идентичной: 2,67 ± 0,49, 2,67 ± 0,49, 2,56 ± 0,62 и 2,11 ± 0,68 (рис. 3). Различия между группами до начала терапии статистически незначимы (р > 0,05).
Оба варианта противоаллергической терапии приводят к выраженному снижению тяжести таких назальных симптомов, как зуд носа, чихание, ринорея, заложенность носа. Динамика изменений тяжести назальных симптомов в первой и второй группах представлена на рис. 4.
| |
| Рис. 4. Динамика градиента падения среднего значения назальных симптомов (в баллах от исходного уровня к 3-му, 14-му, 35-му, 56-му дню лечения) в первой («флутиказона пропионат + азеластин») и второй («флутиказона пропионат + плацебо») группах Реклама |
Как видно из графических данных, монотерапия флутиказона пропионатом не уступает по своей эффективности комбинированному использованию флутиказона пропионата с азеластином в отношении такого симптома, как зуд (нет различий между двумя группами), при том и другом режиме терапии на 3-й, 14-й, 35-й, 56-й день лечения достоверно уменьшается тяжесть назальной симптоматики по сравнению с исходным уровнем. Для чихания и ринореи был получен более выраженный ответ на монотерапию флутиказона пропионатом («флутиказона пропионат + плацебо»), чем на комбинацию «флутиказона пропионат + азеластин». Среднее относительное изменение заложенности в ходе терапии «флутиказона пропионат + азеластин» было значительно больше при приеме препарата флутиказона пропионат + плацебо.
По всей вероятности, в связи с высокой противовоспалительной активностью флутиказона пропионата, его использование в виде монотерапии достаточно для полного подавления назальных симптомов и добавление антигистаминов в виде глазных капель способно повлиять только на компонент заложенности, связанный с избирательной блокадой азеластином гистаминовых H1-рецепторов и уменьшением проницаемости капилляров и экссудации, присущих этому классу препаратов (при проникновении в полость носа через слезно-носовой канал) [6, 7].
Влияние на глазные симптомы
Основные глазные симптомы
До начала лечения в первой группе («флутиказона пропионат + азеластин») среднее значение для основных глазных симптомов (зуд глаз, слезотечение и покраснение конъюнктивы) было соответственно 2,58 ± 0,5, 1,93 ± 0,59 и 2,35 ± 0,48 балла. В группе «флутиказона пропионат + плацебо» среднее значение для основных глазных симптомов составляло 2,44 ± 0,62, 1,94 ± 0,64 и 2,22 ± 0,55 балла (рис. 3). Различия в двух группах до начала терапии являлись статистически незначимыми (p > 0,05).
В ходе лечения отмечено уменьшение балльной оценки глазных симптомов у пациентов, получавших оба режима терапии. Динамика градиента падения среднего значения основных глазных симптомов (в баллах) в исследуемых группах представлена на рис. 5.
| |
| Рис. 5. Динамика градиента падения среднего значения основных глазных симптомов (в баллах от исходного уровня к 3-му, 14-му, 35-му, 56-му дню лечения) в первой («флутиказона пропионат + азеластин») и второй («флутиказона пропионат + плацебо») группах Реклама |
В ходе исследования установлено, что оба режима терапии приводят к достоверному снижению тяжести основных глазных симптомов — зуда глаз, слезотечению, покраснению. На фоне терапии «флутиказона пропионат + азеластин» (первая группа) градиент снижения отчетливый, быстрый и высокодостоверный (Р < 0,001 по сравнению с исходным уровнем). Монотерапия флутиказона пропионатом («флутиказона пропионат + плацебо», вторая группа) приводит к меньшему падению средней балльной оценки по сравнению с первой группой. Тем не менее, значимость влияния терапии флутиказоном пропионатом на основные глазные симптомы не вызывает сомнения (для всех основных симптомов по сравнению с исходным значением, начиная с 3-го дня до 56-го, отмечено снижение тяжести, уменьшение балльной оценки, Р < 0,01 по сравнению с исходным уровнем).
Вторичные глазные симптомы
До начала терапии среднее балльное значение (М ± s) для жжения глаз составляло 0,79 ± 0,86 для первой группы («флутиказона пропионат + азеластин») и 0,83 ± 0,86 балла для второй группы («флутиказона пропионат + плацебо»). Светобоязнь до начала лечения соответственно 1,12 ± 0,88 и 1,39 ± 0,98 балла. Отек и склеивание век, а также чувство инородного тела в глазах в первой группе до начала лечения составляли соответственно 1,88 ± 0,76, 1,39 ± 0,82 и 1,49 ± 0,94 балла, а во второй группе 1,83 ± 0,62, 1,22 ± 0,81 и 1,39 ± 0,85 балла (рис. 3). Различия в группах до начала терапии являлись статистически незначимыми (p > 0,05).
Жжение глаз, светобоязнь, отек и склеивание век, чувство инородного тела в глазах под влиянием терапии в обеих группах существенно уменьшались.
Динамика градиента падения среднего значения вторичных глазных симптомов (в баллах) в исследуемых группах представлена на рис. 6.
| |
| Рис. 6. Динамика градиента падения среднего значения вторичных глазных симптомов (в баллах от исходного уровня к 3-му, 14-му, 35-му, 56-му дню лечения) в?первой («флутиказона пропионат + азеластин») и второй («флутиказона пропионат + плацебо») группах |
В первой группе («флутиказона пропионат + азеластин») отмечено выраженное влияние на все вторичные глазные симптомы: жжение, светобоязнь, отек, склеивание век, чувство инородного тела с первых дней лечения до периода завершения исследования.
Флутиказона пропионат продемонстрировал нестабильную эффективность в отношении вторичных глазных симптомов у пациентов с сезонным аллергическим ринитом. Монотерапия флутиказона пропионатом без топических антигистаминных глазных капель не сопровождалась снижением чувства жжения глаз на протяжении всего периода исследования, отмечалось значительно меньшее падение среднего балла при оценке отека, склеивания век, чувства инородного тела. Различия между обеими группами в контексте влияния на вторичные глазные симптомы были достоверными.
Оба режима терапии продемонстрировали благоприятный профиль безопасности, побочные явления не зарегистрированы.
Таким образом, назальный спрей флутиказона пропионата (Фликсоназе®) редуцирует назальные и основные, но не вторичные глазные симптомы при пыльцевых аллергических риноконъюнктивитах.
Выводы
- Монотерапия флутиказона пропионатом высокоэффективна для купирования главных назальных симптомов пыльцевого персистирующего аллергического риноконъюнктивита (зуд носа, чихание, ринорея, заложенность) в условиях продолжительной поллинации сорных трав.
- При добавлении к терапии флутиказона пропионатом топических антигистаминовых глазных капель азеластина тяжесть назальных симптомов — зуда носа, чихания, ринореи существенно не меняется, но отмечается дополнительный эффект в отношении уменьшения заложенности носа.
- В группе, получавшей монотерапию флутиказона пропионатом, отмечено статистически значимое уменьшение основных глазных симптомов (зуд глаз, слезотечение, покраснение) с 3-го по 56-й день терапии по сравнению с исходным уровнем. При комбинации флутиказона пропионата с топическими антигистаминовыми глазными каплями азеластина эффективность терапии существенно выше в отношении всех основных глазных симптомов. Терапевтическая разница между двумя группами статистически достоверна.
- Монотерапия флутиказона пропионатом уменьшала явления светобоязни, но не влияла на симптомы жжения; отмечена нестабильная эффективность в отношении других вторичных глазных симптомов: склеивание век, чувство инородного тела.
Комбинированная терапия флутиказона пропионатом (назальный спрей) и азеластином (глазные капли) обеспечивает непрерывное облегчение вторичных глазных симптомов у пациентов с аллергическими риноконъюнктивитами.
Литература
- Allergic Rhinitis and its Impact on Asthma (ARIA), 2008 update (in collaboraton with the World Health Organisation, GA2 LEN и AllerGen) // Allergy. 2008; 63 (suppl. 860: 8–160.
- Allergic Rhinitis and its Impact on Asthma (ARIA) guidelines 2010 Revision // J. Allergy Clin Immunol. 2010, September, vol. 126, № 3, 466–476.
- Горячкина Л. А., Астафьева Н. Г., Передкова Е. В. Поллиноз. В кн.: Клиническая аллергология и иммунология: руководство для практикующих врачей. Под ред. Л. А. Горячкиной и К. П. Кашкина. М.: Миклош, 2009. С. 351–362.
- Астафьева Н. Г., Удовиченко Е. Н., Гамова И. В. и др. Пыльцевая аллергия в Саратовской области // РАЖ. 2010, № 1, с. 17–25.
- Астафьева Н. Г. Эффективность нового назального глюкокортикоида Авамис при сезонном аллергическом рините // РАЖ. 2010, № 3, с. 74–84.
- Williams P. B., Crandall E., Sheppard J. D. Azelastine hydrochloride, a dual-acting anti-inflammatory ophthalmic solution, for treatment of allergic conjunctivitis // Clin Ophthalmol. 2010, Sep 7; 4: 993-10-01.
- Kaliner M. A., Storms W., Tilles S. et al. Comparison of olopatadine 0.6% nasal spray versus fluticasone propionate 50 microg in the treatment of seasonal allergic rhinitis // Allergy Asthma Proc. 2009, May-Jun; 30 (3): 255–262.
Н. Г. Астафьева, доктор медицинских наук, профессор
И. А. Перфилова
Д. Ю. Кобзев
Е. Н. Удовиченко, кандидат медицинских наук
И. В. Гамова, кандидат медицинских наук, доцент
СГМУ, Саратов
Контактная информация об авторах для переписки: astang@mail.ru
Купить номер с этой статьей в pdf