Несмотря на очевидные научные достижения и противоэпидемические мероприятия, врачи, эпидемиологи и организаторы здравоохранения вынуждены констатировать, что острые респираторные вирусные инфекции (ОРВИ) и грипп остаются до сих пор плохо контролируемыми инфекциями. Это объясняется полиэтиологичностью возбудителей, отсутствием вакцин (за исключением гриппа) для специфической профилактики, массовостью заболеваний, смешанным характером инфекций, изменчивостью антигенных свойств вирусов и развивающейся резистентностью к препаратам.
Суммарный экономический ущерб от заболеваемости гриппом и ОРВИ в России, по оценке специалистов, составляет в последние годы не менее 40 млрд. рублей ежегодно. С ОРВИ связано 30–50% потерь рабочего времени у взрослых и 60–80% пропусков школьных занятий у детей, до 80% всех случаев острых респираторных заболеваний (ОРЗ) приходится именно на часто болеющих детей. В детских стационарах частота перекрестной инфекции респираторными вирусами может достигать 40–80% [1].
ОРВИ составляют более половины всех острых заболеваний. Наиболее уязвимыми группами риска являются «часто болеющие дети», переносящие в течение года от 6 до 12 эпизодов респираторной заболеваемости и дети с хронической, в частности сердечно-сосудистой, патологией, где высоки частота вторичной иммуносупрессии, рецидивирующей и хронической бронхолегочной и ЛОР-патологии.
Можно констатировать, что, хотя 90–95% инфекций верхних дыхательных путей вызвано вирусами и только 5% — бактериями, в 75% случаев пациентам назначаются антибиотики [2]. При этом данные о целесообразности использования антибиотиков при ОРВИ неоднозначны. Известно, что антибиотики синтетического происхождения против вирусов бесполезны и не рекомендуются [3]. Установлено, что антибактериальная терапия при вирусной инфекции не влияет на длительность заболевания, динамику основных клинических симптомов, выраженность постинфекционного астенического синдрома, состояние здоровья пациента.
Антивирусные препараты являются соединениями природного и/или синтетического происхождения, обладающими этиотропным действием и применяемыми для лечения и/или профилактики вирусных инфекций. Данная группа включает противовирусные химиопрепараты, интерфероны и индукторы интерферона. Противовирусные препараты, применяемые при ОРВИ, можно разделить на две группы: специфического (например, осельтамивир (Тамифлю) для лечения гриппа, паливизумаб (Синагис) для лечения РС-вирусной инфекции) и широкого действия, назначаемые при ОРВИ любой этиологии (препараты рекомбинантного альфа-интерферона, в т. ч. лейкоцитарный назальный интерферон, Реаферон, Виферон; индукторы интерферона, такие как Арбидол, Циклоферон, Неовир, Амиксин).
Орвирем был разработан НИИ гриппа (Санкт-Петербург) совместно с другими организациями РАМН с целью расширения показаний применения римантадина у детей. Он представляет собой полимерный препарат прочного солевого комплекса римантадина с полимерным природным соединением — альгинатом натрия. Присутствие альгината натрия значительно изменило фармакологические свойства римантадина в Орвиреме, по сравнению с обычным римантадином. Входящий в состав препарата низкомолекулярный модифицированный альгинат натрия, выполняя функцию полимерной матрицы, обладает адсорбирующими и дезинтоксикационными свойствами, что способствует его антитоксической активности.
В данной фармакологической форме римантадин высвобождается не сразу, что дает постепенное и продолжительное его поступление в кровь, пролонгированную циркуляцию его в организме, постоянную концентрацию препарата в крови, улучшается фармакокинетика и механизм действия препарата, который в настоящий момент хорошо изучен. Орвирем предназначен для детей от одного года и позиционируется для лечения гриппа А. Однако уже в процессе предрегистрационного изучения (НИИ гриппа, Санкт-Петербург, проф. Дриневский В. П., 2000) была установлена его эффективность и безопасность в терапии и других ОРВИ. Исследования препаратав период 2003–2004 гг. проводили: Институт вирусологии имени Д. И. Ивановского РАМН РФ, Москва; ГУ Всесоюзный научно-исследовательский институт гриппа, Санкт-Петербург; кафедра детских инфекционных болезней РГМУ, Москва.
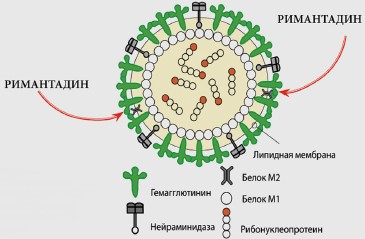
Экспериментальные исследования показали избирательное взаимодействие Орвирема с трансмембранным вирусным белком М2, выполняющим функцию протонного насоса. Препятствуя понижению рН эндосом, препарат блокирует слияние оболочки вируса с мембранами эндосом и предотвращает, таким образом, передачу вирусного генетического материала в цитоплазму клетки. В результате угнетение выхода вирусных частиц из клетки прерывает транскрипцию генома вируса (рис. 1). Подавление репродукции вируса гриппа Орвиремом сопровождается индукцией интерферона, второго уровня защиты, что позволяет усилить химиотерапевтическое действие препарата и предотвратить развитие наиболее тяжелых осложнений гриппа: ларингита и пневмонии [4, 5].
Вышеизложенное объясняет наш интерес к Орвирему и явилось предпосылкой клинического изучения эффективности данного препарата в качестве этиотропного противовирусного и противовоспалительного средства в ДИКБ № 6 УЗ САО г. Москвы (на клинической базе педиатрического факультета РУДН) у детей, госпитализированных по поводу острых респираторных вирусных заболеваний, в том числе у детей с сопутствующими врожденными пороками сердца, госпитализированных в открытое здесь с 2004 года первое в России отделение инфекционной кардиологии. Данная категория пациентов документировано имеет вторичную иммунологическую недостаточность, что способствует персистенции респираторных вирусов, причастных к развитию миокардита, тонзиллогенных заболеваний сердца эндотелиальной дисфункции и других осложнений, включая риск раннего атерогенеза. По современным представлениям, острый бронхиолит, как одна из форм ОРВИ, особенно опасен для детей с врожденными пороками сердца (ВПС), 18% которых умирают от острого бронхиолита [6–9].
Прекращение рецепции и репликации вируса имеет важное значение для профилактики развития «инфекционного сердца», обратимого, транзиторного (не более 2–4 суток), коронарогенного расширения границ сердца с явлениями недостаточности кровообращения, наблюдаемого в активной фазе острых инфекций, чаще при гипертермии, утяжеляющего заболевания и особенно опасного для детей с пороками сердца. Кроме того, возможное обострение очаговой хронической инфекции на фоне ОРВИ у детей с пороками сердца существенно увеличивает риск развития инфекционного эндокардита. Все это обусловило наш интерес к этиотропным препаратам для лечения гриппа и ОРВИ, ранее редко использовавшимся в стационаре.
Целью настоящего исследования явилась оценка эффективности Орвирема в терапии среднетяжелых и тяжелых (осложненных) форм острой респираторной патологии у детей в условиях инфекционного педиатрического стационара.
Материалы и методы
Проведено открытое двойное слепое рандомизированное исследование. Основную группу составили 50 «часто болеющих» детей от 1,3 до 7,5 лет (средний возраст 4,5 ± 1,5 года), включая 19 детей с ВПС. Общее число интеркуррентных заболеваний с обострением хронических очагов ЛОР-патологии было у каждого их них не менее 6–7 раз в год. Дети поступали в стационар в 1–3 сутки заболевания, из них 50% на первый день болезни, с катаральными явлениями, интоксикацией и фебрильными подъемами температуры (табл. 1).
Критериями включения детей в основную группу являлись наличие симптомов ОРЗ, интоксикация и фебрильные подъемы температуры, первые 3 дня заболевания, отсутствие антибактериальной, противовирусной и иммуномодулирующей терапии до госпитализации. При оценке тяжести течения использовались принятые критерии тяжести ОРВИ, а именно: выраженность синдрома интоксикации и синдрома поражения респираторного тракта. Легкой формой считали слабо выраженный синдром интоксикации, температуру тела не более 38–38,5 °С; среднетяжелой формой — умеренно выраженную интоксикацию с температурой тела 39–39,5 °С, умеренно выраженными местными изменениями; тяжелая (токсическая) форма характеризовалась наличием нейротоксикоза, менингеального, энцефалитического, судорожного синдромов, выраженной интоксикации, первично возникающих тяжелых местных осложнений, геморрагического синдрома.
На основании данных критериев среднетяжелое течение было диагностировано у 29 детей (58%) и тяжелое у 21 ребенка (42%) детей основной группы (табл. 2).
Контрольную группу составили 30 детей идентичного возраста со сходной патологией, госпитализированные в ДИКБ № 6 УЗ САО г. Москвы, получавшие с момента поступления с 1–3 дня заболевания только симптоматическую терапию и/или антибактериальное лечение.
Основные клинические симптомы при поступлении в стационар в основной и контрольной группах были сопоставимы (табл. 3). При раннем поступлении и неосложненных формах ОРВИ 21-му ребенку основной группы назначался только Орвирем в качестве монотерапии с момента госпитализации в стационар в дозе: детям 1–3 лет по 2 ч. л. (10 мл) 3 раза в день на 1-й и 2-й день заболевания, 2 раза в день на 3-й и 1 раз в день на 4-й день болезни. Детям 3–7 лет в дозе по 3 ч. л. (15 мл) 3 раза в день на 1-й и 2-й день заболевания, 2 раза в день на 3-й и 1 раз в день на 4-й день болезни. Детям с исходно осложненными (бронхитом, пневмонией, острым тонзиллитом, отитом) формами ОРВИ, преимущественно в возрасте до двух лет, и детям с ВПС и недостаточностью кровообращения Орвирем назначался на фоне антибактериальной терапии (Цефазолин, Сумамед) в возрастных дозировках (n = 29). Дети осматривались ЛОР-врачом на первые, пятые, седьмые и десятые сутки лечения. Идентификация возбудителей ОРВИ (вирусов гриппа А и В, вирусов парагриппа, аденовируса, РС-вируса, микоплазмы пневмонии) проводилась методами иммуноферментного анализа (ИФА) и полимеразной цепной реакции (ПЦР) по принятым стандартам.
Результаты исследования
При оценке данных вирусологического исследования, проведенного в первые 24 ч с момента поступления в стационар у 22 детей основной группы (в 44% наблюдений) и у 14 детей контрольной группы (в 46,7% наблюдений) были идентифицированы возбудители респираторных инфекций. Возбудители идентифицированы не были у 28 детей основной группы (56%) и 16 детей контрольной (53,7%).
Анализ частоты положительных результатов вирусологического исследования в основной и контрольной группах, а также характера основных клинических проявлений респираторного заболевания в зависимости от вида возбудителя показал полную сопоставимость групп сравнения для последующего анализа эффективности терапии.
Как следует из рис. 2, рис 3, в целом на фоне терапии Орвиремом интоксикационный и катаральный синдром регрессировали существенно быстрее и у большего числа пациентов основной группы по сравнению с контрольной. Лихорадочный период сокращался в среднем до 12–48 часов, уменьшение других симптомов интоксикации (слабость, адинамия, потливость) наблюдалось в среднем к 2–3 суткам приема препарата. Катаральные явления, ринит и кашель достаточно быстро ликвидировались в течение 2–4 суток у 50% больных основной группы.
За период наблюдения у пациентов основной группы, получавших Орвирем, ни в одном случае не было отмечено вновь возникших бактериальных осложнений и обострений хронической очаговой инфекции.
В контрольной группе больных с идентичной симптоматикой динамика реконвалесценции отставала по срокам и выраженности, несмотря на использование современных антибактериальных средств, в 5% наблюдений отмечено обострение хронической очаговой инфекции (хронического тонзиллита) или бактериальных осложнений (бронхит, пневмония).
Выраженность катарального и интоксикационного синдромов оценивалась в условных баллах от «0» (при отсутствии симптомов) до «5» (при их максимальной выраженности) по суммарной выраженности их клинических составляющих (лихорадка, вялость, гиподинамия, воспалительные изменения со стороны слизистых рото- и носоглотки, кашлевой синдром и др.).
Анализ динамики интоксикационного и катарального синдромов в основной группе на фоне терапии Орвиремом в зависимости от вида возбудителя показал достаточно высокую эффективность при гриппе А, в соответствии с аннотацией препарата, однако сопоставимая высокая эффективность была подтверждена в случаях аденовирусной, РС-вирусной и микоплазменной инфекций.
Анализ динамики интоксикационного и катарального синдромов в основной группе на фоне терапии Орвиремом показал тенденцию к более быстрой ликвидации симптомов у пациентов с положительными результатами вирусологического исследования. Это, с большой вероятностью, позволяет считать, что в этиологии ОРЗ у детей с отрицательными результатами вирусологического исследования могли иметь значение бактериальная и атипичная микрофлора и другие (не изучавшиеся в данном исследовании) вирусные агенты.
Проведенные исследования показали, что в педиатрической практике Орвирем достаточно эффективен для монотерапии и комплексной терапии катарального и интоксикационного синдромов ОРВИ, для профилактики осложнений, ускорения реконвалесценции, сокращения сроков пребывания в стационаре (рис. 4).
Таким образом, помимо ранее декларированной для гриппа А, достаточная эффективность Орвирема отмечена для РС-вирусной, микоплазменной и аденовирусной инфекций, а также для гриппа В и для смешанной вирусно-бактериальной этиологии респираторных инфекций.
Наши исследования показали, что на фоне лечения Орвиремом в основной группе существенно реже, чем в контрольной группе, отмечались обострения хронической очаговой ЛОР-патологии в виде хронического тонзиллита и ринофарингита (соответственно у 10% и 30% больных детей). Таким образом, применение Орвирема уменьшало показания к назначению дорогостоящих симптоматических средств (в частности, бронхолитиков), уменьшало полипрагмазию. Орвирем хорошо переносился детьми, его прием не сопровождался аллергическими реакциями и иным побочным действием.
Заключение
- Использование противовирусного препарата Орвирем в ранние сроки острого инфекционного поражения респираторного тракта у детей в возрасте 1–7 лет (включая детей с сопутствующей кардиальной патологией) сокращает длительность интоксикационного и катарального синдромов, уменьшает частоту специфических и неспецифических бактериальных осложнений, сокращает сроки пребывания в стационаре.
- Максимальная эффективность препарата по динамике основных клинических синдромов отмечена при этиологически подтвержденных гриппе А, адено- и РС-вирусной инфекции, микоплазменной инфекции. Достаточная эффективность подтверждена для гриппа В и при смешанной вирусно-бактериальной этиологии респираторных инфекций.
- Романцов М. Г., Ершов Ф. И. Часто болеющие дети. Современная фармакотерапия: Руководство для врачей. М., 2009. 352 с.
- Grossman R. F. Chest/113/205 ff (1998).
- Информационное письмо проф. Ильенко Л. И. и др. М., 1999.
- Романцов М. Г., Горячева Л. Г., Коваленко А. Л. Противовирусные и имунотропные препараты в детской практике. Руководство для врачей. СПб. 2008. 123 с., с. 12.
- Самсыгина Г. А. Современные подходы к лечению острой инфекции респираторного тракта у часто болеющих детей // Педиатрия. Consilium Medikum. 2008. № 2.
- Пикуза О. И, Ослопов В. Н., Вахитов Х. М., Бабкшкина А. А., Никольский С. Е. Прогнозирование атеросклероза у детей и возможности ранней профилактики ишемической болезни сердца // Казанский медицинский журнал. 1999, т. LXXX, № 4, с. 296–297.
- Вахитов Х. М, Пикуза О. И. Повторные острые респираторные заболевания как фактор риска развития дислипидемий у детей // Педиатрия Сперанского. 2004. № 5. С. 35–37.
- Degtyareva H., Samuilova D. Sh., Razuvaev M. K., Khurges I. S. Immunological Scrining and Immune Correction in Cardiosurgery ofInfants // Bul. of Experimental Biology and Medisin, Consultants Bureau. New-York. 1993. Vol. 115. № 4. P. 417–421.
- Дегтярева Е. А. Иммунологическая недостаточность и иммунореабилитация в детской кардиологии // Лекции по педиатрии. 4 том. Кардиология, 2004. М., с. 323–344.
Е. А. Дегтярева
Д. Ю. Овсянников, кандидат медицинских наук, доцент
О. И. Жданова
С. И. Лазарева
РУДН, Детская инфекционная клиническая больница № 6, Москва
Контактная информация об авторах для переписки: dag@diod.ru; helendoc@hotdox.ru
Сроки госпитализации от момента начала заболевания в основной и контрольной группах
Купить номер с этой статьей в pdf