Стартовая терапия тяжелых и осложненных внебольничных пневмоний. Тяжелое и осложненное течение пневмонии, как правило, отмечается у детей с иммунодефицитными состояниями, пороками развития, органическими поражениями центральной нервной системы (ЦНС) и другими серьезными нарушениями здоровья. Однако нельзя забывать о том, что причинами данных форм пневмонии могут также являться поздняя диагностика и неадекватное лечение, в первую очередь ошибки при проведении антимикробной терапии.
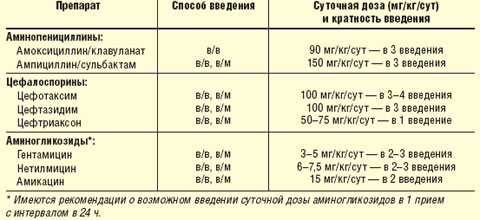
Лечение детей с тяжелыми пневмониями включает рациональную антибактериальную терапию, адекватную респираторную поддержку, иммунотерапию, коррекцию и поддержание гомеостатических параметров (водно-электролитный баланс и др.), а также купирование патологических синдромов (гипертермический, геморрагический, судорожный, синдром сердечной недостаточности и др.). Особо следует отметить, что лечение детей с легочными осложнениями пневмонии (абсцесс легкого, пиоторакс, пиопневмоторакс, эмпиема) должно осуществляться в условиях хирургического стационара или в отделениях интенсивной терапии и реанимации, но с обязательным привлечением детского хирурга. Важным компонентом лечения пневмонии является рациональная антимикробная терапия. Стартовая антибактериальная терапия при этом проводится комбинациями препаратов (ингибиторозащищенный аминопенициллин + аминогликозид или цефалоспорин III поколения + аминогликозид). Следует подчеркнуть, что при тяжелых и осложненных формах пневмоний предпочтение должно отдаваться внутривенному введению антибиотиков. Антибиотики при этом должны назначаться в таких режимах дозирования, которые создают максимальные терапевтические концентрации. Так, амоксициллин/клавуланат при внутривенном введении используют в разовой дозе 30 мг/кг (по амоксициллину) с интервалом 6–8 ч (табл. 1). Цефотаксим, цефтизоксим и цефтазидим назначают в суточной дозе 100 мг/кг в 3–4 введения. В то же время особенности фармакокинетики такого цефалоспорина III поколения, как цефтриаксон (75 мг/кг/сут), позволяют использовать его соответственно 1 раз в сутки. Среди аминогликозидов, назначаемых в комбинации с «защищенными» аминопенициллинами или цефалоспоринами, наиболее часто используются гентамицин (суточная доза 3–5 мг/кг в 2–3 введения), амикацин (суточная доза 15 мг/кг в 2 введения) и нетилмицин (суточная доза 6–7,5 мг/кг в 2–3 введения). Следует подчеркнуть, что в последние годы имеются рекомендации по назначению аминогликозидов 1 раз в сутки с интервалом в 24 ч (табл. 1).
Таблица 1 |
Позитивный клинический эффект и положительная рентгенологическая динамика на фоне проводимой антибактериальной терапии свидетельствуют о том, что стартовый выбор препаратов и их режим дозирования были сделаны правильно. Достижение терапевтического эффекта при этом позволяет выстроить рациональную тактику дальнейшего применения антибиотиков. Так, если лечение ребенка начинали с комбинации аминогликозид + β-лактамный антибиотик («защищенный» аминопенициллин или цефалоспорин) и при этом была достигнута положительная клиническая динамика, то целесообразно продолжить терапию стартовыми препаратами. При этом β-лактамные антибиотики применяют с продолжительностью до 10–14 дней, в то время как использование аминогликозидов не должно превышать 5–7 дней в связи с высоким риском развития ото- и нефротоксических эффектов.
Отрицательная динамика заболевания, а также появление клинических и рентгенологических признаков деструкции легочной ткани или вовлечение в патологический процесс плевры свидетельствуют о неэффективности проводимой антибактериальной терапии и требуют ее коррекции. Развитие плевропневмонии, абсцесса, пиоторакса и других гнойно-воспалительных изменений в легких является абсолютным показанием для привлечения детских хирургов к совместной курации таких пациентов. Коррекция антимикробной терапии должна обязательно учитывать результаты бактериологического обследования, предварительные результаты которого, как правило, в этот период уже готовы. В тех же случаях, когда приходится проводить смену антимикробной терапии эмпирически, должны назначаться препараты резерва — антибиотики «сверхширокого спектра действия» — карбапенемы (имипенем, меропенем) или цефалоспорин 4-й генерации (цефепим — 100 мг/кг/сут в 3 введения). Имипенем назначается в суточной дозе 60 мг/кг, которая вводится в 4 приема. Суточная доза меропенема — 30–60 мг/кг в 3 введения (табл. 2). Указанные антибиотики обладают сверхширокой антибактериальной активностью, «перекрывая» практически весь спектр потенциальных возбудителей пневмонии. При этом следует особо отметить, что назначение «антибиотиков резерва» без веских на то оснований может привести к селекции полирезистентных штаммов. В то же время к карбапенемам и цефалоспоринам IV поколения резистентны метициллиноустойчивые стафилококки и энтерококки, для которых препаратом выбора является ванкомицин. Однако в последние годы из-за необоснованно частого применения ванкомицина отмечено появление устойчивости к нему у некоторых штаммов стафилококка и энтерококка.
Таблица 2 |
Таким образом, пневмония по-прежнему остается одним из наиболее серьезных заболеваний у детей раннего возраста, прогноз которого во многом определяется ранней верификацией и назначением адекватной антибактериальной терапии. При этом своевременная диагностика пневмонии и рациональное использование антибиотиков позволяет существенно снизить риск развития осложнений и неблагоприятных исходов заболевания.
Литература
- Таточенко В. К. Практическая пульмонология детского возраста. М., 2001. 268 с.
- Острые респираторные заболевания у детей: лечение и профилактика / Научно-практическая программа Союза педиатров России. М.: Международный фонд охраны здоровья матери и ребенка, 2002. 69 с.
- Классификация клинических форм бронхолегочных заболеваний у детей // Рос. вест. перинатол. и педиатр. 1996. № 2. С. 52-56.
- Пневмонии у детей / под ред. С. Ю. Каганова, Ю. Е. Вельтищева. М.: Медицина, 1995.
- Churgay C. A. The diagnosis and management of bacterial pneumonias infant and children // Primary Care. 1996; 4: 822-835.
- Gendrel D. Pneumonies communautaires de I'enfant: etiologie et treatment // Arh. Pediatr. 2002; 9(3): 278-288.
- Red Book: Report of the Committee on Infectious Diseases / 27h ed. Elk Grove Village, IL: American Academy of Pediatrics, 2006; 992.
- management of acute respiratory infections in children. Practical guidelines for outpatient care, WHO, Geneva, 1995.
- World Health Report 1995: Bridging the gaps. WHO, Geneva, 1995.
- Коровина Н. А., Заплатников А. Л., Захарова И. Н. Антибактериальная терапия пневмоний у детей. М.: Медпрактика-М, 2006. 48 с.
- Международная статистическая классификация болезней и проблем, связанных со здоровьем. 10-й пересмотр. ВОЗ, 1994 (пер. на рус.) М.: Медицина, 1998.
- Антибактериальная терапия пневмонии у детей: пособие для врачей // Клиническая микробиология и антимикробная терапия у детей. 2000. № 1. С. 77-87.
- Страчунский Л. С. Антибактериальная терапия пневмоний у детей: руководство по фармакотерапии в педиатрии и детской хирургии / под ред. С. Ю. Каганова. М.: Медпрактика-М, 2002. Т. 1. С. 65-103.
- Самсыгина Г. А., Дудина Т. А. Тяжелые внебольничные пневмонии у детей: особенности клиники и терапии // Consilium Medicum. 2002. № 2. С. 12-16.
- Практическое руководство по антиинфекционной химиотерапии / под ред. Л. С. Страчунского, Ю. Б. Белоусова, С. Н. Козлова. М., 2002.
- Белоусов Ю. Б., Омельяновский В. В. Антимикробные средства // Клиническая фармакология болезней органов дыхания. М.: Универсум Паблишинг, 1996. С. 16-85.
- Государственный реестр лекарственных средств. М.: МЗиСР РФ (интернет-версия: www.drugreg.ru, 2007).
- Block S., Hedrick J., Hamerschlag M. R. et al. Mycoplasma pneumoniae and Chlamydia pneumoniae in pediatric community-acquired pneumonia // Pediatr. Infect. Dis. J. 1995; 14: 471-477.
- Principi N., Esposito S., Blasi F., Allegra L. Role of Mycoplasma pneumoniae and Chlamydia pneumoniae in children with community-acquired lower respiratory tract infections // Clin. Infect. Dis. 2001; 32: 1281-1289.
А. Л. Заплатников, доктор медицинских наук, профессор
РМАПО, Москва
(Продолжение. Начало см. в № 7)