Острые вирусные гепатиты (ОВГ) составляют группу самых распространенных заболеваний печени. Ежегодно в мире фиксируется 1–2 млн смертельных исходов ОВГ.
Острый вирусный гепатит может выступать как самостоятельная нозологическая форма (гепатиты А, В, С, D, E, F) и как «спутник» общей вирусной инфекции (герпетической, аденовирусной, инфекции, вызываемой вирусом Эпштейна–Барра, и др.).
По механизму заражения, биологическим особенностям возбудителей и характеру течения острые вирусные гепатиты можно разделить на две группы.
Первая группа — ОВГ с энтеральным (фекально-оральным) механизмом заражения. Основные пути передачи — водный, пищевой, контактно-бытовой. Возбудителями в этих случаях являются безоболочечные вирусы: вирус гепатита А (HAV — hepatitis A virus), вирус гепатита Е (HEV) и предположительно вирус гепатита F (HFV). ОВГ с энтеральным механизмом заражения разрешается без формирования вирусоносительства.
Вторая группа — ОВГ с парентеральным механизмом заражения. Возбудители гепатита этого типа — вирусы гепатитов B, C, D, G (соответственно, HBV, HCV, HDV, HGV) — имеют оболочку. Особенностью течения болезни является наклонность к персистенции вирусов и развитию хронического поражения печени.
Прежде чем перейти к рассмотрению особенностей острой инфекции вирусом гепатита А, целесообразно кратко рассмотреть некоторые клинические особенности, присущие всем острым вирусным гепатитам.
Клиническая картина ОВГ характеризуется широким спектром проявлений. Однако можно выделить следующие основные типы течения ОВГ: самоограничивающийся, фульминантный (молниеносный), холестатический, рецидивирующий (рис. 1).
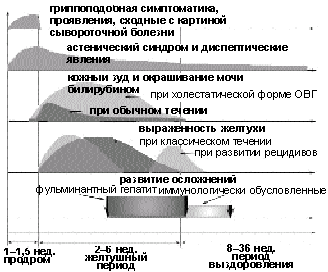 |
Рисунок 1. Динамика клинических проявлений при ОВГ |
Cамоограничивающийся (циклический) тип течения ОВГ. Тяжесть течения болезни варьирует от субклинических до тяжелых форм. Независимо от этиологии заболевания, характерно его начало с продромального периода, во время которого у больного появляются неспецифические общие (астения) и желудочно-кишечные (снижение аппетита, тошнота, рвота, боли в правом подреберье, изменения стула) симптомы; могут отмечаться гриппоподобные явления. В редких случаях развивается синдром, подобный сывороточной болезни (кожные сыпи, артралгии, симметричная артропатия, полимиозит). Длительность продромального периода составляет 7–10 дней. Следует отметить, что в подавляющем большинстве случаев возникновение симптоматики продромального периода вследствие ее неспецифичности ни пациент, ни врач не связывают с развивающимся ОВГ, и изменения в состоянии больного расцениваются как острое респираторное заболевание, грипп, пищевая токсикоинфекция или переутомление.
Выраженность продромальных явлений уменьшается с развитием желтушного периода (периода разгара болезни), в котором выделяют фазы нарастания, максимального развития и уменьшения желтухи. Появлению желтухи предшествует потемнение мочи. В фазу нарастания желтухи может отмечаться преходящий кожный зуд. В этот период общее самочувствие пациента обычно улучшается, выраженность астении уменьшается. При осмотре выявляют умеренно увеличенную болезненную печень, непостоянным признаком является увеличение селезенки и лимфатических узлов заднешейной группы. Длительность желтушного периода составляет от 1–2 дней до нескольких месяцев (в среднем — 2–6 нед).
Начиная с острого периода инфекции, у пациента могут манифестировать разнообразные внепеченочные проявления, имеющие иммунокомплексное происхождение (кожные сыпи, артралгии, хронический мембранозный гломерулонефрит, узелковый артериит, миокардит, синдром Гийена–Барре, эссенциальная смешанная криоглобулинемия). Возможно, их развитие обусловлено также изменением функций мононуклеарных фагоцитов.
В ряде случаев даже в разгар болезни она может протекать стерто, без желтухи и заметного изменения цвета мочи и кала. Поэтому даже в этот период ОВГ может остаться нераспознанным.
В крови обнаруживают увеличение активности аланиновой аминотрансферазы (АЛТ) и аспарагиновой аминотрансферазы (АСТ) в 10–100 раз, а также увеличение концентрации билирубина в 2–10 раз (количественное соотношение «общий билирубин / прямой билирубин» близко таковому при механической желтухе, что отражает развитие внутриклеточного холестаза).
Достоверной связи между степенью повышения активности сывороточных трансаминаз и тяжестью поражения печени не выявлено.
Тяжесть течения ОВГ в большей степени отражает не столько выраженность гипербилирубинемии, сколько длительность желтушного периода.
Уровень щелочной фосфатазы, протромбиновый индекс и уровень сывороточного альбумина обычно остаются в пределах нормы. Наблюдается лейкопения с развитием относительного лимфоцитоза или без него.
Гистологические изменения в печени в фазе разгара ОВГ включают: гидропическую баллонную дистрофию и некрозы гепатоцитов, апоптозные тельца, сходные с тельцами Каунсильмена, эндофлебит центральных венул, мононуклеарную инфильтрацию портальных трактов (в составе инфильтрата преобладают цитотоксические лимфоциты и клетки — натуральные киллеры) с сегментарным разрушением терминальной пластинки и паренхимы долек. Клетки Купфера увеличены в размерах, содержат липофусцин и клеточный детрит.
Фаза реконвалесценции продолжается 2–12 мес и сопровождается остаточными астеновегетативными и диспепсическими проявлениями. В этой фазе в течение нескольких месяцев происходит новообразование соединительной ткани в портальных и перипортальных зонах ацинуса.
При отсутствии нормализации клинико-лабораторных параметров в течение 3 мес болезнь расценивают как «ОВГ затянувшегося течения».
Фульминантный гепатит.
Клиническая картина характеризуется быстрым нарастанием признаков печеночной недостаточности (желтуха, печеночная энцефалопатия, коагулопатия, асцит, анасарка), развитием полиорганной недостаточности (респираторный дистресс-синдром взрослых, гипотензия, нарушения сердечного ритма, гепато-ренальный синдром). При динамическом осмотре отмечается уменьшение размеров печени.
При лабораторном исследовании выявляют тяжелую коагулопатию, лейкоцитоз, гипонатриемию, гипокалиемию, гипогликемию. Уровни билирубина и трансаминаз значительно повышены. При повторных исследованиях уровни трансаминаз могут снижаться до нормы, несмотря на прогрессирование заболевания.
Биопсию печени при фульминантном гепатите проводят редко из-за наличия противопоказания — тяжелой коагулопатии. Гистологическая картина изучена на аутопсийном материале; в подобных случаях выявляют массивные участки некроза паренхимы (с тотальным вовлечением ацинуса) и коллапс ретикулярной стромы.
Летальность при этой форме течения ОВГ составляет около 60%. Основными причинами смерти являются отек мозга и легких, массивное желудочно-кишечное кровотечение.
Холестатический гепатит. Такой вариант течения наиболее характерен при инфекции, обусловленной HAV. Характерный клинический симптом — выраженная желтуха, которая сохраняется в течение 2–5 мес и сопровождается кожным зудом и лихорадкой. У части больных отмечаются длительный период снижения или полного отсутствия аппетита и диарея.
Характерно значительное повышение уровней билирубина (до 20 раз) и щелочной фасфатазы в крови. Уровни трансаминаз умеренно повышены и могут достигать нормальных значений на фоне сохраняющегося холестаза.
При гистологическом исследовании печени выявляют дистрофию и некроз гепатоцитов, воспалительную инфильтрацию, такую же, как при самоограничивающемся течении гепатита, большое количество желчных цилиндров в расширенных желчных канальцах, накопление билирубиновых гранул в гепатоцитах и их псевдогранулярную трансформацию. Прогноз при этой форме течения гепатита обычно благоприятный.
Рецидивирующий гепатит. Основной этиологический фактор при этой клинической форме ОВГ — это HAV.
На фоне разрешения острого гепатита или уже после клинического выздоровления у больного повторно появляются клинико-лабораторные признаки, наблюдающиеся в остром периоде, включая иммунологически опосредованные внепеченочные проявления (см. выше). Гистологические признаки соответствуют таковым при самоограничивающемся течении гепатита. Заболевание заканчивается выздоровлением.
Представляется, что с предшествующим ОВГ могут быть патогенетически связаны такие патологические состояния, как синдром Гийена–Барре, апластическая анемия, панмиелофтиз.
В случае развития ОВГ на фоне уже имеющегося хронического заболевания печени может наблюдаться выраженная декомпенсация функции печени. Если причины резкого ухудшения состояния больного с хронической патологией печени, нарастания уровня трансаминаз и билирубина неясны, следует заподозрить присоединение ОВГ.
Общие принципы лечения ОВГ
При самоограничивающемся течении госпитализация больного не является обязательной в том случае, если у него отсутствуют многократная рвота, анорексия, диарея (которые могут привести к дегидратации и нарушениям электролитного обмена), а также если ухаживающие за пациентом на дому способны обеспечить необходимые санитарно-противоэпидемические меры. В течение всего периода течения ОВГ необходим периодический врачебный контроль состояния больного для своевременного распознавания фульминантной формы течения.
Следует обеспечить пациенту достаточную калорийность пищи и прием жидкости в нужном объеме. Необходимости придерживаться строгих диетических предписаний нет. В острой фазе болезни противопоказано употребление алкоголя. Целесообразно избегать интенсивных или длительных физических нагрузок. Степень физической и умственной активности во многом определяется самочувствием пациента.
Специфических методов лекарственной терапии не разработано. В ряде случаев по показаниям назначают противорвотные средства, спазмолитики, анальгетики, при дегидратации проводят инфузионную терапию (внутривенное введение раствора глюкозы). Кортикостероиды, в связи с опасностью повышения частоты хронизации инфекции, не показаны.
При ОВГ С и ОВГ G показано проведение противовирусной терапии для снижения риска формирования хронической инфекции.
При появлении признаков развития фульминантного гепатита необходима срочная госпитализация больного, по возможности в гепатологические центры, где возможно проведение трансплантации печени. В клинике устанавливают наблюдение за состоянием пациента, проводят контроль рН, содержания электролитов и глюкозы в крови, мониторинг центрального венозного и внутричерепного давления, осуществляют мероприятия по поддержанию жизненно важных функций и лечение осложнений. В частности, назначают маннитол при прогрессировании отека мозга, антибиотики для подавления кишечной микрофлоры и лечения инфекционных осложнений. При отсутствии положительной динамики больного готовят к трансплантации печени.
При холестатическом варианте течения с целью уменьшения выраженности кожного зуда и ускорения разрешения холестаза проводят лечение преднизолоном (30 мг/сут в течение 3 нед) или препаратами урсодеоксихолевой кислоты. Возможно назначение холестирамина и антигистаминных средств.
Рекомендации по ведению пациента с рецидивирующим гепатитом аналогичны тем, которые даются при самоограничивающемся течении заболевания.
Острый вирусный гепатит А
Возбудитель. HAV представляет собой РНК-содержащий вирус из группы Picornaviridae (подкласс Hepatovirus), не имеющий оболочки, диаметром 27–30 нм, с кубической симметрией (рис. 2). Белки капсида образуют 60 центромер. Одноцепочечная линейная молекула РНК кодирует структуру белков капсида, протеаз Р2, Р3 и РНК-полимеразы. Идентифицирован один серотип и несколько генотипов HAV.
Рисунок 2. Схематическое изображение строения вируса гепатита А |
Эпидемиология. Источником заражения является больной ОВГ А.
Вирус выделяется из организма больного в течение 1–2 нед в преджелтушном и по меньшей мере 1 нед — в желтушном периоде.
HAV обладает высокой устойчивостью во внешней среде.
Механизм передачи инфекции — преимущественно фекально-оральный. Число случаев заражения парентеральным (при переливании крови инфицированного донора) и половым (у гомосексуалистов, рассматриваемый как фекально-оральный) путем небольшое. Нельзя полностью исключить возможность воздушно-капельной передачи. Вертикальная передача вируса (от матери плоду) не установлена.
Восприимчивость к инфекции высокая. Уровень заболеваемости значительно различается в разных регионах. В странах Восточной Европы он составляет в среднем 250 случаев на 100 тыс. населения в год. В северных широтах выражена сезонность заболеваемости с повышением в осенне-зимний период. ОВГ А регистрируется спорадически, в виде вспышек или в виде эпидемий, которые в развивающихся странах возникают с периодичностью 4–5 лет.
Основные факторы риска развития ОВГ А: перенаселенность, несоблюдение правил гигиены, поездки за рубеж, контакты с больным в быту, гомосексуальные контакты, контакты с детьми из детских садов, наркомания.
Инкубационный период — среднем 30 (15–50) дней.
Патогенез. Из желудочно-кишечного тракта вирус попадает в печень. Вирионы реплицируются в цитоплазме гепатоцита и выделяются в желчь (рис. 3).
Рисунок 3. Репликация HAV в клетках печени |
Лизис гепатоцитов опосредован иммунным ответом на инфекцию при участии цитотоксических Т-лимфоцитов и/или механизма антителозависимой клеточно-опосредованной цитотоксичности. Предполагается, что HAV не обладает значительной прямой цитопатогенностью.
Клиническая картина. Субклиническое течение, часто под маской острого гастроэнтерита, как правило (до 90% случаев), наблюдается у детей. У взрослых ОВГ А обычно протекает в манифестной форме.
В продромальном периоде возможна лихорадка (до 39° С). С появлением желтухи отмечается улучшение самочувствия.
В острый период может наблюдаться кореподобная или сходная с крапивницей кожная сыпь. В целом частота внепеченочных проявлений существенно ниже, чем при ОВГ В или С.
В фазе реконвалесценции у незначительного числа больных развиваются преходящий асцит, не являющийся неблагоприятным прогностическим признаком, а также преходящая протеинурия и гематурия. Происхождение этих симптомов не установлено.
Для ОВГ А наиболее характерно развитие холестатических форм с мучительным кожным зудом. Чаще, чем при других ОВГ, наблюдаются рецидивы, особенно в детском возрасте. Они развиваются спустя 30–90 дней от начала болезни, что связано, как предполагают, с повторным заражением или реактивацией первичной инфекции. Картина рецидива напоминает таковую при первой атаке, с повторным выделением вируса. Рецидивы заканчиваются выздоровлением, изредка сопровождаются артритом, васкулитом, криоглобулинемией. Прогнозировать развитие рецидива можно по отсутствию тенденции к снижению уровня сывороточной АЛТ.
Серологическая диагностика. В крови, кале, дуоденальном содержимом в остром периоде может быть обнаружен антиген HAV (HААg) с помощью реакции иммунофлюоресценции, метода фиксации комплемента, радиоиммунного метода или иммуноферментного метода (ELISA). Однако в клинической практике эти методики не нашли широкого применения.
Наиболее доступными методами вирусологической диагностики служит выявление антител классов IgM и IgG к вирусу.
Высокоспецифичные для ОВГ А анти-HAV класса IgM можно обнаружить в сыворотке крови на протяжении всей острой фазы болезни и последующих 3– 6 мес (до 1 года в низком титре).
Анти-НАV класса IgG, по всей вероятности, обеспечивают стойкий иммунитет и сохраняются в течение всей жизни после перенесенного ОВГ А.
Течение и прогноз. Длительность заболевания в среднем составляет 6 нед. Как правило, больные выздоравливают без специального лечения.
Вероятность летального исхода не превышает 0,001%.
Хронизации инфекции не наблюдается. Функция и гистологическая картина печени обычно нормализуются в течение 6 мес.
Таблица Риск развития острой печеночной недостаточности при острых вирусных гепатитах |
Среди осложнений описано развитие мезангиопролиферативного гломерулонефрита с нефротическим синдромом. Имеются данные о пусковой роли ОВГ А в развитии аутоиммунного гепатита I типа у лиц с нарушениями функции Т-лимфоцитов-супрессоров.
Профилактика. Неспецифические методы профилактики включают изоляцию больных и лиц, контактировавших с ними на протяжении 2 последних недель преджелтушного и 1 нед желтушного периода, дезинфекцию предметов, которыми пользуется больной, мытье рук, соответствующую кулинарную обработку пищи во время болезни.
Профилактические меры до контакта с больным (профилактика с «отсроченным эффектом») включают в себя активную иммунизацию инактивированной HAV-вакциной.
Вакцинация показана жителям областей с низким и средним уровнем заболеваемости, лицам, входящим в группы риска: выезжающим в эндемичные районы; пациентам, которым часто производят инъекции лекарственных препаратов; детям и молодым людям, проживающим в условиях скученности; военнослужащим; пациентам с хроническими заболеваниями печени; работникам лабораторий, контактирующим с HAV; гомосексуалистам; иногда — работникам детских учреждений и предприятий пищевой промышленности.
Режим дозирования: взрослым старше 19 лет — введение вакцины в два этапа по 1440 Elisa Units (EU) с перерывом в 6–12 мес. Детям старше 2 лет вакцинацию проводят с использованием трехэтапного режима — по 360 ЕU c перерывом в 1 и 6–12 мес, — или двухэтапного — по 720 ЕU с перерывом в 6–12 мес.
Однократная вакцинация обеспечивает иммунитет в течение 1 года, повторная («усиливающая») — в течение 5-10 лет.
Профилактическая эффективность вакцины составляет 95–100%. Иммуногенность весьма высока: почти у 100% здоровых пациентов вакцина вызывает продукцию анти-HAV (у 85% вакцинированных — в течение 15 дней). Переносимость хорошая. Отсутствует опасность заражения других лиц после вакцинации.
Введение живой аттенуированной вакцины также служит эффективным способом профилактики ОВГ А, однако он еще не нашел широкого применения.
Рисунок 4. Изменения серологических показателей при ОВГ А |
Профилактические меры после контакта с больным (профилактика с «немедленным эффектом») подразумевают проведение пассивной иммунизации сывороточным иммуноглобулином. Показания к ее проведению: внутрисемейные и близкие контакты с больным ОВГ А (иммунизируют, в том числе и грудных детей). Не применяют при случайных спорадических контактах вне дома. Иммунизация больших групп оправдана при реальной опасности возникновения эпидемий.
Режим дозирования иммуноглобулина: 0,02 мл/кг массы тела вводят в дельтовидную мышцу не позднее 14 дней после контакта с больным.
Метод может быть также использован для быстрой иммунизации лиц, выезжающих в эндемичные районы, но в более высокой дозе — 0,06 мл/кг массы тела (предварительно желательно определить у пациента наличие анти-HAV в крови).
При сохранении напряженной эпидемиологической обстановки возможна повторная иммунизация.
Эффективность пассивной иммунизации в предупреждении клинически манифестных форм ОВГ А составляет 100% при введении до контакта и 80–90% — при введении в пределах шести дней после контакта. Переносимость иммуноглобулина оценивается как хорошая.
Возможны одновременное проведение активной и пассивной вакцинации с контралатеральным введением (при выезде в эндемичные районы), а также одновременная активная вакцинация против гепатитов А и В.
Ю.О. Шульпекова, кандидат медицинских наук
ММА им. И. М. Сеченова, Москва
По вопросм литературы обращайтесь в редакцию.