Доброкачественная гиперплазия предстательной железы (ДГПЖ) представляет собой одно из наиболее распространенных заболеваний у мужчин пожилого и старческого возраста и характеризуется морфологическим наличием доброкачественной фиброэпителиальной ткани, расположенной в окружности проксимальной части мочеиспускательного канала.
Аутопсийные исследования демонстрируют, что морфологические признаки ДГПЖ обнаруживаются у 50% мужчин в возрасте от 40 до 50 лет и у 90% мужчин в возрасте старше 80 лет. Клинически заболевание также имеет достаточно широкое распространение, при этом признаки нарушенного мочеиспускания устанавливаются у 60% мужчин в возрасте свыше 60 лет.
Уменьшение диаметра струи мочи констатируют 25% мужчин в возрасте 55 лет, а среди пациентов старше 75 лет их число достигает уже 50% (J. J. Medina,1999). Расчеты, основанные на результатах эпидемиологических исследований, свидетельствуют о том, что у мужчин в возрасте от 50 лет вероятность оперативного вмешательства по поводу ДГПЖ составляет 30%.
Симптоматика заболевания при ДГПЖ формируется за счет трех компонентов: статического (механического), динамического, а также нарушения функциональной способности мочевого пузыря.
Статический компонент ДГПЖ формируется вследствие увеличения в размерах фиброзно-мышечной ткани переходной зоны предстательной железы. Динамическая составляющая симптоматики заболевания связана с повышенным тонусом α1-адренергических рецепторов предстательной железы и шейки мочевого пузыря, что обусловливает сокращение гладкомышечных элементов данной анатомической зоны. Назначение препаратов группы α1-адреноблокаторов, расслабляющих гладкомышечные элементы предстательной железы, приводит к снижению степени обструкции. Кроме этого, у 25% мужчин, страдающих ДГПЖ, также обнаруживается снижение сократительной активности стенки мочевого пузыря и развиваются признаки нестабильности детрузора, что особенно характерно для больных пожилого и старческого возраста.
Клинически заболевание проявляет себя обструктивной и ирритативной симптоматикой. К симптомам первой группы (обструктивным) относятся затрудненное мочеиспускание, ощущение неполного опорожнения мочевого пузыря, несвоевременное начало акта мочеиспускания, натуживание во время мочеиспускания. К симптомам второй группы (ирритативным) — учащенное, императивное мочеиспускание, симптомы императивного недержания мочи. При переполненном мочевом пузыре может иметь место недержание мочи — так называемая парадоксальная ишурия. Осложнения клинического течения ДГПЖ характеризуются развитием инфекционно-воспалительных заболеваний мочевыводящих путей, формированием камней мочевого пузыря и почечной недостаточности, развитием острой и хронической задержки мочеиспускания, появлением макрогематурии (Л. М. Гориловский, 1999).
С целью стандартизации оценки жалоб больного при обследовании больных ДГПЖ применяются различные шкалы симптомов, наиболее широкое распространение из которых получила международная шкала симптомов при заболеваниях предстательной железы (I-PSS). Данная анкетная форма заполняется пациентом и содержит в себе семь вопросов, характеризующих различные аспекты нарушенного мочеиспускания, симптомы которого объективизируются, что особенно важно для пожилых больных со сниженными аналитическими способностями. Наибольшая сумма баллов, соответствующая в данной анкете крайне выраженной симптоматике нарушенного мочеиспускания, составляет 35. Сумма баллов от 0 до 7 характеризует больного со слабо выраженной симптоматикой ДГПЖ, от 8 до 19 баллов — с умеренно выраженной симптоматикой заболевания, и от 20 до 35 баллов — выраженной симптоматикой нарушенного мочеиспускания (В. Н. Степанов, 1999).
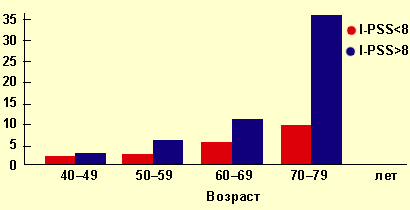
Следует отметить тот факт, что существует взаимосвязь между возрастом больных, симптомами ДГПЖ и развитием осложнений заболевания, которые диктуют необходимость госпитализации подобных пациентов и проведения у них оперативного лечения (см. рисунок 1).
Помимо оценки симптоматики заболевания в диагностическом процессе у больных ДГПЖ применяются пальцевое ректальное исследование, клиническое исследование мочи и биохимическое исследование крови, определение простато-специфического антигена (ПСА) сыворотки крови. Ультразвуковое исследование с определением размеров всей предстательной железы и ее переходной зоны, а также количества остаточной мочи может быть использовано в качестве неинвазивного скрининг-метода.
С помощью урофлоуметрии можно оценить зависимость объемной скорости потока мочи при мочеиспускании от времени. Максимальная скорость потока мочи менее 15 мл/с является показателем нарушенного мочеиспускания. Перечисленные методы высокоинформативны и могут многократно применяться у пациентов пожилого и старческого возраста с многочисленными сопутствующими заболеваниями.
Лечение больных ДГПЖ преследует следующие цели: уменьшение степени инфравезикальной обструкции, стихание симптоматики нарушенного мочеиспускания и улучшение качества жизни больных, снижение объема остаточной мочи, уменьшение риска развития острой задержки мочеиспускания и почечной недостаточности.
Абсолютными показаниями для лечения ДГПЖ являются выраженная клиническая симптоматика, значительно нарушающая качество жизни больного (суммарный балл симптомов по шкале I-PSS превышает 19), острая или хроническая задержка мочеиспускания, рецидивирующая макрогематурия, формирование почечной недостаточности и камней в мочевом пузыре, повторные инфекционно-воспалительные заболевания мочевыводящих путей.
Традиционно лечение ДГПЖ подразумевало выжидательную тактику, т. е. наблюдение, которое проводилось до тех пор, пока симптомы заболевания не оказывались настолько выраженными, что требовалось хирургическое вмешательство. Выжидательная тактика считалась допустимой в тех случаях, когда симптоматика не приводила к формированию выраженного дискомфорта или развитию осложнений ДГПЖ у больного. Стихание симптоматики заболевания и временное прекращение дальнейшего лечения становились возможны благодаря рекомендациям, подразумевающим некоторое изменение образа жизни больных. В частности, речь шла об ограничении употребления напитков, содержащих кофеин и алкоголь, контроле за опорожнением мочевого пузыря и некоторых других мероприятиях. Если возникает необходимость в выполнении хирургического вмешательства, то «золотым» стандартом считается трансуретральная резекция предстательной железы (ТУРП).
В ряде случаев также выполняются трансуретральное эндоскопическое рассечение предстательной железы и открытая аденомэктомия. В последние годы для применения в клинической практике стали доступны лекарственные способы лечения, которые в настоящее время наиболее широко распространены в лечении больных ДГПЖ (G. M. Clifford, 2000).
При выборе такого способа лечения большое значение имеет оценка симптоматики ДГПЖ. В случае слабо выраженной симптоматики заболевания (суммарный балл шкалы I-PSS превышает 8) возможно проведение динамического наблюдения. Чем более выраженной оказывается симптоматика ДГПЖ, тем более «активные» методы применяются при ее лечении (см. рисунок 2).
У больных с умеренно выраженной симптоматикой заболевания в настоящее время предпочтительнее проводить лекарственную терапию ДГПЖ. С этой целью применяются лекарственные препараты, относящиеся к трем группам, — это антагонисты α1-адренергических рецепторов, ингибиторы 5α1-редуктазы и экстракты растительного происхождения.
Препараты группы антагонистов α1-адренорецепторов воздействуют на динамический компонент инфравезикальной обструкции посредством расслабления гладкомышечных структур предстательной железы и шейки мочевого пузыря. Данные лекарственные средства, такие, как омник («Яманучи»), дальфаз СР («Санофи»), корнам (КРКА), кардура («Пфайзер»), сетегис («Эгис»), характеризуются быстрым началом лечебного действия.
В таблице 1 представлена характеристика клинической эффективности α1-адреноблокаторов (M. C. Beduschi, 1998; H. Lepor, 1998; C. G. Roehrborn, 1996).
Побочные действия антагонистов α1-адренорецепторов связаны с воздействием на α1-адренорецепторы кровеносных сосудов, что клинически выражается в снижении артериального давления и появлении симптоматики ортостатической гипотензии. Данных побочных эффектов лишен один из препаратов данной группы — тамсулозин, который обладает специфичностью в отношении подтипов α1a/d-адренорецепторов. Данный препарат особенно предпочтителен у больных пожилого и старческого возраста, страдающих интеркуррентными заболеваниями и принимающими иные лекарственные препараты. Тамсулозин, в дозировке 0,4 мг в сутки, не требует коррекции при проведении у больных одновременного лечения диуретиками, бета-блокаторами, ингибиторами ангиотензин-конвертирующего фермента и др.
Дополнительными побочными эффектами α-адреноблокаторов могут объясняться определенные преимущества, связанные с их применением у пожилых больных с ДГПЖ со множеством сопутствующих заболеваний. Так, гипотензивный эффект α-адреноблокаторов, благоприятное действие на углеводный обмен и липидный состав крови, отсутствие влияния на бронхиальную проходимость позволяют выбирать их для лечения ДГПЖ у больных с сопутствующей артериальной гипертонией, сахарным диабетом, гиперлипидемией, хроническими обструктивными заболеваниями легких. Наблюдения показывают, что при ДГПЖ с нормальным исходным АД адреноблокаторы не оказывают существенного антигипертензивного действия, что делает их пригодными для лечения ДГПЖ у больных как с повышенным, так и с нормальным АД. Вместе с тем, надо помнить о так называемом «эффекте первой дозы» — резком снижении АД, особенно в ортостатическом положении, возможности сильного головокружения и даже обморока. Подобный эффект чаще развивается при приеме празозина и менее характерен для доксазозина.
Ко второй группе лекарственных препаратов относится финастерид, являющийся ингибитором 5α-редуктазы. Финастерид обладает способностью снижать концентрацию дигидротестостерона путем подавления его образования из тестостерона. Клинические исследования позволили установить 60–70-процентное снижение концентрации дигидротестостерона, 25-процентное уменьшение размеров предстательной железы и сопутствующее уменьшение обструктивной симптоматики заболевания (на 25%), а также увеличение значения максимальной объемной скорости мочеиспускания (также на 25%) при терапии финастеридом, проводимой на протяжении двух и более лет (J. D. McConnell, 1998). Эффективность клинического действия финастерида зависит от размеров предстательной железы. Так, в частности, увеличение показателя максимальной объемной скорости мочеиспускания варьирует от 0,89 мл/с при размерах предстательной железы менее 20 см3 до 1,84 мл/с при размерах простаты свыше 60 см3. Эффективность действия препаратов, относящихся к категории антагонистов α1-адренорецепторов, не зависит от объема предстательной железы пациентов, страдающих от симптоматики ДГПЖ. Кроме этого, для достижения клинической эффективности финастерид необходимо принимать на протяжении по меньшей мере шести месяцев, что обусловлено гормональным механизмом его действия. К числу положительных аспектов применения финастерида относится его способность снижать риск возникновения острой задержки мочеиспускания у больных ДГПЖ (с 2,4/100 пациентов, страдающих ДГПЖ, в год до 0,93/100 пациентов в год). Финастерид снижает риск хирургического вмешательства на 55%, т. е. позволяет улучшить качество жизни больных без полостных или трансуретральных инвазивных вмешательств. К побочным эффектам финастерида относится снижение либидо и потенции, которые, однако, восстанавливаются после его отмены.
Среди лекарственных препаратов растительного происхождения ингибирующей активностью в отношении фермента 5a-редуктазы обладает экстракт американской вееролистной пальмы Serenoa repens пермиксон. Пермиксон подавляет процесс связывания дигидротестостерона с цитоплазматическими рецепторами и конкурирует с дигидротестостероном на уровне его связывания с внутриклеточными рецепторами. Действие пермиксона характеризуется также уменьшением образования простагландинов в ткани предстательной железы, что находит отражение в его противовоспалительном и противоотечном действии. Клиническое применение пермиксона в дозировке 320 мг в сутки на протяжении трех месяцев приводит к снижению выраженности симптоматики заболевания и увеличению значения максимальной объемной скорости мочеиспускания. Пермиксон хорошо переносится и, в отличие от финастерида, не влияет на половую активность.
К препаратам растительного происхождения относится таденан, который изготавливается на основе коры африканской сливы. Считается, что таденан подавляет избыточную пролиферацию фибробластов и оказывает противовоспалительное действие. На фоне применения таденана в суточной дозе 100 мг в течение трех месяцев отмечается улучшение мочеиспускания, устранение никтурии, усиление струи мочи. Потенция и либидо не нарушаются.
На протяжении последнего десятилетия динамично развиваются новые технологические способы лечения ДГПЖ. По эффективности своего действия и инвазивности они занимают промежуточное положение между лекарственными и хирургическими методами лечения. К данной группе относятся микроволновая термотерапия, трансуретральная игольчатая аблация предстательной железы, интерстициальная лазерная коагуляция простаты, установка простатических стентов и др. Меньшая травматичность и большая безопасность применения данных методов, по сравнению с традиционными оперативными способами удаления гиперплазированной части предстательной железы (открытая аденомэктомия, ТУРП), делают их использование предпочтительным у лиц пожилого и старческого возраста в тех случаях, когда лекарственная терапия оказывается неэффективной и существуют противопоказания к оперативному вмешательству.
Л. М. Гориловский, доктор медицинских наук, профессор
М. Зингеренко, кандидат медицинских наук
РМАПО, г. Москва
Приложения
-
- Доброкачественная гиперплазия предстательной железы - Рисунок 1.
Частота развития острой задержки мочеиспускания в зависимости от симптоматики ДГПЖ и возраста больных.
-
- Доброкачественная гиперплазия предстательной железы - Рисунок 2.
Распространенность основных методов лечения ДГПЖ (в %) в зависимости от симптоматики заболевания.
-
- Доброкачественная гиперплазия предстательной железы - Таблица 1.
Эффективность α1-адреноблокаторов, применяющихся в клинической практике для лечения больных ДГПЖ.