Инфекционные заболевания верхних дыхательных путей, к числу которых относятся и ринофарингиты, являются одной из самых частых причин обращения к врачу [3]. Развивающийся комплекс симптомов: насморк, заложенность носа, головная боль, температура, боль в горле, затрудненное дыхание и болезненный кашель, — ведет к потере работоспособности, обострению хронических заболеваний, существенно снижает качество жизни человека. К сожалению, многие больные пытаются заниматься самолечением, которое помимо средств так называемой народной медицины обычно включает применение сосудосуживающих капель в нос, антипиретиков, анальгетиков, а также витаминов. Результаты подобного лечения нередко носят неубедительный характер, о чем свидетельствует укоренившееся представление о том, что «если насморк лечить, то он проходит за 14 дней, а если не лечить, то за две недели».
Однако углубление наших представлений о природе и механизмах проникновения патогенов, ключевых моментах воспалительного процесса в верхних дыхательных путях и особенностях иммунных реакций слизистых оболочек, вероятно, дают основание для более оптимистичного взгляда на перспективы профилактики и лечения ринофарингитов. Это особенно актуально в связи с тем, что в последние годы за счет изменения свойств патогенных микроорганизмов ринофарингиты из сезонных заболеваний осенне-зимнего периода фактически стали круглогодичными [1, 2, 10].
По данным как отечественных, так и зарубежных исследователей, к числу главных патогенов, вызывающих развитие ринофарингитов, относятся Staphylococcus aureus, Haemophilus influenzae, различные штаммы Streptococcus pneumoniae, а также Klebsiella sp., Moraxella sp. и Neisseria sp., на долю которых приходится не менее 80% всех случаев заболевания. Усиление их патогенных свойств и всесезонность заболеваемости стали следствием их собственной эволюции, загрязнения окружающей среды, широкого и далеко не всегда оправданного использования антибиотиков. Поэтому основная нагрузка в борьбе с этими и другими возбудителями ложится на факторы неспецифической резистентности и иммунитета, особенно на уровне слизистой оболочки верхних дыхательных путей, принимающей на себя первый, самый мощный удар патогенов [5, 7, 10].
Неспецифическая защита верхних дыхательных путей осуществляется фагоцитирующими клетками слизистой оболочки, выходящими на ее поверхность или расположенными в ее основе, и антимикробными факторами, содержащимися в слое слизи, выстилающем всю поверхность дыхательных путей. К числу этих факторов относятся лизоцим, опсонины, обеспечивающие усиление фагоцитоза, а также компоненты каскада комплемента, которые сами по себе или после взаимодействия с молекулами антител обеспечивают высокоэффективный бактериолизис. Еще одним важным фактором неспецифической защиты является мукоцилиарный клиренс, т. е. постоянный ток слизи, покрывающей поверхность клеток эпителия. Этот ток создается за счет работы микроресничек клеток эпителия, выстилающих верхние дыхательные пути. Вместе со слизью с поверхности эпителия удаляется значительная часть бактерий и вирусов, пытающихся колонизировать ее [10].
Однако главным недостатком факторов неспецифической защиты является идентичность их действия в отношении всех патогенов, в свою очередь сильно различающихся по биологическим свойствам. Поэтому главная роль в защите слизистых оболочек от инфекции принадлежит иммунным механизмам, среди которых особого упоминания заслуживает секреторная форма иммуноглобулина А (sIgA). Важными отличительными чертами этой молекулы являются, с одной стороны, высокая специфичность действия, т. е. нацеленность на конкретный патоген, а с другой — устойчивость к действию агрессивных факторов окружающей среды и микробных ферментов. Кроме того, sIgA образуется в ответ на инфекцию главным образом в самой слизистой оболочке, поэтому его концентрация значительно возрастает, а действие становится высокоэффективным; sIgA связывается с бактериальными и вирусными патогенами и блокирует возможность их адгезии к клеткам эпителия, предотвращая начало инфекционного процесса. Нейтрализованные sIgA патогены легко удаляются за счет мукоцилиарного клиренса. Поэтому формирование защитной пленки из sIgA на поверхности клеток эпителия важно как с точки зрения обеспечения защиты в ходе патологического процесса, так и с точки зрения профилактики инфекций, ибо молекулы sIgA, направленные против конкретного микроба, сохраняются в составе слизистого секрета до 6 месяцев [4, 8].
С учетом иммунологических аспектов функционирования слизистой оболочки верхних дыхательных путей препарат ИРС19 является необходимым средством профилактики и лечения острых респираторных инфекций, в том числе ринофарингитов. Действуя на лимфоциты слизистой оболочки носа, ИРС19 заставляет их формировать огромное количество секреторного IgA, направленного против всех возбудителей, компоненты которых входят в состав препарата. Поэтому профилактическое действие ИРС19 общепризнанно, оно носит строго антигенспецифический характер.
ИРС19 высокоэффективен в лечении острых ринофарингитов, вызываемых не только возбудителями, входящими в его состав, но и другими. Это подтверждено многочисленными исследованиями отечественных и зарубежных отоларингологов и иммунологов. Каков механизм действия ИРС19 в этом случае?
Объяснение этого феномена имеет чисто иммунологический характер. ИРС19 воздействует на общие этапы регуляции любого иммунного ответа слизистых оболочек, поэтому усиление синтеза sIgA на фоне применения ИРС19 при остром заболевании происходит независимо от того, входят компоненты патогена в состав препарата или нет. В любом случае результатом становятся существенное ускорение иммунного ответа и восстановление утраченной при инфицировании защитной пленки из sIgA на поверхности клеток эпителия. Более того, ИРС19 стимулирует фагоциты слизистой оболочки к усиленному фагоцитозу бактерий, повышает концентрацию факторов неспецифической защиты (опсонинов, комплемента и лизоцима) в составе слизи и даже, за счет стимуляции клеток иммунной системы, повышает местный синтез интерферонов, защищающих клетки от вирусов. Именно поэтому применение ИРС19 в терапии острых ринофарингитов опровергает распространенную точку зрения об обязательности затяжного характера насморка. Следует принять во внимание и длительность профилактического действия ИРС19 (одного двух-трехнедельного профилактического курса препарата достаточно для повышения защищенности слизистой оболочки верхних дыхательных путей на 4–6 месяцев [4, 5, 9].
Результаты исследования, проведенного нами на базе Санкт-Петербургского НИИ уха, горла, носа и речи МЗ РФ и поликлиники № 38 Санкт-Петербурга, еще раз подтвердили высокую эффективность ИРС19 в лечении ринофарингитов [4]. В табл. 1 приведены наиболее существенные показатели обследованных больных до их разделения на подгруппы ИРС19 и контрольную. В среднем пациенты обращались к врачу через два дня после начала заболевания (сроки варьировали до четырех суток). В большинстве случаев причиной ринофарингита была острая респираторная вирусная инфекция, хотя у пятой части заболевших имела место выраженная инфекция бактериальной этиологии, а в 8,3% случаев процесс сопровождался обострением хронического тонзиллита.
Показатели температуры тела и СОЭ у больных обеих групп в период наблюдения в целом незначительно отличались от нормальных. Показатель СОЭ ни у одного больного не превышал 10 мм/ч как в группе ИРС19, так и в контрольной.
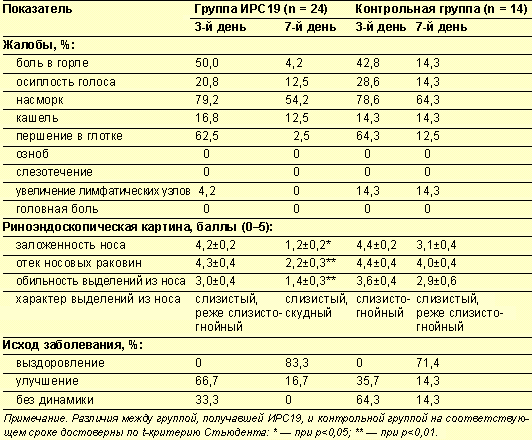
Через семь дней амбулаторного лечения отмечено достоверное снижение числа жалоб как в группе ИРС19, так и в контрольной группе, а исчезновение озноба, слезотечения, головных болей в обеих группах отмечено уже на третий день. Динамика клинических показателей приведена в табл. 2. Из приведенных данных следует, что преимущества применения ИРС19 становятся достоверно заметными в период с третьих по седьмые сутки, при этом они касаются как субъективных, так и объективных критериев. При интраназальном применении ИРС19, помимо существенного сокращения объема и улучшения характера выделений из носа, отмечено практически полное исчезновение болей (на седьмые сутки они сохранялись лишь у одного пациента из 24) и першения в горле, а также уменьшение размеров увеличенных лимфатических узлов.
Достоверное преимущество применения ИРС19 установлено по объективным критериям риноэндоскопической картины, т. е. заложенности носа, степени отека носовых раковин, количеству и характеру выделений из носа. При анализе исхода заболевания установлено, что в группе ИРС19 улучшение после семи дней применения препарата отмечено в 100% случаев, полное выздоровление наблюдалось у 20 больных из 24 (83,3%). Для сравнения: в контрольной группе улучшение отмечено в 85,7% случаев, в том числе полное выздоровление — в 71,4% наблюдений.
Один из крупнейших австрийских микробиологов профессор Рёттинг еще в 1979 г. писал, говоря о препарате ИРС19, что важные с практической точки зрения преимущества местной иммунизации ИРС19 заключаются в быстром наступлении действия и полной безвредности [11]. Прошедшие годы полностью подтвердили справедливость этих слов и доказали высокую клиническую эффективность и иммунологическую обоснованность применения препарата ИРС19.
Литература
1. Богомильский М. Р., Маркова Т. П., Гаращенко Т. И., Чувиров Д. Г., Ягольникова О. В., Радциг Е. Ю., Стребкова О. А., Сквира И. Е. Клинико-иммунологическое обоснование применения топического бактериального иммунокорректора ИРС19 для профилактики заболеваний верхних дыхательных путей у детей // Детский доктор. 2000. № 4. С.16-20.
2. Кладова О. В., Харламова Ф. С., Щербакова А. А., Легкова Т. П., Знаменская А. А., Учайкин В. Ф. Результаты применения интраназальной вакцины (бактериального лизата) ИРС19 у часто болеющих детей с синдромом крупа и другими поражениями бронхолегочной системы // Детский доктор /Спецвыпуск. 2001. № 4.
3. Лучихин Л. А., Белякова Л. В., Гуров А. В. Профилактика и лечение воспалительных заболеваний верхних дыхательных путей препаратами ИРС19 // Вестник оториноларингологии. 2000. № 4. С. 54-56.
4. Полевщиков А. В., Рязанцев С. В., Хлебникова Н. А. Оценка клинической эффективности препарата ИРС19 при лечении острых ринофарингитов // Новости оториноларингологии и логопатологии. 2000. № 3(23). С. 231-234.
5. Ярилин А. А. Основы иммунологии. М.: Медицина, 1999. 720 с.
6. Brandtzaeg P., Jahnsen F.L., Farstad I.N., Haraldsen G. Mucosal immunology of the upper airways: an overwiev // Annals NY Acad. Sci. 1997. Vol. 830. P. 1-18.
7. Clavel R., Bamier F., Bouin P. ИРС-19: исследование двойным слепым перекрестным методом // Детский доктор. 2000. № 1. С. 25-27.
8. Januway Ch., Travers P., Walport M., Capra J. D. Immunobiology: the immune system in health and disease. 4th ed. Current Biology Ltd. 1999. 740 pp.
9. MacKay C. R. Immunological memory // Adv. Immunol. 1993. Vol. 53. P. 217-265.
10. Martin L. D., Rochelle L. G., Fisher B. M. et al. Airway epithelium as an effector of imflammation: molecular regulation of secondary mediators // Eur. Respir. J. 1997. Vol. 10. P. 2139-2146.
11. Raetting H. Tierexperimente zur kombinierten, lokalen Immunisierung gegen eine Influenzavirus-Erkrankung // Wien. klin. Wschr. 1979. Vol. 91. P. 13-18.
Приложения
-
- Преимущества местной иммунотерапии в лечении и профилактике ринофарингитов - Таблица 2.
Оценка клинического состояния больных острыми ринофарингитами через 3 и 7 суток после начала применения ИРС19
-
- Преимущества местной иммунотерапии в лечении и профилактике ринофарингитов - Таблица 1.
Оценка клинического состояния больных острыми ринофарингитами до начала лечения (n = 40 человек)