Резюме
Цель работы. Данная статья освещает наиболее важные вопросы питания пациентов с IgA-нефропатией, ассоциированной с высоким титром целиакийных антител в крови. Подчеркивается значимость лечебного питания, входящего в состав нефропротективной стратегии как неотъемлемой части терапии пациентов нефрологического профиля. Выход отдельных клинических практических рекомендаций KDOQI (2020 г.) еще раз подчеркнул большое значение немедикаментозного воздействия для эффективной терапии заболеваний почек различной этиологии.
Цель работы. Адаптация лечебного питания как компонента нефропротективной стратегии для больных IgA-нефропатией, ассоциированной с высоким титром целиакийных антител в крови.
Результаты. На основании убедительных данных мировой литературы, которые согласуются с результатами собственных исследований, подтверждающих ассоциацию вышеуказанных состояний (даже в отсутствие клинических проявлений энтеропатии), эффективности аглютеновой диеты в комплексном лечении IgA-нефропатии, – адаптирован лечебный рацион для данной категории больных по необходимому химическому составу и энергетической ценности.
Заключение. Модификация питания является важнейшим элементом комплексной терапии пациентов нефрологического профиля. Индивидуальный подход к подбору диетотерапии, в том числе элиминации глютена, позволит не только снизить иммунологическую активность основного гломерулярного заболевания, но и, возможно, замедлит скорость прогрессирования хронической болезни почек, отсрочив развитие терминальной почечной недостаточности и повысив резервные возможности почек.
Конфликт интересов. Авторы статьи подтвердили отсутствие конфликта интересов, о котором необходимо сообщить.
Диета – неотъемлемая часть процесса профилактики и лечения хронических заболеваний, в том числе патологии нефрологического профиля. В вышедших отдельных клинических практических рекомендациях по питанию при хронической болезни почек (ХБП) KDOQI (2020 г.) подчеркивается большое значение немедикаментозного воздействия для эффективной терапии этого заболевания [1]. В зависимости от этиологии и клинических проявлений ХБП подходы, в том числе к немедикаментозной терапии, могут отличаться [2].
Хронические заболевания почек в зависимости от стадии ХБП требуют не только оптимального потребления пациентом белка, но и основных макро- и микронутриентов, избыток которых может влиять как на неиммунные, так и на иммунные механизмы повреждения гломерулярного аппарата, приводя к прогрессированию основного почечного заболевания [3]. Кроме того, при составлении лечебного питания необходимо учитывать нутриционный статус, нарушения липидного, водно-электролитного и фосфорно-кальциевого обменов, которые могут наблюдаться у пациентов с ХБП [1].
В оптимизации пищевого рациона нуждаются пациенты с ХБП и некоторыми сопутствующими заболеваниями, где диетотерапия выступает как основной метод лечения. В такой ситуации особого внимания требуют больные с ХБП, обусловленной IgA-нефропатией (ИГАН) в сочетании с целиакией (ЦК) или изолированно высоким уровнем целиакийных антител (ЦАТ) в крови без явных признаков энтеропатии, когда элиминация глютена положительно влияет в том числе на клиническое течение гломерулярного заболевания [4, 5]. Принимая во внимание тот факт, что ряд авторов [6-8] продолжает изучать возможную роль глютена не только в патогенезе ЦК, но и в развитии и/или усугублении течения ИГАН, целью настоящей работы стала попытка адаптировать рекомендации по питанию для данной категории пациентов.
IGA-НЕФРОПАТИЯ И ХБП. РЕКОМЕНДАЦИИ ПО ПИТАНИЮ
Коррекция образа жизни и особенностей питания с целью воздействия на модифицируемые факторы риска развития и прогрессирования ХБП являются значимыми направлениями профилактики и лечения [1]. Коррекции питания на стадиях ХБП С1-С2 практически не требуется, в то время как на стадиях С3а-С5, напротив, необходимы определенные ограничения.
ПОТРЕБЛЕНИЕ БЕЛКА И ЭНЕРГИИ
В организме человека ежедневно метаболизируется примерно 250,0 г белка, что приводит к образованию продуктов белкового распада (мочевина, аммиак и др.), которые, как правило, выводятся из организма почками с мочой [9]. При снижении скорости клубочковой фильтрации потребляемый белок может создавать дополнительную нагрузку на почки, а ответная гиперфильтрация, связанная с его потреблением, – играть деструктивную роль в их функционировании [9]. Таким образом, в ситуации сокращения числа действующих нефронов уменьшение количества белка в рационе снижает гиперфильтрацию, защищает клубочки почек от ускоренного гиалиноза и уменьшает выраженность протеинурии [9]. Кроме того, адекватное потребление белка приводит к снижению уремии и улучшению почечной гемодинамики, что может уменьшить выраженность клинических симптомов и отсрочить необходимость начала заместительной почечной терапии [1].
Выделяют малобелковую диету, при которой количество потребляемого белка составляет 0,55-0,6 г на кг массы тела в сутки (г/кг/сут) и строгую малобелковую диету, когда количество потребляемого белка составляет 0,28-0,43 г/кг/сут [1]. Для обеспечения потребностей в белке 0,55-0,6 г/кг/сут малобелковую диету рекомендовано соблюдать в сочетании с применением кетоаналогов аминокислот [1]. Для адекватного контроля гликемии и стабильного нутриционного статуса пациентам с ХБП С3а-С5 и сахарным диабетом рекомендовано потребление белка в количестве 0,6-0,8 г/кг/сут [1].
Для профилактики белково-энергетической недостаточности необходимо потребление достаточного количества энергии. С учетом возраста, пола, уровня физической активности, целевой массы тела, стадии ХБП, сопутствующих заболеваний или наличия воспаления для поддержания адекватного нутриционного статуса и нейтрального азотистого баланса рекомендовано получать энергию из расчета 25-35 ккал/кг массы тела в день [10].
ПОТРЕБЛЕНИЕ КАЛЬЦИЯ И ФОСФОРА
Как правило, концентрация кальция в сыворотке крови сохраняется нормальной (2,1-2,55 ммоль/л) до поздних стадий ХБП [11]. Избыток кальция может способствовать внекостной кальцификации, что повышает риск сердечно-сосудистых заболеваний и, напротив, его дефицит при снижении всасывания кальция в кишечнике может приводить к развитию минерально-костных нарушений [12]. Таким образом, для поддержания нейтрального баланса кальция его суточное потребление, в том числе в составе продуктов питания и лекарственных препаратов, должно составлять 800-1000 мг/день [1].
Ограничения фосфора с пищей у пациентов с ХБП четко не установлены. Для поддержания нормального уровня фосфора (0,81-1,45 ммоль/л) необходимо учитывать его биодоступность в различных источниках (животной и растительной пище, в составе биодобавок). Обычно количество допустимого фосфора составляет 800-1000 мг/день [1].
ПОТРЕБЛЕНИЕ КАЛИЯ И НАТРИЯ
Рабочая группа Национальной ассоциации нефрологов рекомендует на ранних стадиях ХБП ограничить потребление калия уровнем, свойственным здоровым лицам, – 4-5 г/сутки, с рекомендациями более жесткого конт-роля калия на поздних стадиях ХБП (2-3 г/сут) для предупреждения гиперкалиемии и редукции риска смерти [13].
Для улучшения волемического статуса, снижения артериального давления и протеинурии в сочетании с медикаментозной терапией пациентам с ХБП рекомендовано ограничить потребление натрия до уровня менее 100 ммоль/сут, или 2,3 г/сут [1].
ЦЕЛИАКИЯ. РЕКОМЕНДАЦИИ ПО ПИТАНИЮ
В основе элиминационной диеты лежит полное исключение из рациона питания продуктов, содержащих глютен или его следы [14]. Так, прием даже 100 мг глютена может спровоцировать атрофию ворсин кишечника, что может привести к рецидиву заболевания [15]. Международными организациями установлено предельно допустимое содержание глютена в безглютеновых продуктах – менее 20 ppm (20 мг/кг готового продукта) [16].
Аглютеновая диета (АГД) является полноценной по основным макро- и микронутриентам, механически и химически щадящей, с повышенным содержанием белка, кальция и несколько увеличенной энергетической ценностью [17]. Способ приготовления зависит от функционального состояния кишечника. Так, в период неустойчивого стула пища измельчается или протирается, а при нормализации стула не требует специальной обработки [17].
Рекомендованный химический состав и энергоценность АГД: белки – 100-120 г, жиры – 100-110 г, углеводы – 400-450 г, калорийность – 2940-3270 ккал, поваренная соль – 6-7 г, свободная жидкость – 1,5 л [17]. Состав рациона зависит от возраста, тяжести и периода заболевания и строится на основании общих принципов: углеводный компонент – за счет переносимых круп, бобовых, фруктов и овощей; белковый и жировой – за счет мяса, птицы, рыбы, молочных продуктов, растительных и сливочного масел [17]. На рисунке приведен список разрешенных и запрещенных продуктов в составе АГД.
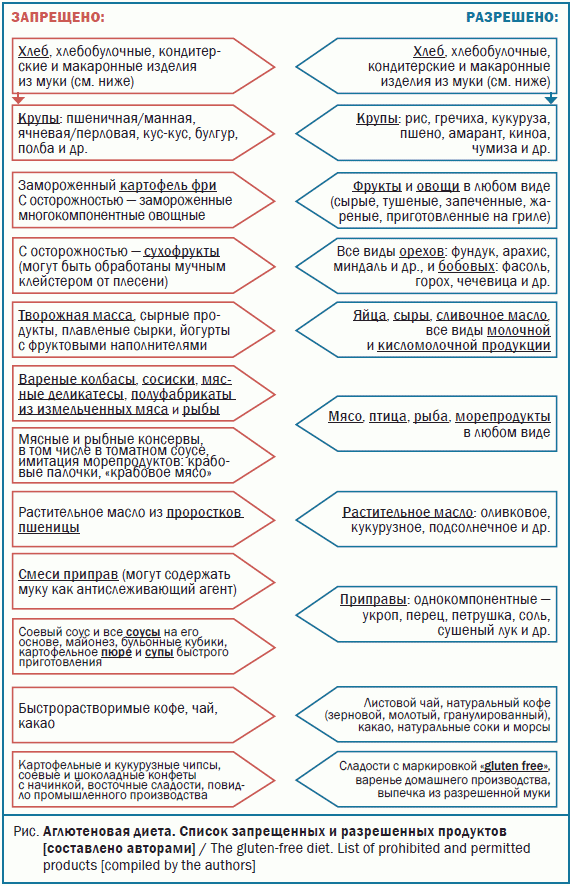
Важным аспектом лечебного питания является полный отказ от продуктов, содержащих не только явный, но и скрытый глютен, который используют производители в качестве добавки [18]. Таким образом, при выборе продуктов необходимо тщательно изучать состав на упаковке. Как правило, продукты без глютена промаркированы «gluten free» (без глютена) или на этикетке размещен знак в виде перечеркнутого колоса с регистрационным номером. Перечень всех продуктов со значком российских производителей можно найти в свободном доступе в сети Интернет на сайте
IGA-НЕФРОПАТИЯ В СОЧЕТАНИИ С ЦЕЛИАКИЙНЫМИ АНТИТЕЛАМИ В КРОВИ. РЕКОМЕНДАЦИИ ПО ПИТАНИЮ
В основе АГД лежит элиминация глютена из рациона, не требующая, как правило, ограничений по основным макро- и микронутриентам. Принимая во внимание, что АГД является высокобелковой с повышенной энергоценностью, для данной категории больных количество белка и энергии необходимо учитывать исходя из стадии ХБП. Кроме того, по мере прогрессирования ИГАН необходима коррекция рациона с ограничением кальция, фосфора и калия (см. табл.)
ЗАКЛЮЧЕНИЕ
Таким образом, модификация питания совместно с медикаментозным лечением является важнейшим элементом комплексной терапии пациентов нефрологического профиля. Индивидуальный подход к подбору диетотерапии, составленной согласно необходимому химическому составу, энергетической ценности и перечню разрешенных продуктов, позволит не только снизить иммунологическую активность основного гломерулярного заболевания, но и, возможно, замедлит скорость прогрессирования ХБП, отсрочив развитие терминальной почечной недостаточности и повысив резервные возможности почек.
Вклад авторов.
Авторы внесли равный вклад на всех этапах работы и написания статьи.
Authors’ contribution.
All authors contributed equally to this work and writing of the article at all stages.
Литература/References
- Икизлер Т. А., Берроуз Д. Д., Байхем-Грей Л. Д. и др. Клинические практические рекомендации по питанию при ХБП KDOQI: в редакции 2020 г. Нефрология и диализ. 2022; 24 (2): 143-278. DOI: 10.28996/2618-9801-2022-2-143-278. [Ikizler T. A., Burroughs D. D., Bayhem-Gray L. D., etc. Clinical practical recommendations on nutrition in CKD KDOQI: as amended in 2020. Nefrologiya i dializ. 2022; 24 (2): 143-278. DOI: 10.28996/2618-9801-2022-2-143-278. (In Russ.)]
- Боровик Т. Э. и др. Диетотерапия при заболеваниях почек у детей. Вопросы питания. 2016; 85 (2): 67-83. [Borovik T. E., et al. Diet therapy for kidney diseases in children. Voprosy pitaniya. 2016; 85 (2): 67-83. (In Russ.)]
- Халфина Т. Н., Нуруллина Г. И., Фахрутдинова О. Ю. Особенности лечебного питания при гломерулонефритах (обзор литературы). Практическая медицина. 2021; 19 (4): 20-25. [Khalfina T. N., Nurullina G. I., Fakhrutdinova O. Yu. Features of therapeutic nutrition in glomerulonephritis (literature review). Prakticheskaya meditsina. 2021; 19 (4): 20-25. (In Russ.)]
- Манцаева М. Е., Борисов А. Г., Смирнова М. А., Стремоухов А. А. Эффективность безглютеновой диеты у пациентов с IgA-нефропатией. Лечащий Врач. 2023; 26 (3): 43-47. DOI: 10.51793/OS.2023.26.3.007. [Mantsaeva M. E., Borisov A. G., Smirnova M. A., Stremoukhov A. A. The effectiveness of a gluten-free diet in patients with IgA nephropathy. Lechaschi Vrach. 2023; 26 (3): 43-47. DOI: 10.51793/OS.2023.26.3.007. (In Russ.)]
- Coppo R. The Gut-Renal Connection in IgA Nephropathy. Seminars in Nephrology. 2018; 5 (38): 504-512.
- Papista C., et al. Gluten exacerbates IgA nephropathy in humanized mice through gliadin-CD89 interaction. Kidney International. 2015; 2 (88): 276-285. DOI: 10.1038/ki.2015.94.
- Habura I., et al. IgA nephropathy associated with coeliac disease. Central European Journal of Immunology. 2019; 1 (44): 106-108. DOI: 10.5114/ceji.2019.84021.
- Манцаева М. Е., Борисов А. Г., Стремоухов А. А. Клиническое наблюдение: в фокусе IgA-нефропатия, ассоциированная с нарушением обмена глютена. Лечащий Врач. 2021; 24 (5): 57-61. DOI: 10.51793/OS.2021.54.20.012. [Mantsaeva M. E., Borisov A. G., Stremoukhov A. A. Clinical observation: IgA-nephropathy associated with impaired gluten metabolism is in focus. Lechaschi Vrach. 2021; 24 (5): 57-61. DOI: 10.51793/OS.2021.54.20.012. (In Russ.)]
- Kalantar-Zadeh D., Fouque K. Nutritional management of chronic kidney disease. N Engl J Med. 2017; 377 (18): 1765-1776. DOI: 10.1056/NEJMra1700312.
- Fouque D., et al. EBPG guideline on nutrition. Nephrol Dial Transplant. 2007; 22 (2): 45-87.
- Levin A., et al. Prevalence of abnormal serum vitamin D, PTH, calcium, and phosphorus in patients with chronic kidney disease: results of the study to evaluate early kidney disease. Kidney Int. 2007; 71 (1): 31-38.
- Sigrist M. K., et al. Progressive vascular calcifi cation over 2 years is associated with arterial stiffening and increased mortality in patients with stages 4 and 5 chronic kidney disease. Clin J Am Soc Nephrol. 2007; 2 (6): 1241-1248.
- Клинические рекомендации. Хроническая болезнь почек (ХБП). Нефрология. 2021; 25 (5): 10-82. [Clinical recommendations. Chronic kidney disease (CKD). Nephrology. 2021; 25 (5): 10-82. (In Russ.)]
- Рославцева Е. А, Дмитриева Ю. А, Захарова И. Н. и др. Целиакия у детей: проект клинических рекомендаций. Экспериментальная и клиническая гастроэнтерология. 2021; 4 (188): 199-227. DOI: 10.31146/1682-8658-ecg-188-4-199-227. [Roslavtseva E. A., Dmitrieva Yu. A., Zakharova I. N., et al. Celiac disease in children: draft clinical recommendations. Eksperimentalnaya i klinicheskaya gastroenterologiya. 2021; 4 (188): 199-227. DOI: 10.31146/1682-8658-ecg-188-4-199-227. (In Russ.)]
- Ревнова М. О. Целиакия у детей – новый взгляд на старую проблему. РМЖ. 2008; 16 (18): 1209-1212. [Revnova M. O. Celiac disease in children – a new look at an old problem. RMZh. 2008; 16 (18): 1209-1212. (In Russ.)]
- Standard for foods for special dietary use for persons intolerant to gluten https://www.wheatfree.org/documents/Gluten%20Codex%20Alimentarius%20CXS_118e_2015.pdf (Accessed: 15.09.2023)
- Преображенская Э. Н. Диета при целиакии. Практическая диетология. 2014; 11 (3). [Preobrazhenskaya E. N. Diet with celiac disease. Prakticheskaya dietologiya. 2014; 11 (3). (In Russ.)]
- Парфенов А. И. и др. Всероссийский консенсус по диагностике и лечению целиакии у детей и взрослых. Терапевтический архив. 2017; 89 (3): 94-107. DOI: 10.17116/terarkh201789394-107. [Parfenov A. I., et al. All-Russian consensus on the diagnosis and treatment of celiac disease in children and adults. Terapevticheskii arkhiv. 2017; 89 (3): 94-107. DOI: 10.17116/terarkh201789394-107. (In Russ.)]
А. Г. Борисов2, 3, https://orcid.org/0000-0001-7063-6563, bag22@rambler.ru
С. В. Чернавский2, 4, chernavskijsv@mail.ru
А. А. Стремоухов5, https://orcid.org/0000-0002-4393-3543, astremo@bk.ru
1 Отраслевой клинико-диагностический центр Публичного акционерного общества «Газпром»; 117420, Россия, Москва, ул. Наметкина, 16
2 Федеральное государственное бюджетное образовательное учреждение дополнительного профессионального образования Российская медицинская академия непрерывного профессионального образования Министерства здравоохранения Российской Федерации; 125993, Россия, Москва, ул. Баррикадная, 2/1, стр. 1
3 Государственное бюджетное учреждение здравоохранения Городская поликлиника № 11 Департамента здравоохранения города Москвы; 119331, Россия, Москва, ул. Кравченко, 14
4 Федеральное государственное бюджетное учреждение Главный военный клинический госпиталь имени академика Н. Н. Бурденко Министерства обороны Российской Федерации; 105094, Россия, Москва, Госпитальная пл., 3
5 Некоммерческая организация Ассоциация врачей первичного звена СИРАНО; 117587, Россия, Москва, Варшавское шоссе, 125Ж, корп. 6
Сведения об авторах:
Манцаева Мария Евгеньевна, нефролог Отраслевого клинико-диагностического центра Публичного акционерного общества «Газпром»; 117420, Россия, Москва, ул. Наметкина, 16;
Борисов Алексей Геннадьевич, к.м.н., доцент кафедры общей врачебной практики и поликлинической терапии Федерального государственного бюджетного образовательного учреждения дополнительного профессионального образования Российская медицинская академия непрерывного профессионального образования Министерства здравоохранения Российской Федерации; 125993, Россия, Москва, ул. Баррикадная, 2/1, стр. 1; главный врач Государственного бюджетного учреждения здравоохранения Городская поликлиника № 11 Департамента здравоохранения города Москвы; 119331, Россия, Москва, ул. Кравченко, 14; bag22@rambler.ru
Чернавский Сергей Вячеславович, д.м.н., доцент кафедры общей врачебной практики и поликлинической терапии Федерального государственного бюджетного образовательного учреждения дополнительного профессионального образования Российская медицинская академия непрерывного профессионального образования Министерства здравоохранения Российской Федерации; 125993, Россия, Москва, ул. Баррикадная, 2/1, стр. 1; заведующий эндокринологическим отделением Федерального государственного бюджетного учреждения Главный военный клинический госпиталь имени академика Н. Н. Бурденко Министерства обороны Российской Федерации; 105094, Россия, Москва, Госпитальная пл., 3; chernavskijsv@mail.ru
Стремоухов Анатолий Анатольевич, д.м.н., профессор, директор института профессионального образования Некоммерческой организации Ассоциация врачей первичного звена СИРАНО; 117587, Россия, Москва, Варшавское шоссе, 125Ж, корп. 6;
Information about the authors:
Mariya E. Mantsaeva, nephrologist of the Branch Clinical and Diagnostic Center of Gazprom Public Joint Stock Company; 16 Nametkina str., Moscow, 117420, Russia; 79054341140@yandex.ru
Alexey G. Borisov, Cand. of Sci. (Med.), Associate Professor of the Department of General Medical Practice and Polyclinic Therapy at the Federal State Budgetary Educational Institution of Additional Professional Education Russian Medical Academy of Continuous Professional Education of the Ministry of Health of the Russian Federation; 2/1 b.1 Barricadnaya str., Moscow, 125993, Russia; Chief physician of the State Budgetary Healthcare Institution City Polyclinic No. 11 of the Moscow Department of Health; 14 Kravchenko str., Moscow, 119331, Russia; bag22@rambler.ru
Sergey V. Chernavsky, Dr. of Sci. (Med.), Associate Professor of the Department of General Medical Practice and Polyclinic Therapy at the Federal State Budgetary Educational Institution of Additional Professional Education Russian Medical Academy of Continuous Professional Education of the Ministry of Health of the Russian Federation; 2/1 b.1 Barricadnaya str., Moscow, 125993, Russia; Head of the Endocrinology Department at the Federal State Budgetary Institution The Main Military Clinical Hospital named after Academician N. N. Burdenko of the Ministry of Defense of the Russian Federation; 3 Hospital Square, Moscow, 105094, Russia;
Anatoly A. Stremoukhov, Dr. of Sci. (Med.), Professor, Director of the Institute of Professional Education at the Non-profit organization Association of Primary Care Physicians SIRANO; 125ZH, bldg. 6 Varshavskoe shosse, Moscow, 117587, Russia; astremo@bk.ru
Особенности рациона питания у пациентов с IgA-нефропатией и целиакийными антителами в крови/ М. Е. Манцаева, А. Г. Борисов, С. В. Чернавский, А. А. Стремоухов
Для цитирования: Манцаева М. Е., Борисов А. Г., Чернавский С. В., Стремоухов А. А. Особенности рациона питания у пациентов с IgA-нефропатией и целиакийными антителами в крови. Лечащий Врач. 2024; 2 (27): 43-47. https://doi.org/010.51793/OS.2024.27.2.008
Теги: почки, нефропатия, лечебное питание, нефропротективная стратегия
Купить номер с этой статьей в pdf