Желчнокаменная болезнь относится к числу наиболее распространенных заболеваний. По данным бюро медицинской статистики Москвы, количество больных желчнокаменной болезнью на 100 000 жителей за последние 10 лет увеличилось почти в 1,5 раза. Ежегодно возрастает число нуждающихся в хирургическом лечении [4, 8]. Внедрение в практику современных миниинвазивных технологий несколько снизило процент послеоперационных осложнений и летальных исходов, но кардинально не решило проблему [1, 6]. Желчнокаменная болезнь нередко существует или развивается на фоне других заболеваний пищеварительного тракта, например гепатита, панкреатита, заболеваний желудка и двенадцатиперстной кишки и др. [2, 7]. Этому способствуют тесные анатомо-функциональные связи органов гастрогепатопанкреатодуоденальной зоны. В послеоперационном периоде существует реальная угроза обострения билиарного панкреатита и гепатита, развития холангита и других осложнений. Известно, что 60% больных после холецистэктомии предъявляют жалобы на боли в эпигастрии и диспепсию. В литературе нет единого мнения об их причинах. Большое значение в восстановлении после операций имеет реабилитация, единая методика которой отсутствует и которая оценивается по-разному [9]. Необходимы дальнейшее внедрение и усовершенствование малоинвазивных методов диагностики и хирургического лечения холелитиаза, формирование новых технологических подходов в прогнозировании и профилактике интра- и послеоперационных специфических и неспецифических осложнений, особенно у групп высокого операционного риска [3, 5].
Для профилактики и лечения осложнений после лапароскопической холецистэктомии необходима разработка специальных патогенетически обоснованных комплексов, в частности, с включением в них комплексных гомеопатических препаратов Гепар композитум, Траумель С, Коэнзим композитум, Убихинон композитум, Хепель. В соответствии с имеющимися научными данными, эти препараты должны оказать значимый клинический эффект при рассматриваемой патологии. Клиническому изучению этого предположения посвящено настоящее исследование.
Цель исследования заключается в изучении лечебной эффективности, безопасности и переносимости комплексных гомеопатических препаратов Гепар композитум, Коэнзим композитум, Траумель С, Убихинон композитум и Хепель в периоперационном периоде у больных желчнокаменной болезнью.
Пациенты и методы исследования
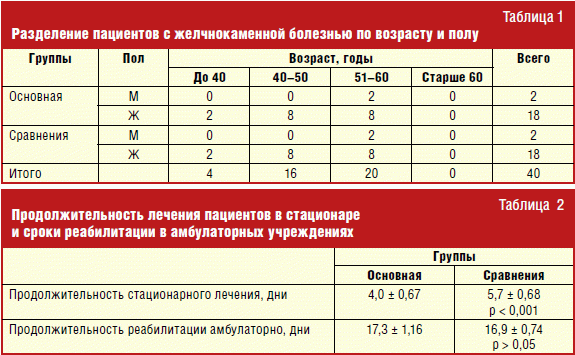
Под нашим наблюдением находилось 40 пациентов с желчнокаменной болезнью, перенесших лапароскопическую холецистэктомию и разделенных на две группы: основную (20 пациентов) и группу сравнения (20 пациентов). Возраст пациентов колебался от 31 до 60 лет (табл. 1) и составил в среднем в основной группе 48,6 ± 7,85 года, а в группе сравнения — 48,4 ± 8,52 года (p > 0,05). Из общего числа пациентов мужчины в обеих группах составили 10%, а женщины по 90%.
Всем больным по поводу желчнокаменной болезни, осложнившейся хроническим калькулезным холециститом, выполнена лапароскопическая холецистэктомия и дренирование подпеченочного пространства полихлорвиниловой трубкой. Для холецистэктомии применена эндоскопическая система Stryker и набор хирургических инструментов фирмы Auto Suture. В предоперационном периоде пациенты основной группы в течение трех дней получали ежедневные внутривенные капельные вливания в 200 мл 0,9% раствора хлорида натрия препаратов: 1-я инъекция — Гепар композитум, Траумель С, Коэнзим композитум (по 1 амп.); 2-я инъекция — Гепар композитум, Траумель С, Убихинон композитум (по 1 амп.); 3-я инъекция включала Гепар композитум, Траумель С, Коэнзим композитум (по 1 амп.). Во время лапароскопической холецистэктомии в 20,0 мл 0,9% раствора хлорида натрия внут��ивенно вводили по 1 амп. Гепар композитум, Траумель С и Коэнзим композитум. В послеоперационном периоде в течение 5 дней осуществляли инфузии антигомотоксических препаратов в 200,0 мл 0,9% раствора хлорида натрия: 1-я инъекция — Гепар композитум, Траумель С, Коэнзим композитум (по 1 амп.); 2-я инъекция — Гепар композитум, Траумель С, Убихинон композитум (по 1 амп.); 3-я инъекция — Гепар композитум, Траумель С, Коэнзим композитум (по 1 амп.); 4-я инъекция — Гепар композитум, Траумель С, Убихинон композитум (по 1 амп.); 5-я инъекция — Гепар композитум, Траумель С, Коэнзим композитум (по 1 амп.). После выписки из стационара в поликлинике или во время реабилитации в специализированном отделении курорта Усть-Качка назначали следующее лечение в течение 2,5 недель: Траумель С (по 1 таблетке 3 раза в день сублингвально) и Хепель (по 1 табл. 3 раза в день сублингвально). Препараты назначали натощак за 15 мин до еды. Пациенты принимали их вместе.
Пациенты группы сравнения каких-либо препаратов в предоперационном периоде не принимали. В послеоперационном периоде пациентам обеих групп в течение первых суток осуществляли внутривенные инфузии 500,0 мл 5% раствора глюкозы и 1000,0 мл 0,9% раствора хлорида натрия, в течение 5 дней внутримышечно инъецировали ампициллин (0,5 г через 8 часов). Дренажи из брюшной полости удаляли через 1 сутки после операции.
Оценку эффективности лечения проводили по динамике жалоб (боли в верхних отделах живота, слабость, быстрая утомляемость), по данным объективного обследования (изменение цвета кожных покровов, гепатомегалия, спленомегалия, энцефалопатия). Выраженность болевого синдрома оценивали в баллах по следующей схеме: ноющая, тупая боль слабой интенсивности — 1 балл, давящая — 2 балла, распирающая — 3 балла, острая — 4 балла, колющая, высокой интенсивности — 5 баллов. Интенсивность диспепсических синдромов определяли по наличию тошноты (постоянная/после еды), изжоги (постоянная/после еды), отрыжки (воздухом/пищей), горечи во рту (постоянная/утром), метеоризма, неустойчивого стула. Измеряли температуру тела в динамике, оценивали характер заживления ран, наличие послеоперационных раневых и других осложнений.
При общепринятых исследованиях определяли содержание эритроцитов, гемоглобина, лейкоцитов, СОЭ. Уровень билирубина исследовали колориметрическим диазаметодом по Jendrassik, холестерина — энзиматическим колориметрическим методом, щелочной фосфатазы — оптимизированным кинетическим методом, глюкозы — глюкозооксидантным методом, альфа-амилазы — оптимизированным энзиматическим кинетическим методом. Уровень аланинаминотрансферазы (АЛТ) и аспартатаминотрансферазы (АСТ) исследовали оптимизированным энзиматическим кинетическим методом. Креатинин определяли основанным на реакции Яффе без депротеинизации псевдокинетическим двухточечным методом, а мочевину — уреазным кинетическим методом. О состоянии системы гемостаза судили по величине протромбинового индекса и концентрации фибриногена. Последнюю определяли по Рутбергу.
Ультразвуковое исследование внутренних органов и изучение печеночного кровотока проводили на аппаратах Toshiba SAL-383 и Medison-8800, а компьютерную томографию — на компьютерном спиральном томографе Picker-PQS. По показаниям проводили диагностическую лапароскопию при помощи эндоскопической видеосистемы фирмы Stryker.
Материалы исследования подвергнуты математической обработке с помощью пакетов статистических программ Excel 2003, Statistica for Windows 6.0. Для характеристики количественных признаков в разных группах применялись непараметрические критерии Вальда–Вольфовитса, Манна–Уинти и Колмогорова–Смирнова. Статистически значимыми считались различия при уровне этих критериев, меньшем 0,05.
Результаты и обсуждения
Назначенные лечебные комплексы антигомотоксических препаратов переносились больными хорошо, каких-либо нежелательных реакций и осложнений при их использовании не наблюдалось. Не отмечено также признаков несовместимости антигомотоксических препаратов с аллопатическими средствами.
Включение в лечебный комплекс антигомотоксических препаратов способствовало сокращению сроков стационарного лечения пациентов с 5,7 ± 0,68 суток в группе сравнения до 4,0 ± 0,67 суток в основной группе (p < 0,001) (табл. 2). Амбулаторная реабилитация составила в основной группе 17,3 ± 1,16 дня, а в группе сравнения — 16,9 ± 0,74 суток.
В табл. 3 представлена динамика температуры тела у пациентов обеих групп. После операции более выраженная гипертермия (37,6 ± 0,21 °C) была в группе сравнения, чем в основной, где она была равна 36,9 ± 0,37 °C (p < 0,001). Это свидетельствует о том, что антигомотоксические средства, примененные в предоперационном периоде и во время оперативного вмешательства, обладают противовоспалительным, детоксикационным и иммуномодулирующим действием. Послеоперационный период в основной группе отличался меньшей встречаемостью и выраженностью болевого и диспепсического синдромов (табл. 4).
Из табл. 4 видно, что распространенность болевого синдрома при выписке из стационара составляла по 50% в основной группе и группе сравнения, а после окончания курса реабилитации она снизилась в основной группе до 20%, а в группе сравнения до 30%. Аналогичная закономерность обнаружена и в регрессе диспепсических синдромов. Встречаемость их после окончания курса стационарного лечения была одинаковой в обеих группах, составив 40%, а после окончания курса реабилитации она в основной группе снизилась до 10%, а в группе сравнения — до 30%.
Выраженность болевого синдрома при выписке из клиники в основной группе составила 3,0 ± 0,82 балла, а в группе сравнения — 3,6 ± 0,52 балла. Различия между этими показателями не существенны и статистически недостоверны (p > 0,05). Окончание курса реабилитации характеризовалось снижением интенсивности болевых ощущений в основной группе до 1,2 ± 0,42 балла, что существенно отличалось от аналогичного показателя группы сравнения — 2,5 ± 0,53 балла (p < 0,001). Интенсивность диспепсических синдромов после окончания курса реабилитации также была более выраженной в группе сравнения (2,1 ± 0,74 балла) по сравнению с основной группой (1,0 ± 0,67 балла, p < 0,001).
Определенные положительные тенденции в течении послеоперационного периода обнаружены и при лабораторных исследованиях. Из табл. 5 видно, что примененный лечебный комплекс с включением антигомотоксических препаратов способствовал умеренному повышению содержания гемоглобина, снижению концентрации лейкоцитов и величины СОЭ.
У пациентов группы сравнения зарегистрировано снижение уровня гемоглобина. Уменьшение показателей содержания лейкоцитов и СОЭ в группе сравнения было выражено в меньшей степени, чем в основной группе. Биохимические исследования крови подтвердили положительное влияние антигомотоксических средств на функциональные способности печени, о чем свидетельствует снижение уровня билирубина, АЛТ, АСТ и щелочной фосфатазы. В группе сравнения зарегистрировано лишь снижение уровня АСТ и щелочной фосфатазы (табл. 6). Оперативные вмешательства на желчном пузыре сопровождались повышением содержания α-амилазы до 133,6 ± 9,37 ЕД/л в основной группе и 153,6 ± 9,37 ЕД/л в группе сравнения (p < 0,05). После окончания курса лечения содержание α-амилазы существенно снизилось в обеих группах, достигнув в основной группе 93,2 ± 9,65 ЕД/л, а в группе сравнения 101,5 ± 12,78 ЕД/л (p > 0,05).
В обеих группах пациентов произошло умеренное снижение уровня креатинина, а содержание мочевины не претерпело существенных изменений (табл. 7). Протромбиновый индекс повысился в основной группе с 71,6 ± 3,7% до 76,1 ± 3,5% (p < 0,05), а в группе сравнения произошло его повышение с 72,8 ± 3,79% до 74,7 ± 5,74%, что оказалось не существенным и статистически недостоверным (p > 0,05).
Уровень фибриногена после операции был одинаков в обеих сравниваемых группах, а после окончания курса реабилитации в основной группе составил 3,32 ± 0,25 г/л, а в группе сравнения 2,63 ± 0,43 г/л (p < 0,05).
В основной группе послеоперационные раны у всех пациентов зажили первичным натяжением без явлений воспаления, а в группе сравнения у шести больных были воспалительные инфильтраты краев ран, которые завершились нагноением у четырех пациентов. Для лечения этих больных были сняты швы, эвакуирован гной и осуществлено дренирование подкожной клетчатки. Раны зажили вторичным натяжением.
Выводы
На основании полученных нами результатов следует рекомендовать для внедрения в клиническую практику антигомотоксические препараты Гепар композитум, Траумель С, Коэнзим композитум, Убихинон композитум, которые целесообразно применять в предоперационном периоде, во время лапароскопической холецистэктомии и в первые 5 дней послеоперационного периода. В процессе реабилитации в амбулаторных условиях в специализированных отделениях курорта Усть-Качка хорошо зарекомендовал себя прием препаратов Траумель С и Хепель в течение 2,5 недель.
Включение в программу лечения этих препаратов позволяет уменьшить интоксикацию, нормализовать иммунологические реакции, достичь обезболивающего и кровоостанавливающего эффекта, укрепить печеночные клетки, защитить поджелудочную железу. Переносимость пациентами препаратов хорошая, они сочетаются с примененными аллопатическими средствами.
Литература
- Заривчацкий М. Ф., Сандрацкая А. В., Колыванова М. В., Ермашов А. Г., Голованенко А. В. Эндоскопические методы лечения желчнокаменной болезни и ее осложнений. В кн.: Миниинвазивная хирургия в клинике и эксперименте. Материалы Рос. науч-практ. конф. Пермь, 2003. С. 52–53.
- Мохов Е. М., Семененко И. А., Лубашевский В. Т. Морфологические изменения печени при желчнокаменной болезни и качество жизни оперированных больных // Анналы хирургической гепатологии. 2008. № 2. С. 65–68.
- Ремизов А. С., Киселев А. И., Желнинов М. Г., Ефанов Д. А., Лодыгин А. В., Ахметов А. Опыт бездренажной холецистэктомии/Тез. докл. XVI Международного конгресса хирургов-гепатологов стран СНГ «Актуальные проблемы хирургической гепатологии. Екатеринбург, 2009. С. 190–191.
- Руководство по хирургии печени и желчевыводящих путей // Под ред. А. Е. Борисова. Том I. СПб: Изд-во «Скифия», 2003. 485 с.
- Рутгайзер Я. М. Возможности использования клинико-психологических методов в гастроэнтерологии // Рос. журн. гастроэнтерологии, гепатологии, колопроктологии. 1997. № 6. С. 38–45.
- Сандаков П. Я., Самарцев В. А., Дьяченко М. И. Миниинвазивные технологии в хирургии желчевыводящих путей у геронтологических больных // Эндоскопическая хирургия. № 5. 2003. С. 122.
- Сотниченко Б. А., Макаров В. И., Савинцева Н. В. Эндовидеохирургическое лечение больных осложненными формами острого холецистита // Анналы хирургической гепатологии. 2007. № 2. С. 75–78.
- Хирургия печени и желчевыводящих путей / Под ред. Б. И. Альперовича. Томск, 1997. 605 с.
- Черкасов В. А., Попов А. В., Гущинский Л. Б., Палатова Л. Ф. Тактика ведения раннего послеоперационного периода у больных холелитиазом // Пермский медицинский журнал. 2003. № 3–4. С. 27–30.
М. Ф. Заривчацкий1, доктор медицинских наук, профессор
О. Ю. Пирожников
А. Г. Ермашов
А. В. Сандрацкая
ГБОУ ВПО ПГМА им. ак. Е. А. Вагнера МЗ РФ, Пермь
1 Контактная информация: msch11957@mail.ru
Купить номер с этой статьей в pdf