Нестероидные противовоспалительные препараты (НПВП) — важнейший класс препаратов, используемых для купирования острой и контроля хронической боли в терапевтической практике. НПВП отличает сочетание анальгетического, противовоспалительного и жаропонижающего действия, что обеспечивает их преимущество в сравнении с парацетамолом и опиоидами [1–3].
В настоящее время в России зарегистрировано девятнадцать различных НПВП. Это «международные непатентованные наименования», т. е. химические субстанции, а конкретных коммерческих препаратов больше на целый порядок. К сожалению, ни один из современных НПВП не может считаться идеальным: если какой-либо препарат имеет преимущество по тому или иному параметру, скорее всего, у него найдутся и серьезные недостатки.
Основным различием между разными представителями группы НПВП является их безопасность. До последнего времени главной проблемой этих лекарств считалось развитие осложнений со стороны желудочно-кишечного тракта (ЖКТ). Все НПВП являются ингибиторами циклооксигеназы (ЦОГ) 2, однако, помимо этого действия, они могут подавлять близкий по структуре фермент ЦОГ-1. Работа последнего необходима для поддержания защитного потенциала слизистой оболочки ЖКТ, поэтому его блокада может приводить к развитию опасной патологии ЖКТ — т. н. НПВП-гастропатии и НПВП-энтеропатии [4].
Селективность в отношении ЦОГ-2, а следовательно, риск развития патологии ЖКТ, стала основой разделения НПВП на две группы: «традиционные», или неселективные (н-НПВП), и селективные (с-НПВП). с-НПВП, т. н. «коксибы», были созданы в конце 90-х годов прошлого века как более безопасная для ЖКТ альтернатива «традиционным» НПВП. Но, как оказалось, «коксибы» имеют серьезный недостаток: селективная блокада ЦОГ-2 способна нарушать баланс факторов, влияющих на свертывание крови, — синтез тромбоксана А2 и простациклина, что определяет протромботический эффект. У пациентов с болезнями сердечно-сосудистой системы (ССС) это чревато повышением риска тромбоэмболических осложнений, таких как инфаркт миокарда (ИМ) и ишемический инсульт [4].
Эта проблема возродила интерес практикующих врачей к «традиционным» НПВП, применение которых, как представлялось, ассоциируется с существенно меньшей опасностью кардиоваскулярных (КВ) осложнений.
Но далеко не все н-НПВП безопасны в отношении ССС. Так, риск КВ-осложнений при использовании наиболее популярного в России представителя «традиционных» НПВП диклофенака весьма высок. Этот факт показывает метаанализ 25 популяционных исследований, проведенных в 18 независимых популяциях и представляющих индивидуальный риск КВ-осложнений для разных НПВП. Критерием оценки была частота ИМ, развитие которого было отмечено у ~100 000 пациентов. Минимальный риск ИМ был показан для напроксена (отношение шансов (ОШ) — 1,06) и целекоксиба (ОШ — 1,12); для диклофенака этот показатель составил 1,38 [5].
Существенно меньший риск КВ-осложнений демонстрирует другой популярный н-НПВП — кетопрофен. Этот препарат появился в Европе в 1971 г. и быстро завоевал репутацию эффективного и надежного анальгетика [6]. За сорок лет клинического применения он не утратил своего значения. P. Sarzi-Puttini и соавт. подчеркивают этот факт в обзоре с весьма характерным названием: «Боль и кетопрофен: его роль в клинической практике», который был опубликован в 2010 году. Они указывают на огромную базу доказательств его эффективности, широкий спектр показаний — по сути, все патологические процессы, сопровождающиеся ноцицептивной болью, и хорошую репутацию у врачей [7].
Интерес к кетопрофену можно оценить по росту его назначений в странах Европы. Так, M. Venegoni и соавт. показали, что на фоне небольшого, но явного снижения общих продаж «рецептурных» НПВП в Италии за период с 2006 по 2009 гг. популярность кетопрофена выросла почти в 2 раза (на 93%). Если в 2006 г. кетопрофен приобрели 263 897 жителей этой страны, то в 2009 г. — уже 508 699 [8].
Многие эксперты связывают высокий анальгетический потенциал кетопрофена с особенностями его молекулы. Липофильность и относительно небольшие размеры кетопрофена определяют его способность легко проникать в воспаленную ткань (например, в синовиальную полость при артрите), создавая высокую концентрацию [7, 9]. Большое значение придается диффузии кетопрофена через гематоэнцефалический барьер и его действию на центральные структуры болевой системы. Экспериментальные данные подтверждают равновесие концентрации несвязанной фракции кетопрофена в плазме крови и ликворе. При этом центральный эффект этого препарата связывается не только с блокадой ЦОГ-2, но и иными механизмами, в частности, с его влиянием на серотонинергическую антиноцицептивную систему [10].
Как было отмечено выше, опыт использования кетопрофена включает все заболевания и патологические состояния, при которых назначение НПВП представляется целесообразным. Работу с кетопрофеном облегчает наличие полного спектра лекарственных форм: раствора для внутривенного (в/в) и внутримышечного (в/м) введения, стандартных таблеток, капсул контролируемого высвобождения, форм для местного применения, ректальных свечей.
Кетопрофен — весьма удачное средство для ургентного обезболивания. В 2009 г. были опубликованы данные метаанализа Cochrane, оценивающего результаты однократного приема кетопрофена в дозе 25–100 мг при острой послеоперационной боли. Материалом послужили данные 14 рандомизированных контролируемых исследований (РКИ) (968 больных, получавших кетопрофен, 520 плацебо), а основным критерием оценки было снижение боли > 50% на срок от 4 до 6 часов. Исследователи использовали индекс NNT (number need to treat), показывающий число больных, которых необходимо пролечить для достижения значимого отличия от плацебо. Этот индекс составил 2,4–3,3, что показывает достаточно высокую эффективность препарата [11].
Недавно опубликованы данные масштабного исследования (n = 338), в котором изучалось действие однократного внутривенного введения парекоксиба 40 мг и кетопрофена 100 мг для купирования острой почечной колики. Кетопрофен, выступавший в роли препарата сравнения, нисколько не уступал представителю «коксибов»: снижение боли (по визуальной аналоговой шкале — ВАШ) через 30 мин после инъекции составило 35,2 ± 26,0 и 33,8 ± 24,6 мм [12].
Работа S. Karvonen и соавт. является примером успешного применения кетопрофена в хирургической практике. Здесь кетопрофен в дозе 300 мг/сут был использован у 60 больных, перенесших ортопедические операции. Контроль составили пациенты, получавшие плацебо или парацетамол 4 г/сутки. Критерием эффективности, кроме снижения выраженности боли, была оценка «опиоид-сберегающего» действия, которое определялось при сравнении необходимой для стойкой анальгезии дозы фентанила. Этот эффект был отмечен лишь в группе кетопрофена: средняя доза фентанила здесь оказалась на 22% меньше по сравнению с группой плацебо и на 28% меньше в сравнении с группой парацетамола [13].
Хорошие результаты были отмечены при использовании кетопрофена в стоматологии. J. Olson N. и соавт. провели исследование, в ходе которого 239 пациентам после удаления 3-го моляра был назначен кетопрофен в минимальной дозе (25 мг), ибупрофен 400 мг или парацетамол 1000 мг; «пассивным» контролем являлось плацебо. Главным методом оценки являлось сравнение числа пациентов, у которых спустя 6 часов после экстракции зуба боль полностью отсутствовала. Этот результат был достигнут почти у всех больных, получивших кетопрофен, — 99%, у 96% получивших ибупрофен и 88% — парацетамол (разница недостоверна). Все активные препараты превосходили плацебо, на фоне которого боль купировалась лишь у одной трети пациентов (33,6%). Как видно, даже минимальная доза кетопрофена дает столь же выраженное (и даже несколько большее) облегчение боли, как стандартные терапевтические дозы ибупрофена и парацетамола [14].
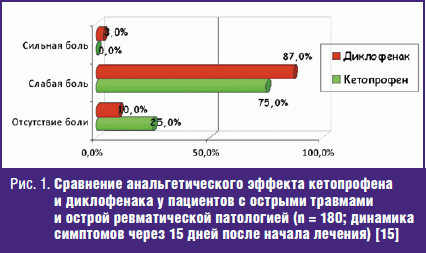
Удачной демонстрацией преимущества кетопрофена стала работа I. Jokhio и соавт., которые сравнили его с диклофенаком у 180 пациентов, испытывающих выраженные боли (среднее значение по ВАШ ~70 мм) вследствие травмы или острой патологии мягких тканей ревматической природы. При этом была использована т. н. «ступенчатая» терапия: в первый день НПВП применяли в виде в/м инъекций, а затем перорально. Соответственно, половина пациентов получила две инъекции кетопрофена по 100 мг, а затем принимали этот препарат по 100 мг 2 раза в день. Вторая группа больных получила две инъекции диклофенака по 75 мг, а в дальнейшем принимали его по 50 мг 3 раза в день внутрь. Курс лечения составил 2 недели. К концу периода наблюдения кетопрофен демонстрировал лучшие результаты (рис. 1). При этом 72% больных, получавших кетопрофен, оценили его переносимость как «хорошую или отличную»; такую оценку диклофенаку дали лишь 50% пациентов [15].
Одним из последних доказательств высокой анальгетической эффективности кетопрофена стала работа итальянских ученых P. Sarzi-Puttini и соавт. — метаанализ 13 РКИ (n = 898), в которых сравнивалось действие кетопрофена 50–200 мг/сут с ибупрофеном 600–1800 мг/сут или диклофенаком 75–100 мг/сут у больных с разными ревматическими заболеваниями. Кетопрофен показал достоверное превосходство над препаратами сравнения в 9 из 13 РКИ. При этом вероятность достижения благоприятного эффекта при назначении кетопрофена была почти в 2 раза выше (ОШ 0,459: 0,33–0,58, p = 0,000) [16].
Кетопрофен показал себя действенным средством для купирования приступа мигрени. Согласно результатам исследования M. Dib и соавт., он не уступал золмитриптану — представителю группы триптанов, которые являются важнейшим патогенетическим средством для лечения этого заболевания. В этой работе 235 пациентов с мигренью однократно приняли кетопрофен 75 или 150 мг или золмитриптан. Во всех группах отмечался практически одинаковый результат: через 2 часа боль прекратилась у 62,6%, 61,6% и 66,8% пациентов соответственно [17].
Необходимо отметить, что кетопрофен обладает хорошим противовоспалительным потенциалом. Наилучшей моделью оценки противовоспалительного эффекта НПВП является купирование подагрического артрита, при котором выраженная боль определяется острой воспалительной реакцией. «Золотым стандартом» лечения этой патологии долгое время считался индометацин, обладающий выраженными противовоспалительными свойствами. Кетопрофен, как показали R. Altman и соавт., успешно прошел сравнение с этим препаратом. В ходе исследования 59 пациентов с острым подагрическим артритом в течение 7 дней принимали кетопрофен 100 мг 3 раза в день или индометацин 50 мг 3 раза в день. Кетопрофен обеспечил значимое облегчение боли в первый же день лечения у 92% больных; в контрольной группе их оказалось 91%. Через неделю лечения приступ был полностью купирован у 24% и 22% пациентов. Как видно, кетопрофен не уступал индометацину по эффективности. Но при этом он отчетливо превосходил его по безопасности — на фоне приема индометацина какие-либо побочные эффекты были отмечены у 20% больных, а в группе кетопрофена — лишь у 11% [18].
Помимо экстренного обезболивания, кетопрофен оказался эффективным средством для длительного контроля боли при хронических заболеваниях опорно-двигательного аппарата.
Важным доказательством достоинств кетопрофена стало европейское проспективное открытое исследование, охватившее около 20 тыс. больных с различной ревматической патологией, в основном остеоартрозом (ОА). Через 1 месяц более 70% пациентов, принимавших кетопрофен в дозе 200 мг/сут, отметили хороший или превосходный результат; при этом ЖКТ-осложнения суммарно возникли у 13,5%, а язвы и кровотечения всего у 0,03% [19].
Работа M. Schattenkirchner и соавт. показала хорошую переносимость кетопрофена при длительном использовании. В их исследовании 823 больных ОА и ревматоидным артритом получали кетопрофен в течение года. На фоне лечения осложнения со стороны ЖКТ возникли у 28% пациентов (лишь у 1,7% серьезные), а со стороны ССС — у 3,2%, что относительно немного, учитывая преимущественно пожилой возраст пациентов и тяжелый коморбидный фон [20].
Удачные результаты были получены при использовании кетопрофена у больных анкилозирующим спондилоартритом (АС). При АС НПВП играют роль основного терапевтического агента, позволяющего контролировать развитие болезни. В исследовании M. Dougados и соавт. 246 больных АС в течение 6 недель принимали целекоксиб 200 мг, кетопрофен 200 мг или плацебо. Достоверной разницы по обезболивающему действию обоих НПВП не было, при этом они существенно превосходили плацебо. Особый интерес представляет влияние НПВП на такие симптомы, как ночная боль и утренняя скованность, которые в большей степени отражают противовоспалительный эффект. Действие кетопрофена и целекоксиба практически не различалось: уменьшение ночных болей составило в среднем 21 и 27 мм ВАШ (в группе плацебо увеличилось на 13 мм), утренняя скованность уменьшилась на 16 и 17 минут (в группе плацебо не изменилась). Таким образом, кетопрофен оказывает четкое противовоспалительное действие при АС. Интересно, что число ЖКТ-осложнений на фоне приема «коксиба» и кетопрофена не различалось: они возникли у 13% и 14% больных (8% на плацебо) [21]. Обсуждая безопасность кетопрофена, нельзя обойти вниманием тот факт, что ряд популяционных исследований демонстрируют для этого препарата существенный риск ЖКТ-осложнений. Так, J. Castellsague и соавт. провели метаанализ 28 эпидемиологических работ (1980–2011 гг.), в которых оценивалось развитие ЖКТ-осложнений при использовании разных НПВП. Наименьший риск был отмечен для целекоксиба — ОШ 1,45, ацеклофенака 1,4 и ибупрофена — 1,84. Существенно выше опасность была при использовании диклофенака — 3,34, мелоксикама — 3,47 и нимесулида — 3,83. Кетопрофен вошел в «тройку» препаратов с наибольшим риском — 3,92, как и напроксен — 4,1 и индометацин — 4,14 [22].
С другой стороны, одно из наиболее крупных популяционных исследований показало для кетопрофена относительно низкий риск ЖКТ-осложнений. Эта работа финских ученых A. Helin-Salmivaara и соавт., основанная на оценке причин 9191 случая ЖКТ-кровотечения, язв и перфорации, отмеченных с 2000 по 2004 гг. Контроль составили 41 780 лиц, соответствующих по полу и возрасту. Риск ЖКТ-осложнений при использовании кетопрофена оказался ниже, в сравнении с диклофенаком: ОШ 3,7 и 4,2 соответственно. Любопытно, что кетопрофен демонстрировал аналогичный или даже меньший риск развития патологии ЖКТ, чем более селективные НПВП (за исключением целекоксиба). Так, ОШ для мелоксикама, нимесулида и эторикоксиба составило 3,4, 4,0 и 4,4 соответственно [23].
Следует отметить, что в России накоплен большой собственный опыт применения кетопрофена. В частности, в нашей стране был проведен ряд клинических исследований, результаты которых показали не только хороший терапевтический потенциал этого препарата, но и низкую частоту осложнений [24, 25].
Среди них следует выделить работу Л. Б. Лазебника и соавт., в которой проводилось 3-месячное сравнение 4 НПВП: лорноксикама, нимесулида, целекоксиба и кетопрофена у 132 больных ОА. Авторы изучали риск осложнений со стороны ЖКТ, суточную динамику артериального давления (АД). Кетопрофен демонстрировал хорошую переносимость: число больных с эрозиями и язвами после использования лорноксикама составило 66% (!), нимесулида — 13,5%, кетопрофена — 13,0%, целекоксиба — 8,3%. Повышение АД свыше 130/90 мм рт. ст. было отмечено лишь у 2% больных, получавших кетопрофен. В отношении лорноксикама и нимесулида ситуация оказалась совсем иной — у пациентов, принимавших эти препараты, повышение АД было отмечено у 11% и 13% [26] (рис. 2). Эта работа показывает одно из наиболее ценных преимуществ кетопрофена — относительно низкий риск осложнений со стороны ССС.
Связь между приемом кетопрофена и КВ-катастрофами определялась в нескольких эпидемиологических исследованиях. Так, низкий риск ИМ при использовании кетопрофена был показан американскими учеными G. Singh и соавт. Проанализировав причины 15 343 эпизодов ИМ (61 372 человека составили соответствующий контроль), авторы сопоставили частоту этого осложнения у лиц, принимавших НПВП. Оказалось, что прием кетопрофена ассоциировался с наименьшим риском ИМ (ОШ 0,88), даже в сравнении с напроксеном (ОШ 1,08), который традиционно считается препаратом, наиболее безопасным в отношении ССС [27].
Близкие результаты были получены M. Solomon и соавт., сравнившими использование различных НПВП у 4425 больных, у которых развился ИМ, и 17 700 лиц без данного осложнения. Согласно полученным данным, разницы по приему кетопрофена в этих группах не было: его получали 53 больных, развивших ИМ (1,2%), и 190 лиц, составлявших контроль (1,1%). Таким образом, использование кетопрофена, по данным этого исследования, не повышало риск развития КВ-катастроф [28].
Низкий риск КВ-осложнений для кетопрофена показали и результаты популяционного исследования финских ученых A. Helin-Salmivaara и соавт. Их работа была основана на сопоставлении данных о приеме НПВП у 33 309 лиц, перенесших ИМ, и 138 949 здоровых людей. Оказалось, что прием кетопрофена фактически не увеличивал опасность развития КВ-катастроф (ОШ 1,11) [29].
В 2012 г. была опубликована масштабная работа ученых из Тайваня, изучавших КВ-риск при использовании различных НПВП в собственной популяции. Исследуемый материал был получен с использованием данных национальной системы здравоохранения, где имелась информация о 13,7 млн лиц, использовавших НПВП, из которых 8354 перенесли инфаркт миокарда. Пероральный кетопрофен демонстрировал минимальный уровень риска (ОШ 1,17). Он оказался более безопасным, чем подавляющее большинство других НПВП (рис. 3).
Следует отметить, что парентеральное использование НПВП (это был отдельный раздел анализа) ассоциировалось с более высоким риском КВ-осложнений. Так, для кетопрофена риск был повышен более чем вдвое: ОШ 2,34; близкое значение было получено для диклофенака: 1,88, и значительно более высокое — для кеторолака: 4,27 [30].
Таким образом, кетопрофен — универсальный анальгетик, который может с успехом использоваться как для купирования острой, так и длительного контроля хронической боли. Благоприятные фармакологические свойства определяют его преимущества в сравнении с другими НПВП при ургентном обезболивании, когда быстрота облегчения страданий имеет принципиальное значение. Наличие в арсенале врача разных лекарственных форм помогает при выборе стратегии обезболивающей терапии: для получения максимально быстрого эффекта в первые дни лечения может быть оправдано применение парентеральных форм кетопрофена, с последующим переходом на регулярный пероральный прием. Позитивным моментом является также наличие на фармакологическом рынке качественных и недорогих генериков кетопрофена, таких как Фламакс® (Сотекс), доступных большинству пациентов.
Конечно, кетопрофен не лишен недостатков; основной из них, типичный для всех «традиционных» НПВП, — возможность развития патологии ЖКТ. Однако тщательный учет факторов риска перед назначением НПВП и — если соответствующие факторы присутствуют — профилактическое использование гастропротекторов (ингибиторов протонной помпы) позволяют значительно снизить эту опасность. Но при этом кетопрофен показывает низкий риск осложнений со стороны сердечно-сосудистой системы. Это несомненное преимущество, которое расширяет возможность применения данного препарата у лиц пожилого возраста, многие из которых имеют кардиоваскулярные факторы риска.
Литература
- Насонов Е. Л. Анальгетическая терапия в ревматологии: путешествие между Сциллой и Харибдой // Клин. фармакол. терапия. 2003; 12 (1): 64–69.
- Боль (практическое руководство для врачей). Под ред. Яхно Н. Н., Кукушкина М. Л. М.: Издательство РАМН, 2012. 512 c.
- Lee Y. Effect and treatment of chronic pain in inflammatory arthritis // Curr Rheumatol Rep. 2013; 15 (1): 300.
- Каратеев А. Е., Яхно Н. Н., Лазебник Л. Б. и др. Применение нестероидных противовоспалительных препаратов. Клинические рекомендации. М.: ИМА-ПРЕСС, 2009. 167 с.
- Varas-Lorenzo C., Riera-Guardia N., Calingaert B. et al. Myocardial infarction and individual nonsteroidal anti-inflammatory drugs meta-analysis of observational studies // Pharmacoepidemiology and Drug Safety. 2013; 22: 559–570.
- Veys E. 20 years’ experience with ketoprofen // Scand J Rheumatol Suppl. 1991; 90: Suppl 1–44.
- Sarzi-Puttini P., Atzeni F., Lanata L. et al. Pain and ketoprofen: what is its role in clinical practice? // Reumatismo. 2010, 62 (3): 172–188.
- Venegoni M., Da Cas R., Menniti-Ippolito F., Traversa G. Effects of the European restrictive actions concerning nimesulide prescription: a simulation study on hepatopathies and gastrointestinal bleedings in Italy // Ann Ist Super Sanita. 2010; 46 (2): 153–157.
- Kokki H. Ketoprofen pharmacokinetics, efficacy, and tolerability in pediatric patients // Paediatr Drugs. 2010; 12 (5): 313–329.
- Díaz-Reval M., Ventura-Martínez R., Déciga-Campos M. et al. Evidence for a central mechanism of action of S- (+)-ketoprofen // Eur J Pharmacol. 2004; 483 (2–3): 241–248.
- Barden J., Derry S., McQuay H., Moore R. Single dose oral ketoprofen and dexketoprofen for acute postoperative pain in adults // Cochrane Database Syst Rev. 2009, Oct 7; (4): CD007355.
- Glina S., Damiao R., Afif-Abdo J. et al. Efficacy and safety of parecoxib in the treatment of acute renal colic: a randomized clinical trial // Int Braz J Urol. 2011; 37 (6): 697–705.
- Karvonen S., Salomäki T., Olkkola K. Efficacy of oral paracetamol and ketoprofen for pain management after major orthopedic surgery // Methods Find Exp Clin Pharmacol. 2008, 30 (9): 703–706.
- J. Olson N., Otero A., Marrero I. et al. Onset of analgesia for liquigel ibuprofen 400 mg, acetaminophen 1000 mg, ketoprofen 25 mg, and placebo in the treatment of postoperative dental pain // Clin Pharmacol. 2001, 41 (11): 1238–1247.
- Jokhio I., Siddiqui K., Waraich T. et al. Study of efficacy and tolerance of ketoprofen and diclofenac sodium in the treatment of acute rheumatic and traumatic conditions // J Pak Med Assoc. 1998; 48: 373–376.
- Sarzi-Puttini P., Atzeni F., Lanata L., Bagnasco M. Efficacy of ketoprofen vs. ibuprofen and diclofenac: a systematic review of the literature and meta-analysis // Clin Exp Rheumatol. 2013 Sep-Oct; 31 (5): 731–8. Epub 2013 May 17.
- Dib M., Massiou H., Weber M. et al. Efficacy of oral ketoprofen in acute migraine: a double-blind randomized clinical trial // Neurology. 2002, 58 (11): 1660–1665.
- Altman R., Honig S., Levin J., Lightfoot R. Ketoprofen versus indomethacin in patients with acute gouty arthritis: a multicenter, double blind comparative study // J Rheumatol. 1988, 15 (9): 1422–1426.
- Le Loet X. Safety of ketoprofen in the elderly: a prospective study on 20,000 patients // Scand J Rheumatol Suppl. 1989; 83: 21–27.
- Schattenkirchner M. Long-term safety of ketoprofen in an elderly population of arthritic patients // Scand J Rheumatol Suppl. 1991; 91: 27–36.
- Dougados M., Béhier J., Jolchine I. et al. Efficacy of celecoxib, a cyclooxygenase 2-specific inhibitor, in the treatment of ankylosing spondylitis: a six-week controlled study with comparison against placebo and against a conventional nonsteroidal antiinflammatory drug // Arthritis Rheum. 2001, 44 (1):180–185.
- Castellsague J., Riera-Guardia N., Calingaert B. et al. Individual NSAIDs and upper gastrointestinal complications: a systematic review and meta-analysis of observational studies (the SOS project) // Drug Saf. 2012; 35 (12): 1127–1146.
- Helin-Salmivaara A., Saarelainen S., Gronroos J. et al. Risk of upper gastrointestinal events with the use of various NSAIDs: A case-control study in a general population // Scan J Gastroenterol. 2007; 42: 923–932.
- Чичасова Н. В., Иммаметдинова Г. Р., Каратеев А. Е. и соавт. Эффективность и безопасность кетопрофена (кетонал) при ревматоидном артрите (клинико-эндоскопическое исследование) // Научно-практическая ревматология. 2001; 1; 47–52.
- Осипова Н. А., Петрова В. В., Ермолаев П. М., Береснев В. А. Нестероидные противовоспалительные препараты в лечении послеоперационной боли у онкологических больных // Фарматека. 2006, № 6, 121.
- Лазебник Л. Б., Дроздов В. Н., Коломиец Е. В. Сравнительная эффективность и безопасность применения кетопрофена, лорноксикама, нимесулида и целекоксиба у больных остеоартрозом // РМЖ. 2004, 12 (14), 844–847.
- Singh G., Mithal A., Triadafilopoulos G. Both selective COX-2 inhibitors and non-selective NSAIDs increase the risk of acute myocardial infarction in patients with arthritis; selectivity is with patients, not the drug // Ann Rheum Dis. 2005, 64 (suppl 3), 85.
- Solomon D., Glynn R., Levin R., Avorn J. Nonsteroidal Anti-inflammatory Drug Use and Acute Myocardial Infarction. Arch Intern Med. 2002; 162: 1099–1104
- Helin-Salmivaara A., Virtanen A., Vesalainen R. et al. NSAID use and the risk of hospatalisation for first myocardial infarction in the general population: a national case-control study from Finland // Eur Heart J. 2006; 27: 1657–1663.
- Shau W., Chen H., Chen S. et al. Risk of new acute myocardial infarction hospitalization associated with use of oral and parenteral non-steroidal anti-inflammation drugs (NSAIDs): a case-crossover study of Taiwan’s National Health Insurance claims database and review of current evidence // BMC Cardiovasc Disord. 2012, Feb 2; 12: 4. doi: 10.1186/1471–2261–12–4.
А. Е. Каратеев, доктор медицинских наук, профессор
ФГБУ НИИР им. В. А. Насоновой РАМН, Москва
Контактная информация: aekarateev@rambler.ru
Купить номер с этой статьей в pdf