Резюме. Эпидемии гриппа вызывают заболеваемость и смертность как вследствие прямого действия вируса в течение первых нескольких дней, так и по причине развития вторичных бактериальных осложнений, которые обычно проявляются после первой недели. По данным исследований, до 65% лабораторно подтвержденных случаев инфицирования гриппом сопровождаются вторичной бактериальной инфекцией, которая может иметь тяжелые последствия, особенно для пациентов из групп риска. Цель настоящей работы состояла в систематизации доступных научных данных о патогенезе бактериальных осложнений гриппа. По результатам обзора установлено, что грипп типа A наиболее часто осложняется присоединением вторичной бактериальной инфекции, причем инфицирование подтипами, содержащими в своем составе нейраминидазу N2, обычно сопряжено с более тяжелым течением инфекции. Возбудителями, наиболее часто осложняющими течение гриппа с конца 1800-х годов, являются S. pneumoniae, H. influenzae и S. aureus. Показано, что инфицирование вирусом гриппа приводит к возникновению многочисленных изменений эпителия респираторного тракта и нарушениям иммунных реакций, что предрасполагает к присоединению бактериальных осложнений. Вирус гриппа способен повреждать клетки эпителия дыхательных путей и ингибировать механизмы мукоцилиарного клиренса. После бактериальной колонизации развитие заболевания происходит благодаря специфическим характеристикам вирусной инфекции, которые облегчают адгезию и проникновение бактерий. Кроме того, показано, что в альвеолярных макрофагах, нейтрофилах, дендритных и NK-клетках изменяются цитокиновые профили, вследствие чего нарушаются функции указанных клеток. Это приводит к усилению воспалительной реакции и снижению эрадикации бактерий. Однако, несмотря на увеличивающееся количество работ, подробно описывающих различные аспекты патогенеза бактериальных осложнений гриппа, определение точного вклада каждого из описанных факторов представляет собой сложную задачу, решить которую могут помочь дальнейшие исследования.
Острые респираторные вирусные инфекции (ОРВИ), включая грипп и COVID-19, являются наиболее распространенными инфекционными заболеваниями. Грипп (от франц. gripper – хватать) — острая инфекционная болезнь с аэрозольным механизмом передачи возбудителя, характеризующаяся массовым распространением, кратковременной лихорадкой, интоксикацией и поражением респираторного тракта [1]. По данным Всемирной организации здравоохранения (ВОЗ), в Европейском регионе ежегодные эпидемии гриппа обычно отмечаются в осенний и зимний периоды и способны охватывать до 20% населения [2].
История заболевания
Хотя еще в 412 г. до н. э. Гиппократ описал вспышку гриппоподобного респираторного заболевания – «перинфского кашля», включая несколько случаев, осложненных пневмонией [3], достоверных сведений о вышеуказанной болезни до эпохи Средневековья в доступных литературных источниках не встречается [4]. В последующие века произошло несколько эпидемий [5]. Жертвой масштабной эпидемии 1557-1558 гг. считается королева Англии Мария I Тюдор, смерть которой позволила ее младшей сводной сестре Елизавете взойти на престол [6]. Три основные пандемии охватили Европу в XVIII веке, причем пандемия 1781-1782 гг., получившая название «русская болезнь» [7], возможно, является величайшим проявлением инфекционного заболевания в истории: считается, что пострадало более трех четвертей всего английского населения [8], а в Петербурге в январе 1781 г. в течение одного дня заболели 40 тыс. человек при численности населения 192 тыс. [7]. В ходе эпидемии гриппа 1830-1833 гг., охватившей Москву и Санкт-Петербург, врачами были выделены три градации гриппа: катаральный, катарально-ревматический и катарально-гастрический [9]. Пандемия 1889-1890 гг., унесшая жизни около миллиона человек, стала первой мировой, а не только евразийской, эпидемией и была прозвана «русским гриппом», поскольку пришла в Россию из Средней Азии и впоследствии распространилась на Европу.
В конце Первой мировой войны пандемия гриппа типа А (так называемой испанки, вызванной штаммом H1N1), состоявшая из трех волн, прокатилась по всему земному шару, охватив около 550 млн человек, или 29,5% населения планеты [10]. По распространенной версии, источник пандемии находился в штате Канзас и передался человеку от свиньи, после чего вирус пересек Атлантику на военных кораблях и попал в Европу [11, 12].
До 1933 г. бактериологи пытались установить связь между испанским гриппом и описанной Р. Пфайффером в 1892 г. гемоглобинофильной бактерией — «палочкой инфлюэнцы» (Haemophilus influenzae) [13]. Вирус гриппа А был впервые изолирован от свиней американским вирусологом Ричардом Шоупом в 1930 г.; от людей — в 1933 г. группой английских ученых — Вильсоном Смитом, Кристофером Эндрюсом и Патриком Лейдлоу [14]. Грипп вновь стал объектом международной озабоченности в конце Второй мировой войны, а в 1952 г. была создана Глобальная система эпиднадзора за гриппом и принятия ответных мер ВОЗ [15].
Последующие пандемии – так называемый азиатский (штамм H2N2) в 1957 г., гонконгский (H3N2) в 1968 г. и свиной грипп в 1976 г. в США – были вызваны новыми штаммами вируса, происходящими из природных резервуаров (свиньи и дикие птицы) [5]. В 1997 г. впервые зарегистрировано заражение человека вирусом птичьего гриппа A(H5N1), вызвавшее вспышку заболевания в Гонконге [16]. При этом из 18 пациентов с документально подтвержденным диагнозом птичьего гриппа умерли шестеро [17]. Весной 2009 г. началась пандемия свиного гриппа
Антигенная изменчивость вируса определяет высокую восприимчивость населения к гриппу. Механизмы изменчивости вирусов гриппа представлены антигенным дрейфом и антигенным шифтом. Возникновение пандемии гриппа с большим числом тяжелых форм, приводящих к летальному исходу, связано с отсутствием специфического иммунитета к шифтовым вариантам вируса [1]. В 2009 г. грипп типа А(H1N1) имел тройное смешанное происхождение: в его геноме содержались гены вирусов человека, свиней и птиц [19].
Человек является источником вируса гриппа в остром периоде болезни, а также при ее протекании в легкой и бессимптомной формах, реже – на стадии реконвалесценции (в течение двух недель от начала заболевания) [20]. Воздушно-капельный механизм передачи остается основным и реализуется следующими путями: воздушно-капельным, воздушно-пылевым и, в меньшей степени, контактным [21].
Существенное разнообразие клинических проявлений гриппа зависит не только от возраста и уровня иммунитета больных (иммунного статуса), но и от серотипа вируса. Чаще всего пациенты предъявляют жалобы на высокую температуру тела, слабость, снижение аппетита (признаки интоксикации), боли в мышцах, суставах, при движениях глазных яблок, а также на насморк, першение в горле, кашель, ощущение царапанья за грудиной [22]. Большинство симптомов регрессируют в течение недели, однако кашель и общее недомогание могут сохраняться до двух недель [1].
Большей части пациентов с осложненным течением гриппа необходимо лечение в стационаре [23, 24]. Заболевание может способствовать обострению хронического бронхита, хронической обструктивной болезни легких, бронхиальной астмы, присоединению вторичной инфекции с развитием внебольничной пневмонии [25-27]. Проведенный анализ историй болезни госпитализированных взрослых пациентов в Санкт-Петербурге показал, что в период 2018-2019 гг. основными осложнениями гриппа являлись бронхит и пневмония (56,9% и 11,1% случаев) [28].
Бактериальные осложнения гриппа: общие сведения
Эпидемии гриппа вызывают заболеваемость и смертность как вследствие прямого действия вируса в течение первых нескольких дней, так и по причине развития вторичных бактериальных осложнений, которые обычно проявляются позже (после первой недели) [29]. Проведенные лабораторные, клинические и эпидемиологические исследования подтверждают, что бактериальные инфекции могут в значительной степени увеличить заболеваемость и смертность от гриппа [30].
В клинических рекомендациях «Грипп у взрослых» 2021 г. дано такое определение: «Осложненный грипп – грипп, требующий госпитализации и/или с симптомами и признаками инфекции нижних отделов дыхательного тракта (гипоксемия, одышка, легочный инфильтрат), вовлечения центральной нервной системы и/или значительного обострения основного заболевания» [1].
Заражение гриппом приводит к повреждению дыхательных путей посредством прямого патогенного действия, которое впоследствии предрасполагает к присоединению вторичной бактериальной инфекции [31]. Во время пандемии 1918 г. бактериальная пневмония была основной причиной заболеваемости и смертности, как показали исследования того времени, а также ретроспективный анализ [32]. Считается, что высокий уровень смертности был частично обусловлен неспособностью эффективно лечить вторичный бактериальный сепсис [29].
Исследования показали, что до 65% лабораторно подтвержденных случаев инфицирования гриппом сопровождаются вторичной бактериальной инфекцией [33]. В условиях эпидемии или пандемии гриппа вторичная бактериальная инфекция может иметь тяжелые последствия, особенно для пациентов из групп риска – например, с ослабленным иммунитетом. Иммуносупрессия сопряжена с более тяжелой заболеваемостью и гораздо более высоким риском смертности от вторичной бактериальной инфекции [34]. Во время пандемии гриппа 2009 г. наблюдался рост числа случаев внутрибольничной пневмонии в результате присоединения вторичной бактериальной пневмонии, которая была выявлена в 29-55% смертельных случаев [35, 36].
Результаты проведенных исследований показывают, что в дыхательных путях содержится разнообразная микробиота, включающая ряд бактериальных патобионтов, или оппортунистических патогенов, то есть бактерий, способных вызывать развитие заболевания в определенных условиях [37, 38]. В литературе описаны случаи коинфекции вирусом гриппа и следующими возбудителями:
На сегодняшний день установлено, что грипп типа A наиболее часто осложняется присоединением вторичной бактериальной инфекции, причем инфицирование подтипами вируса, содержащими нейраминидазу N2, обычно сопряжено с более тяжелым течением инфекции [43]. Грипп типа В также может осложняться присоединением тяжелой вторичной бактериальной инфекции [44]. Известно, что на тяжесть течения гриппа и вероятность бактериальных осложнений оказывают влияние различные факторы, в частности типы поверхностных антигенов – гемагглютинина (H) и нейраминидазы (N) [33].
Гемагглютинин опосредует связывание вириона с клеткой-хозяином через рецепторы, в состав которых входят сиаловые кислоты [45]. После этого вирус проникает в клетку посредством рецептор-опосредованного эндоцитоза с образованием эндосомы [46, 47]. Гемагглютинин связывается с сиалил-гликанами, которые обнаруживаются на поверхности эпителиальных клеток [48]; обычно в организме человека вирус гриппа типа A связывается с α-2-6-сиалил-гликанами клеток верхних дыхательных путей, тогда как высокопатогенный штамм H5N1 связывается с α-2-3-сиалил-гликанами пневмоцитов 2-го типа, выстилающих альвеолы легких [49]. Установлено, что тип гемагглютинина влияет на место и развитие инфекции [33]. Низкий уровень pH в эндосоме, содержащей вирус и формирующейся для его проникновения в клетку, вызывает конформационное изменение гемагглютинина, что является важной стадией проникновения вируса в клетку. Поэтому тип гемагглютинина и доступность соответствующих протеаз в клетках макроорганизма являются детерминантами инфекционности [46].
Нейраминидаза обусловливает высвобождение новых вирионов: посредством гидролиза концевых остатков сиаловых кислот и их отделения от гемагглютинина вирион высвобождается из клетки-хозяина [50]. При этом нейраминидаза должна быть комплементарной и обладать такой же рецепторной специфичностью, как и гемагглютинин: так, если гемагглютинин вируса связывается с α-2-3-сиаловой кислотой, то нейраминидаза также должна гидролизовать α-2-3-сиаловую кислоту [51].
Выделение вирусных пептидов, влия-ющих на целостность клеток хозяина, является еще одним важным фактором развития вторичной бактериальной инфекции [33]. Вирус гриппа типа A может продуцировать вирусный белок PB1-F2 [52], который играет роль в развитии воспаления и, следовательно, повреждении клеток хозяина и адгезии бактерий, что приводит к увеличению показателей заболеваемости и смертности [53]. PB1-F2-индуцированный апоптоз, который наиболее выражен в тканевых макрофагах (в частности, в альвеолярных макрофагах), приводит к снижению гуморального и клеточного иммунного ответа в дыхательных путях и снижению бактериального клиренса, вследствие чего увеличиваются частота возникновения и тяжесть протекания вторичной бактериальной инфекции [52, 54].
Патогенез бактериальных осложнений гриппа
Развитие бактериальных осложнений при гриппе начинается с преодоления патогенами аппарата мукоцилиарного клиренса, который в норме обеспечивает местную защиту слизистой оболочки дыхательных путей. Секреторные железы бокаловидных клеток эпителия респираторного тракта вырабатывают слизь, выступающую в роли барьера, а реснитчатый аппарат носовой полости, трахеи и бронхов очищает поверхность дыхательных путей от экзогенных патогенов [55]. Помимо обеспечения барьерной функции, эпителиальные клетки осуществляют распознавание микроорганизмов посредством экспрессии паттерн-распознающих рецепторов (pattern recognition receptors, PRRs), к которым относятся толл-подобные рецепторы (toll-like receptors, TLRs), RIG-1-подобные рецепторы (RIG-1-like receptors, RLRs) и NOD-подобные рецепторы (NOD-like receptors, NLRs) [56]. Если эпителий оказывается неспособен самостоятельно препятствовать проникновению патогенов, то им запускаются сигнальные механизмы для рекрутинга резидентных клеток иммунной системы, например, альвеолярных макрофагов [57]. Вирус гриппа способен повреждать клетки эпителия дыхательных путей и ингибировать механизмы мукоцилиарного клиренса [58].
Общая схема механизма развития бактериальных осложнений при гриппе приведена на рис. При инфицировании вирусом гриппа отмечаются многочисленные изменения эпителия респираторного тракта и нарушения иммунных реакций, что предрасполагает к присоединению бактериальных осложнений. Поскольку вирус гриппа проникает в клетки и приводит к их гибели, эпителиальные клетки респираторного тракта повреждаются и допускают адгезию бактерий. Повреждаются физические барьеры (в частности, мукоцилиарный транспорт), нарушается распознавание патогена, подавляется экспрессия антимикробных пептидов, усиливается продукция вирусов, происходит трансэпителиальная миграция бактерий, а также утрачиваются механизмы репарации. В альвеолярных макрофагах, нейтрофилах, дендритных и NK-клетках изменяются цитокиновые профили, в результате чего нарушаются функции указанных клеток. Эти изменения приводят к усилению воспалительной реакции и снижению эрадикации бактерий [63].
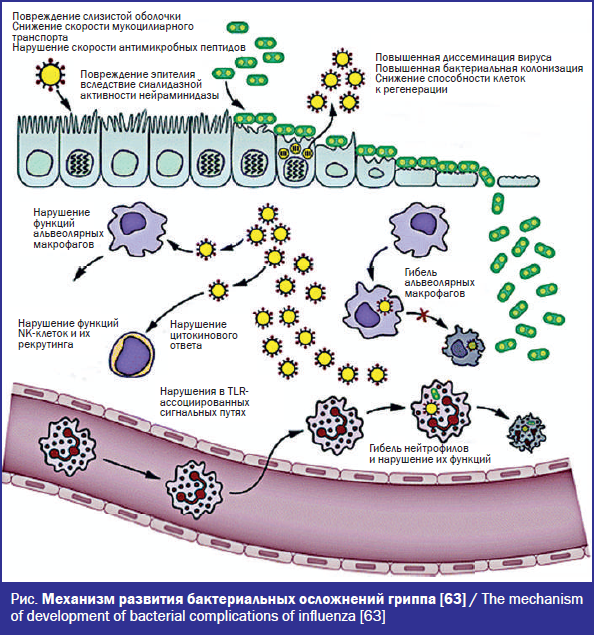
После бактериальной колонизации развитие заболевания происходит благодаря специфическим характеристикам вирусной инфекции, которые облегчают адгезию и проникновение бактерий [59]. Нейраминидаза гриппа увеличивает адгезию некоторых видов бактерий за счет удаления остатков сиаловых кислот [60]. В то же время некоторые бактерии (например, стрептококки группы B) содержат сиаловую кислоту, которая обеспечивает прямое связывание с гемагглютинином вируса, экспрессируемым клетками, инфицированными вирусом гриппа [61]. Клетки хозяина, поврежденные непосредственно вирусом или вследствие развития воспаления и иммунных реакций, содержат дополнительные места адгезии, что приводит к повышенной бактериальной адгезии [33].
Установлено, что в процессах адгезии важную роль играют интегрины – суперсемейство трансмембранных рецепторов, ответственных за взаимодействие с компонентами внеклеточного матрикса, а также белками, расположенными на поверхности бактериальных клеток [62]. Интегрины опосредуют, в частности, адгезию таких бактерий, как S. aureus и P. aeruginosa [63]. Воспалительная реакция, развивающаяся в ответ на вирусную инфекцию, может вызывать повышенную экспрессию молекул, которые бактерии способны использовать в качестве рецепторов [61]. Так, в ряде исследований показано, что некоторые бактерии, например, S. pneumoniae, могут использовать рецепторы фактора активации тромбоцитов (platelet-activating factor, PAF), сопряженные с G-белком, для прикрепления и колонизации в эндотелиальных клетках [64, 65]. В то же время в другом исследовании было высказано предположение, что рецептор PAF не влияет на первоначальную бактериальную адгезию и колонизацию, но в большей степени содействует проникновению бактерий в кровь и их распространению [66].
Грипп повышает уязвимость дыхательных путей организма хозяина к бактериальной инфекции, изменяя и ослабляя реакции иммунного ответа различными способами (табл.) [67]. Вирусная иммуносупрессия способствует присоединению бактериальной инфекции, поскольку при гриппе подавляются иммунные реакции и снижается способность организма к сопротивлению [68]. Многие исследования, проведенные на животных моделях, показали, что грипп усиливает и продлевает бактериальный рост вследствие сниженного накопления макрофагов и уменьшения бактериального клиренса, что связано со снижением фагоцитарной активности [33, 69]. Кроме того, недавно доказано, что коинфекция гриппа и S. pneumoniae приводит к сокращению количества резидентных альвеолярных макрофагов, что обусловлено их гибелью вследствие апоптоза и некроза [70]. Уменьшение количества альвеолярных макрофагов, вероятно, препятствует бактериальному клиренсу, приводя к повышенной бактериальной нагрузке и длительной воспалительной реакции.
Установлено, что грипп приводит к продукции интерферонов (ИФН); легочные провоспалительные цитокины ИФН-γ продуцируются естественными киллерами, являющимися компонентами врожденного иммунного ответа, а также CD4 и CD8 T-клетками, являющимися компонентами приобретенного иммунного ответа [71]. Они стимулируют активацию макрофагов в рамках врожденного иммунного ответа, однако при T-клеточном ответе на вирусную инфекцию они ингибируют бактериальный клиренс из дыхательной системы макрофагами. Подавление фагоцитоза открывает путь для бактериальной инфекции [69]. Кроме того, установлено, что высокие уровни интерферонов первого типа, сопутствующие вирусной инфекции, могут ухудшать антибактериальный иммунный ответ [55]. Интерфероны первого типа ингибируют интерлейкин-23 (ИЛ-23)-зависимую активацию T-хелперов 17 (Th17), регулирующих воспалительный ответ и нейтрофильные реакции, тем самым приводя к сокращению количества CD4+ T-клеток и гамма/дельта T-клеток и, следовательно, к снижению продукции интерлейкина-17 (ИЛ-17) и интерлейкина-22 (ИЛ-22), что препятствует бактериальному клиренсу [72]. В исследованиях также показано, что грипп типа A значительно снижает продукцию интерлейкина-1β (ИЛ-1β), играющего роль в поляризации Th17 [73]. При присоединении бактериальной инфекции, вызванной
Заключение
Инфицирование вирусом гриппа может способствовать развитию бактериальных осложнений сразу несколькими способами, включая повышение бактериальной адгезии, нарушение иммунных реакций и разрушение клеток и тканей, обеспечивающее распространение бактерий и развитие инвазивной инфекции. Бактериальные осложнения гриппа утяжеляют течение заболевания и ухудшают клинический исход. Исходя из этого, специалистам необходимо лучше понимать механизмы взаимодействия между вирусами, бактериями и макроорганизмом, а также патогенез бактериальных осложнений гриппа, особенно в свете повышенной резистентности бактерий к антибиотикам и их способности адаптироваться и уклоняться от индуцированного вакциной иммунитета.
КОНФЛИКТ ИНТЕРЕСОВ. Авторы статьи подтвердили отсутствие конфликта интересов, о котором необходимо сообщить.
CONFLICT OF INTERESTS. Not declared.
Литература/References
- Клинические рекомендации «Грипп у взрослых» (утв. Минздравом России, 2021 г.): https://www.rnmot.ru/public/uploads/RNMOT/clinical/2021/КР%20грипп.pdf. [Clinical recommendations «Influenza in adults» (utv. Minzdravom Rossii, 2021g.): https://www.rnmot.ru/public/uploads/RNMOT/clinical/2021/КР%20грипп.pdf.]
- World Health Organization. Non-pharmaceutical public health measures for mitigating the risk and impact of epidemic and pandemic influenza; 2019. Licence: CC BY-NC-SA 3.0 IGO.
- Mammas I. N., Spandidos D. A. Paediatric Virology in the Hippocratic Corpus // Exp Ther Med. 2016; 12 (2): 541-549. DOI: 10.3892/etm.2016.3420.
- Taubenberger J. K., Morens D. M. Influenza: The Once and Future Pandemic // Public Health Rep. 2010; 125 (Suppl 3): 16-26.
- Barnett R. Influenza // Lancet. 2019; 393 (10170): 396. DOI: 10.1016/S0140-6736(19)30148-5.
- Keynes M. The aching head and increasing blindness of Queen Mary I // J Med Biogr. 2000; 8 (2): 102-109. DOI: 10.1177/096777200000800207.
- Брико Н. И. 100 лет пандемии: уроки истории. Новый этап вакцинопрофилактики // Эпидемиология и вакцинопрофилактика. 2018. Т. 17. № 4 (101). С. 68-75. [Briko N. I. 100 years of the pandemic: the lessons of history. New stage of vaccinal prevention // Epidemiologiya i vaktsinoprofilaktika. 2018. T. 17. № 4 (101). P. 68-75.]
- Vasold M. The influenza pandemic of 1782, with special reference to its occurrence in the Imperial City of Nuremberg // Wurzbg Medizinhist Mitt. 2011; 30: 386-417.
- Широких К. Е., Мазурок О. И. История эпидемий гриппа // Медицинские технологии. Оценка и выбор. 2015; 3 (21): 73-77. [Shirokikh K. Ye., Mazurok O. I. History of influenza epidemics // Meditsinskiye tekhnologii. Otsenka i vybor. 2015; 3 (21): 73-77.]
- Gómez L., Gómez L. A. A century after the 'Spanish flu’: Role of the Great War and the knowledge about the genome as a tool for the control of influenza // Biomedica. 2019; 39 (1): 17-21. DOI: 10.7705/biomedica.v39i1.4884.
- Barry J. M. The Great Influenza: the Epic Story of the Deadliest Plague in History. First. New York: Viking; 2004.
- Humphreys M. The influenza of 1918: Evolutionary perspectives in a historical context // Evol Med Public Health. 2018; 2018 (1): 219-229. DOI: 10.1093/emph/eoy024.
- Васильев К. К., Васильева Е. Г. Из истории борьбы с испанской болезнью в Советской России // Бюллетень Национального научно-исследовательского института общественного здоровья имени Н. А. Семашко. 2021; 3: 10-15. [Vasil'yev K. K., Vasil'yeva Ye. G. From the history of the fight against Spanish disease in Soviet Russia // Byulleten' Natsional'nogo nauchno-issledovatel'skogo instituta obshchestvennogo zdorov'ya imeni N. A. Semashko. 2021; 3: 10-15.]
- Щелканов М. Ю., Колобухина Л. В., Львов Д. К. Грипп: история, клиника, патогенез // Лечащий Врач. 2011; 10: 33-38. [Shchelkanov M. Yu., Kolobukhina L. V., L'vov D. K. Influenza: history, clinic, pathogenesis // The Lechaschi Vrach Journal. 2011; 10: 33-38.]
- Ziegler T., Mamahit A., Cox N. J. 65 years of influenza surveillance by a World Health Organization-coordinated global network // Influenza Other Respir Viruses. 2018; 12 (5): 558-565. DOI: 10.1111/irv.12570.
- Monto A. S., Fukuda K. Lessons From Influenza Pandemics of the Last 100 Years // Clin Infect Dis. 2020; 70 (5): 951-957. DOI: 10.1093/cid/ciz803.
- Lai S., Qin Y., Cowling B. J., Ren X., Wardrop N. A., Gilbert M., Tsang T. K., Wu P., Feng L., Jiang H., Peng Z., Zheng J., Liao Q., Li S., Horby P. W., Farrar J. J., Gao G. F., Tatem A. J., Yu H. Global epidemiology of avian influenza A H5N1 virus infection in humans, 1997-2015: a systematic review of individual case data // Lancet Infect Dis. 2016; 16 (7): e108-e118. DOI: 10.1016/S1473-3099(16)00153-5.
- Ильичева Т. Н. Две пандемии XXI века: COVID-19 и «свиной» грипп 2009 // Медицинская иммунология. 2020; 6 (22): 1035-1044. [Il'icheva T. N. Two pandemics of the 21st century: COVID-19 and swine flu 2009 // Meditsinskaya immunologiya. 2020; 6 (22): 1035-1044]
- Khandaker G., Dierig A., Rashid H., King C., Heron L., Booy R. Systematic review of clinical and epidemiological features of the pandemic influenza A (H1N1) 2009 // Influenza Other Respir Viruses. 2011; 5 (3): 148-56. DOI: 10.1111/j.1750-2659.2011.00199.x.
- Carrat F., Vergu E., Ferguson N. M., Lemaitre M., Cauchemez S., Leach S., Valleron A. J. Time lines of infection and disease in human influenza: a review of volunteer challenge studies // Am J Epidemiol. 2008; 167 (7): 775-785. DOI: 10.1093/aje/kwm375.
- Krammer F., Smith G. J. D., Fouchier R. A. M., Peiris M., Kedzierska K., Doherty P. C., Palese P., Shaw M. L., Treanor J., Webster R. G., García-Sastre A. Influenza // Nat Rev Dis Primers. 2018; 4 (1): 3. DOI: 10.1038/s41572-018-0002-y.
- Keilman L. J. Seasonal Influenza (Flu) // Nurs Clin North Am. 2019; 54 (2): 227-243. DOI: 10.1016/j.cnur.2019.02.009.
- Uyeki T. M., Bernstein H. H., Bradley J. S., Englund J. A., File T. M., Fry A. M., Gravenstein S., Hayden F. G., Harper S. A., Hirshon J. M., Ison M. G., Johnston B. L., Knight S. L., McGeer A., Riley L. E., Wolfe C. R., Alexander P. E., Pavia A. T. Clinical Practice Guidelines by the Infectious Diseases Society of America: 2018 Update on Diagnosis, Treatment, Chemoprophylaxis, and Institutional Outbreak Management of Seasonal Influenza // Clin Infect Dis. 2019; 68 (6): 895-902. DOI: 10.1093/cid/ciy874.
- Yokomichi H., Mochizuki M., Lee J. J., Kojima R., Yokoyama T., Yamagata Z. Incidence of hospitalisation for severe complications of influenza virus infection in Japanese patients between 2012 and 2016: a cross-sectional study using routinely collected administrative data // BMJ Open. 2019; 9 (1): e024687. DOI: 10.1136/bmjopen-2018-024687.
- Taubenberger J. K., Morens D. M. The pathology of influenza virus infections // Annu Rev Pathol. 2008; 3: 499-522. DOI: 10.1146/annurev.pathmechdis.3.121806.154316.
- Rothberg M. B., Haessler S. D., Brown R. B. Complications of viral influenza // Am J Med. 2008; 121 (4): 258-264. DOI: 10.1016/j.amjmed.2007.10.040.
- Rothberg M. B., Haessler S. D. Complications of seasonal and pandemic influenza // Crit Care Med. 2010; 38 (4 Suppl): e91-97. DOI: 10.1097/CCM.0b013e3181c92eeb.
- Волощук Л. В., Го А. А., Писарева М. М., Гужов Д. А., Бичурина М. А., Петрова П. А. Клинико-лабораторная характеристика гриппозной инфекции у госпитализированных взрослых больных в эпидсезон 2018-2019 гг. // Инфекция и иммунитет. 2021; 11 (1): 191-196. DOI: 10.15789/2220-7619-CAL-1467. [Voloshchuk L. V., Go A. A., Pisareva M. M., Guzhov D. A., Bichurina M. A., Petrova P. A. Clinical and laboratory characteristics of influenza infection in hospitalized adult patients in the epidemiological season 2018-2019 gg. // Infektsiya i immunitet. 2021; 11 (1): 191-196. DOI: 10.15789/2220-7619-CAL-1467.]
- MacIntyre C. R., Chughtai A. A., Barnes M., Ridda I., Seale H., Toms R., Heywood A. The role of pneumonia and secondary bacterial infection in fatal and serious outcomes of pandemic influenza a(H1N1)pdm09 // BMC Infect Dis. 2018; 18 (1): 637. DOI: 10.1186/s12879-018-3548-0.
- Gupta R. K., George R., Nguyen-Van-Tam J. S. Bacterial pneumonia and pandemic influenza planning // Emerg Infect Dis. 2008; 14 (8): 1187-1192. DOI: 10.3201/eid1408.070751.
- Madhi S. A., Klugman K. P., Vaccine Trialist Group. A role for Streptococcus pneumoniae in virus-associated pneumonia // Nat Med. 2004; 10 (8): 811-813. DOI: 10.1038/nm1077.
- Brundage J. F., Shanks G. D. Deaths from bacterial pneumonia during 1918-19 influenza pandemic // Emerg Infect Dis. 2008; 14 (8): 1193-1199. DOI: 10.3201/eid1408.071313.
- Morris D. E., Cleary D. W., Clarke S. C. Secondary Bacterial Infections Associated with Influenza Pandemics // Front Microbiol. 2017; 8: 1041. DOI: 10.3389/fmicb.2017.01041.
- Rice T. W., Rubinson L., Uyeki T. M., Vaughn F. L., John B. B., Miller R. R. 3rd, Higgs E., Randolph A. G., Smoot B. E., Thompson B. T., NHLBI ARDS Network. Critical illness from 2009 pandemic influenza A virus and bacterial coinfection in the United States // Crit Care Med. 2012; 40 (5): 1487-1498. DOI: 10.1097/CCM.0b013e3182416f23.
- Centers for Disease Control and Prevention (CDC). Bacterial coinfections in lung tissue specimens from fatal cases of 2009 pandemic influenza A (H1N1) – United States, May-August 2009 // MMWR Morb Mortal Wkly Rep. 2009; 58 (38): 1071-1074.
- Weinberger D. M., Simonsen L., Jordan R., Steiner C., Miller M., Viboud C. Impact of the 2009 influenza pandemic on pneumococcal pneumonia hospitalizations in the United States // J Infect Dis. 2012; 205 (3): 458-465. DOI: 10.1093/infdis/jir749.
- Hooper L. V., Littman D. R., Macpherson A. J. Interactions between the microbiota and the immune system // Science. 2012; 336 (6086): 1268-1273. DOI: 10.1126/science.1223490.
- Cauley L. S., Vella A. T. Why is coinfection with influenza virus and bacteria so difficult to control? // Discov Med. 2015; 19 (102): 33-40.
- Rizzo C., Caporali M. G., Rota M. C. Pandemic influenza and pneumonia due to Legionella pneumophila: a frequently underestimated coinfection // Clin Infect Dis. 2010; 51 (1): 115. DOI: 10.1086/653444.
- Chertow D. S., Memoli M. J. Bacterial coinfection in influenza: a grand rounds review // JAMA. 2013; 309 (3): 275-282. DOI: 10.1001/jama.2012.194139.
- Cruz C. S. D., Wunderink R. G. Respiratory viral and atypical pneumonias // Clin Chest Med. 2017; 38 (1): xiii-xiv. DOI: 10.1016/j.ccm.2016.12.001.
- Yang M., Gao H., Chen J., Xu X., Tang L., Yang Y., Liang W., Yu L., Sheng J., Li L. Bacterial coinfection is associated with severity of avian influenza A (H7N9), and procalcitonin is a useful marker for early diagnosis // Diagn Microbiol Infect Dis. 2016; 84 (2): 165-169. DOI: 10.1016/j.diagmicrobio.2015.10.018.
- Peltola V. T., Murti K. G., McCullers J. A. Influenza virus neuraminidase contributes to secondary bacterial pneumonia // J Infect Dis. 2005; 192 (2): 249-257. Doi: 10.1086/430954.
- Aebi T., Weisser M., Bucher E., Hirsch H. H., Marsch S., Siegemund M. Co-infection of Influenza B and Streptococci causing severe pneumonia and septic shock in healthy women // BMC Infect Dis. 2010; 10: 308. DOI: 10.1186/1471-2334-10-308.
- Плехова Н. Г., Сомова Л. М. Современные представления о механизмах входа вирусов в клетку // Успехи современной биологии. 2009; 1 (129): 39-50. [Plekhova N. G., Somova L. M. Modern ideas about the mechanisms of virus entry into the cell // Uspekhi sovremennoy biologii. 2009; 1 (129): 39-50.]
- Samji T. Influenza A: understanding the viral life cycle // Yale J Biol Med. 2009; 82 (4): 153-159.
- Бревнов В. В. Формирование и рН-индуцированное разрушение слоя матриксного белка М1 вируса гриппа А. Диссертация на соискание учёной степени кандидата физико-математических наук / Московский физико-технический институт. М., 2017. [Brevnov V. V. Formation and pH-induced destruction of the M1 matrix protein layer of the influenza A virus. Dissertatsiya na soiskaniye uchonoy stepeni kandidata fiziko-matematicheskikh nauk / Moskovskiy fiziko-tekhnicheskiy institut. M., 2017.]
- Сорокин Е. В. Эпитопное картирование молекулы гемагглютинина вирусов гриппа в ямагатской и викторианской эволюционных линий с использованием моноклональных антител. Диссертация на соискание учёной степени кандидата биологических наук / Научно-исследовательский институт гриппа им. А.А. Смородинцева. СПб, 2021. [Sorokin Ye. V. Epitope mapping of the hemagglutinin molecule of influenza viruses in the Yamagata and Victorian evolutionary lines using monoclonal antibodies. Dissertatsiya na soiskaniye uchonoy stepeni kandidata biologicheskikh nauk / Nauchno-issledovatel'skiy institut grippa im. A. A. Smorodintseva. SPb, 2021.]
- Shinya K., Ebina M., Yamada S., Ono M., Kasai N., Kawaoka Y. Avian flu: influenza virus receptors in the human airway // Nature. 2006; 440 (7083): 435-436. DOI: 10.1038/440435a.
- Zambon M. C. The pathogenesis of influenza in humans // Rev Med Virol. 2001; 11 (4): 227-241. DOI: 10.1002/rmv.319.
- Baum L. G., Paulson J. C. The N2 neuraminidase of human influenza virus has acquired a substrate specificity complementary to the hemagglutinin receptor specificity // Virology. 1991; 180 (1): 10-15. DOI: 10.1016/0042-6822(91)90003-t.
- Conenello G. M., Palese P. Influenza A virus PB1-F2: a small protein with a big punch // Cell Host Microbe. 2007; 2 (4): 207-209. DOI: 10.1016/j.chom.2007.09.010.
- Lee P. H., Bird N., MacKenzie-Kludas C., Mansell A., Kedzierska K., Brown L., McAuley J. Induction of memory cytotoxic T cells to influenza A virus and subsequent viral clearance is not modulated by PB1-F2-dependent inflammasome activation // Immunol Cell Biol actions Search in PubMed Search in NLM Catalog Add to Search. 2016; 94 (5): 439-446. DOI: 10.1038/icb.2015.115.
- Щелканов М. Ю., Попов А. Ф., Симакова А. И., Зенин И. В., Прошина Е. С., Кириллов И. М., Дмитриенко К. А., Шевчук Д. В. Патогенез гриппа: механизмы модуляции белками возбудителя // Журнал инфектологии. 2015; 7 (2): 31-46. [Shchelkanov M. Yu., Popov A. F., Simakova A. I., Zenin I. V., Proshina Ye. S., Kirillov I. M., Dmitriyenko K. A., Shevchuk D. V. Influenza pathogenesis: mechanisms of modulation by pathogen proteins // Zhurnal infektologii. 2015; 7 (2): 31-46.]
- Балмасова И. П., Малова Е. С., Сепиашвили Р. И. Вирусно-бактериальные коинфекции как глобальная проблема современной медицины // Вестник Российского университета дружбы народов. Серия: Медицина. 2018; 1 (22): 29-42. [Balmasova I. P., Malova Ye. S., Sepiashvili R. I. Viral-bacterial coinfections as a global problem of modern medicine. // Vestnik Rossiyskogo universiteta druzhby narodov. Seriya: Meditsina. 2018; 1 (22): 29-42.]
- Хаитов Р. М., Пинегин Б. В., Пащенков М. В. Эпителиальные клетки дыхательных путей как равноправные участники врожденного иммунитета и потенциальные мишени для иммунотропных средств // Иммунология. 2020; 41 (2): 107-113. DOI: 10.33029/0206-4952-2020-41-2-107-113. [Khaitov R. M., Pinegin B. V., Pashchenkov M. V. Epithelial cells of the respiratory tract as equal participants in innate immunity and potential targets for immunotropic drugs // Immunologiya. 2020; 41 (2): 107-113. DOI: 10.33029/0206-4952-2020-41-2-107-113.]
- Sharma L., Feng J., Britto C. J., Dela Cruz C. S. Mechanisms of Epithelial Immunity Evasion by Respiratory Bacterial Pathogens // Front Immunol. 2020; 11: 91. DOI: 10.3389/fimmu.2020.00091.
- Pittet L. A., Hall-Stoodley L., Rutkowski M. R., Harmsen A. G. Influenza virus infection decreases tracheal mucociliary velocity and clearance of Streptococcus pneumoniae // Am J Respir Cell Mol Biol. 2010; 42 (4): 450-460. DOI: 10.1165/rcmb.2007-0417OC.
- Selinger D. S., Reed W. P., McLaren L. C. Model for studying bacterial adherence to epithelial cells infected with viruses // Infect Immun. 1981; 32 (2): 941-944. DOI: 10.1128/iai.32.2.941-944.1981.
- Manna S., Baindara P., Mandal S. M. Molecular pathogenesis of secondary bacterial infection associated to viral infections including SARS-CoV-2 // J Infect Public Health. 2020; 13 (10): 1397-1404. DOI: 10.1016/j.jiph.2020.07.003.
- Peltola V. T., McCullers J. A. Respiratory viruses predisposing to bacterial infections: role of neuraminidase // Pediatr Infect Dis J. 2004; 23 (1 Suppl): S87-97. DOI: 10.1097/01.inf.0000108197.81270.35.
- Мальцева Д. В., Полозников А. А., Артюшенко В. Г. Избирательное изменение экспрессии α-субъединиц интегринов в клетках кишечного эпителия Caco-2 при гипоксии в условиях микроциркуляции // Вестник РГМУ. 2020; (6): 23–31. DOI: 10.24075/vrgmu.2020.078. [Mal'tseva D. V., Poloznikov A. A., Artyushenko V. G. Selective change in the expression of integrin α-subunits in Caco-2 cells of the intestinal epithelium during hypoxia under microcirculation conditions // Vestnik RGMU. 2020; (6): 23-31. DOI: 10.24075/vrgmu.2020.078.]
- Smith A. M., McCullers J. A. Secondary bacterial infections in influenza virus infection pathogenesis // Curr Top Microbiol Immunol. 2014; 385: 327-356. DOI: 10.1007/82_2014_394.
- Cundell D. R., Gerard N. P., Gerard C., Idanpaan-Heikkila I., Tuomanen E. I. Streptococcus pneumoniae anchor to activated human cells by the receptor for platelet-activating factor // Nature. 1995; 377 (6548): 435-438. DOI: 10.1038/377435a0.
- Van der Sluijs K. F., van der Poll T., Lutter R., Juffermans N. P., Schultz M. J. Bench-to-bedside review: bacterial pneumonia with influenza — pathogenesis and clinical implications // Crit Care. 2010; 14 (2): 219. DOI: 10.1186/cc8893.
- McCullers J. A., Iverson A. R., McKeon R., Murray P. J. The platelet activating factor receptor is not required for exacerbation of bacterial pneumonia following influenza // Scand J Infect Dis. 2008; 40 (1): 11-17. DOI: 10.1080/00365540701477568.
- Kalil A. C., Thomas P. G. Influenza virus-related critical illness: pathophysiology and epidemiology // Crit Care. 2019; 23 (1): 258. DOI: 10.1186/s13054-019-2539-x.
- Joseph C., Togawa Y., Shindo N. Bacterial and viral infections associated with influenza // Influenza Other Respir Viruses. 2013; 7 Suppl 2 (Suppl 2): 105-113. DOI: 10.1111/irv.12089.
- Sun K., Metzger D. W. Inhibition of pulmonary antibacterial defense by interferon-gamma during recovery from influenza infection // Nat Med. 2008; 14 (5): 558-564. DOI: 10.1038/nm1765.
- Sharma-Chawla N., Sender V., Kershaw O., Gruber A. D., Volckmar J., Henriques-Normark B., Stegemann-Koniszewski S., Bruder D. Influenza A Virus Infection Predisposes Hosts to Secondary Infection with Different Streptococcus pneumoniae Serotypes with Similar Outcome but Serotype-Specific Manifestation // Infect Immun. 2016; 84 (12): 3445-3457. DOI: 10.1128/IAI.00422-16.
- Schoenborn J. R., Wilson C. B. Regulation of interferon-gamma during innate and adaptive immune responses // Adv Immunol. 2007; 96: 41-101. DOI: 10.1016/S0065-2776(07)96002-2.
- Mulcahy M. E., McLoughlin R. M. Staphylococcus aureus and Influenza A Virus: Partners in Coinfection // mBio. 2016; 7 (6): e02068-16. DOI: 10.1128/mBio.02068-16.
- Robinson K. M., Choi S. M., McHugh K. J., Mandalapu S., Enelow R. I., Kolls J. K., Alcorn J. F. Influenza A exacerbates Staphylococcus aureus pneumonia by attenuating IL-1β production in mice // J Immunol. 2013; 191 (10): 5153-5159. DOI: 10.4049/jimmunol.1301237.
- Shahangian A., Chow E. K., Tian X., Kang J. R., Ghaffari A., Liu S. Y., Belperio J. A., Cheng G., Deng J. C. Type I IFNs mediate development of postinfluenza bacterial pneumonia in mice // J Clin Invest. 2009; 119 (7): 1910-1920. DOI: 10.1172/JCI35412.
- Абатуров А. Е., Никулина А. А. Развитие иммунного ответа при стафилококковой пневмонии (часть 3) // Здоровье ребенка. 2017; 4 (12): 540-555. [Abaturov A. Ye., Nikulina A. A. Development of the immune response in staphylococcal pneumonia (part 3) // Zdorov'ye rebenka. 2017; 4 (12): 540-555]
- Mulcahy M. E., McLoughlin R. M. Staphylococcus aureus and Influenza A Virus: Partners in Coinfection // mBio. 2016; 7 (6): e02068-16. DOI: 10.1128/mBio.02068-16.
В. В. Никифоров1, ORCID: 0000-0002-2205-9674, v.v.nikiforov@gmail.com
М. З. Шахмарданов1, ORCID: 0000-0002-3168-2169, mur2025@rambler.ru
М. С. Застрожин2, 3, ORCID: 0000-0002-3964-9726, mszastrozhin@gmail.com
1 Федеральное государственное автономное образовательное учреждение высшего образования Российский национальный исследовательский медицинский университет имени Н. И. Пирогова Министерства здравоохранения Российской Федерации; 117997, Россия, Москва, ул. Островитянова, 1
2 Государственное бюджетное учреждение здравоохранения Московский научно-практический центр наркологии Департамента здравоохранения города Москвы; 109390, Россия, Москва, ул. Люблинская, 37/1
3 Федеральное государственное бюджетное образовательное учреждение дополнительного профессионального образования Российская медицинская академия непрерывного профессионального образования Министерства здравоохранения Российской Федерации; 125993, Россия, Москва, ул. Баррикадная, 2/1, стр. 1
Сведения об авторах:
Скрябина Анна Александровна, ассистент кафедры инфекционных болезней и эпидемиологии лечебного факультета Федерального государственного автономного образовательного учреждения высшего образования Российский национальный исследовательский медицинский университет имени Н. И. Пирогова Министерства здравоохранения Российской Федерации; 117997, Россия, Москва, ул. Островитянова, 1;
Никифоров Владимир Владимирович, д.м.н., профессор, заведующий кафедрой инфекционных болезней и эпидемиологии лечебного факультета Федерального государственного автономного образовательного учреждения высшего образования Российский национальный исследовательский медицинский университет имени Н. И. Пирогова Министерства здравоохранения Российской Федерации; 117997, Россия, Москва, ул. Островитянова, 1; v.v.nikiforov@gmail.com
Шахмарданов Мурад Зияудинович, д.м.н., профессор кафедры инфекционных болезней и эпидемиологии лечебного факультета Федерального государственного автономного образовательного учреждения высшего образования Российский национальный исследовательский медицинский университет имени Н. И. Пирогова Министерства здравоохранения Российской Федерации; 117997, Россия, Москва, ул. Островитянова, 1; mur2025@rambler.ru
Застрожин Михаил Сергеевич, д.м.н., ведущий научный сотрудник Государственного бюджетного учреждения здравоохранения Московский научно-практический центр наркологии Департамента здравоохранения города Москвы; 109390, Россия, Москва, ул. Люблинская, 37/1; ассистент кафедры наркологии Федерального государственного бюджетного образовательного учреждения дополнительного профессионального образования Российская медицинская академия непрерывного профессионального образования Министерства здравоохранения Российской Федерации; 125993, Россия, Москва, ул. Баррикадная, 2/1, стр. 1;
Information about the authors:
Anna A. Skryabina, Assistant of the Department of Infectious Diseases and Epidemiology of the Medical Faculty at the Federal State Autonomous Educational Institution of Higher Education N. I. Pirogov Russian National Research Medical University of the Ministry of Health of the Russian Federation; 1 Ostrovityanova str., Moscow, 117997, Russia; anna.skryabina.85@mail.ru
Vladimir V. Nikiforov, Dr. of Sci. (Med.), Professor, Head of the Department of Infectious Diseases and Epidemiology of the Medical Faculty at the Federal State Autonomous Educational Institution of Higher Education N. I. Pirogov Russian National Research Medical University of the Ministry of Health of the Russian Federation; 1 Ostrovityanova str., Moscow, 117997, Russia; v.v.nikiforov@gmail.com
Murad Z. Shakhmardanov, Dr. of Sci. (Med.), Professor of the Department of Infectious Diseases and Epidemiology of the Medical Faculty at the Federal State Autonomous Educational Institution of Higher Education N. I. Pirogov Russian National Research Medical University of the Ministry of Health of the Russian Federation; 1 Ostrovityanova str., Moscow, 117997, Russia; mur2025@rambler.ru
Mikhail S. Zastrozhin, Dr. of Sci. (Med.), Leading Researcher of the State Budgetary Healthcare Institution Moscow Research and Practical Center of Addictions of the Department of Health of the City of Moscow; 37/1 Lublinskaya str., Moscow, 109390, Russia; Assistant of the Department of Narcology at the Federal State Budgetary Educational Institution of Additional Professional Education Russian Medical Academy of Continuing Professional Education of the Ministry of Health of the Russian Federation; 2/1, p. 1 Barrikadnaya str., Moscow, 125993, Russia; mszastrozhin@gmail.com
Бактериальные осложнения гриппа (обзор литературы)/ А. А. Скрябина, В. В. Никифоров, М. З. Шахмарданов, М. С. Застрожин
Для цитирования: Скрябина А. А., Никифоров В. В., Шахмарданов М. З., Застрожин М. С. Бактериальные осложнения гриппа (обзор литературы) // Лечащий Врач. 2022; 11 (25): 48-54. DOI: 10.51793/OS.2022.25.11.008
Теги: вирус гриппа, дыхательные пути, воспаление, тяжелое течение
Купить номер с этой статьей в pdf