Острые респираторные инфекции (ОРИ) встречаются достаточно часто в группе детей младшего возраста. В большинстве случаев они повторяются несколько раз в год, и, несмотря на то, что ОРИ в целом не тяжелые и спонтанно разрешаются в течение нескольких дней, это может приводить к серьезным медицинским, социальным и экономическим проблемам для ребенка, его семьи и общества [1–3]. Иммунологическая незрелость, генетические особенности и факторы окружающей среды, такие как воздействие загрязненного воздуха, посещение детского сада, отсутствие грудного вскармливания и малоподвижный образ жизни, являются факторами, способствующими частым ОРИ [3]. Для снижения общего бремени ОРИ настоятельно рекомендуется профилактика эпизодов инфекции путем устранения экологических факторов и систематического использования имеющихся вакцин. К сожалению, полная элиминация экологических факторов очень сложна и в некоторых случаях практически невозможна [2, 3]. Выбор вакцин, предотвращающих все респираторные заболевания, также ограничен. Полисахаридные пневмококковые конъюгированные вакцины защищают от не более 13 пневмококковых серотипов, хотя более 90 серотипов могут вызвать заболевание [4]. Гриппозные вакцины эффективны не более чем у 80% вакцинированных детей, при этом происходит значительное снижение эффективности при несоответствии между циркулирующими жизненно важными штаммами и штаммами, включенными в вакцину [5]. Для улучшения защиты предложено повышение активности иммунной системы [6].
Применение иммуномодуляторов имеет более чем вековую клиническую историю, причем публикации, исследующие их эффективность, датируются по крайней мере 1950-ми гг. Наиболее изученными иммуномодуляторами на сегодняшний день являются бактериальные лизаты — иммуномодуляторы микробного происхождения. Это комплексные РАМР-содержащие препараты, оказывающие влияние на врожденную иммунную систему преимущественно через сигнальные образраспознающие рецепторы, а эффективность использования данной группы препаратов связана не только с активацией эффекторов врожденного иммунитета, но и с инициацией формирования адаптивного иммунитета [6, 7]. Бактериальные лизаты способны осуществить специфическую и неспецифическую защиту организма посредством стимуляции иммунного ответа Th1-типа, более зрелого, по сравнению с ответом Тh2-типа, с которым дети рождаются. Под влиянием микробной стимуляции у ребенка происходит становление ответа Th1-типа, недостаток которого в настоящее время может быть связан с относительной редкостью бактериальных инфекций и широким неоправданным применением антибиотиков, подавляющих комменсальную флору, нерациональное использование жаропонижающих препаратов при любом повышении температуры, также подавляющих продукцию цитокинов, обусловливающих ответ Th1-типа: интерферона (ИНФ)-γ, ИЛ-1 и ИЛ-2, ФНО-α. Подавление ответа Th1-типа препятствует выработке более стойкого ответа на инфекцию и формированию иммунологической памяти [8, 9].
Одним из современных высокоэффективных бактериальных иммуномодуляторов является ОМ-85 (Бронхо-мунал), содержащий лизаты 21 штамма 8 наиболее частых бактериальных возбудителей респираторных заболеваний (Streptococcus pneumoniae, Haemophilus influenzae, Klebsiella pneumoniae, Klebsiella ozlanae, Staphylococcuc aureus, Streptococcus viridans, Streptococcus pyogenes, Moraxella catarrhalis) [10]. На сегодняшний день проведено около 300 клинических исследований (из них более 53 — контролируемые рандомизированные (4851 пациент)), а также систематических обзоров, посвященных изучению эффективности и безопасности данного препарата в лечении и профилактике острых респираторных инфекций у детей [11]. Препарат применяют внутрь в капсулах, содержащих 3,5 мг лиофилизированного экстракта для детей (Бронхо-мунал П) и 7 мг для взрослых [10].
Защитный эффект ОМ-85 реализует в основном из-за своей модулирующей роли на клеточный и гуморальный ответы. В исследованиях показано, что ОМ-85 индуцирует синергический TLR2/6- и TLR9-зависимый врожденный иммунитет [6, 8, 9]. Он активирует дендритные клетки слизистой оболочки желудочно-кишечного тракта в бляшках Пейера, тем самым стимулируя активность как врожденных, так и адаптивных реакций иммунной системы. Развитие специфического иммунного ответа происходит при кооперации Т- и В-лимфоцитов, макрофагов или дендритных клеток, после попадания антигенстимулированных клеток с поверхностным IgA в лимфоидные органы [8]. Иммунопротекторное действие ОМ-85 опосредуется стимуляцией Th1-клеточного ответа, а также путем стимулирования синтеза иммуноглобулинов, в основном IgA В-лимфоцитами. В кишечнике лиофилизованные бактерии оказывают действие на пейеровы бляшки, тем самым активируя Т- и В-лимфоциты [7–9]. Иммунные клетки затем транспортируются с лимфой в лимфатические узлы брыжейки, чтобы созреть. Активированные иммунные клетки мигрируют в слизистую оболочку дыхательных путей и стимулируют врожденный и адаптивный иммунитет, а также выработку секреторных антител IgA в слизистой дыхательных путей [6, 9]. Антигены бактериальных лизатов, контактируя с макрофагами MALT-системы миндалин, респираторного и желудочно-кишечного трактов, в последующем презентируются лимфоцитами, в результате чего появляются клоны В-лимфоцитов, продуцирующие специфические антитела к возбудителям, антигены которых содержатся в препарате. Миграция В-лимфоцитов в другие лимфоидные образования MALT-системы и последующая их дифференциация в плазмоциты приводят к продукции специфического секреторного IgA и развитию эффективной местной иммунной защиты против основных возбудителей острых респираторных заболеваний. Также ОМ-85 влияет на клеточный ответ, повышает врожденный иммунитет в легких, стимулируя фагоцитарную активность, тем самым увеличивая уничтожение вторгшихся патогенов. Кроме того, показано, что ОМ-85 повышает экспрессию молекул адгезии [8] и CD-14-независимый путь активации лейкоцитов. Также в исследованиях продемонстрирован эффект ОМ-85 в отношении активации СD16+-клеток, повышении функциональной активности макрофагов, выработке ряда цитокинов и медиаторов (ИЛ-6, ИЛ-8, ИЛ-2, ИФН-γ). Одновременно происходит увеличение продукции ИФН-α, снижение уровней ИЛ-4, ФНО-α, а повышение уровня IgG усиливает межклеточные взаимодействия макрофагов, натуральных киллеров. Эти сдвиги можно интерпретировать как переключение иммунного ответа Th2-типа на Th1-тип [6, 8, 11, 12].
В ряде исследований подчеркивалась способность ОМ-85 вызывать иммуномодулирующие и защитные иммунные реакции против различных патогенов, включая грипп и респираторно-синцитиальный вирус, а также бактериальную суперинфекцию после гриппа, а также влияние на продукцию интерферонов типа I или опосредованную воспалением продукцию ИЛ-1. Показано, что ОМ-85 индуцировал продукцию ИФН-β и действовал как эффективный праймирующий агент, индуцирующий субстанциальные уровни proIL-1α и proIL-1β [12]. Противовирусное действие также может быть связано с индукцией образования и активности FoxP3+ Т-клеток, снижением Th2-клеточных цитокинов в пользу Th1-цитокинов. Показано, что ОМ-85 активирует несколько межклеточных сигнальных путей, включая Erk1/2, активированную митогеном протеинкиназу и NFkB. Таким образом, ОМ-85 повышал экспрессию β-дефензина, IgG и Ig A. В отношении защиты хозяина β-дефензин играет важную роль в распознавании микроорганизмов и маркировке их для фагоцитоза. Кроме того, β-дефензин влияет на экспрессию молекулы внутриклеточной адгезии (ICAM), которая действует как докинг-белок по меньшей мере для риновируса и может быть индуцирована OM-85 в фагоцитарных клетках [13]. ОМ-85 значительно уменьшал репликацию риновируса, увеличивал экспрессию вирусных взаимодействующих белков C1q-R и β-дефензина. Кроме того, ОМ-85 значительно снижал риновирусную индуцированную экспрессию ICAM-1 [13].
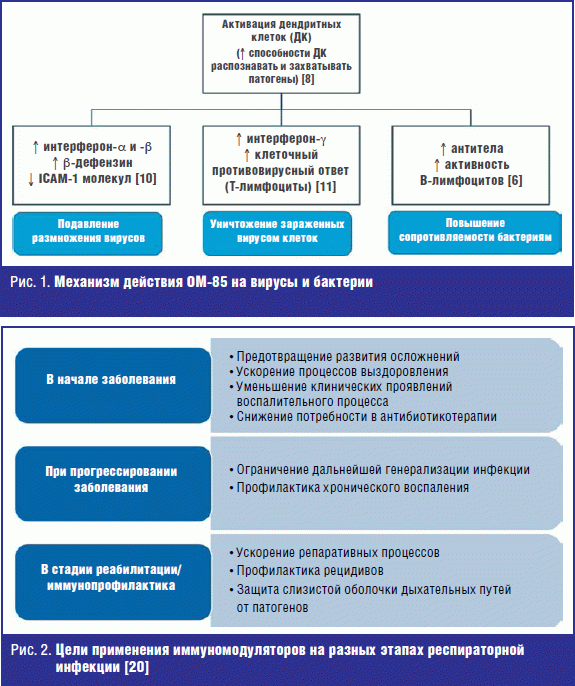
ОМ-85, кроме того, повышает функциональную активность альвеолярных макрофагов против инфекционных и опухолевых антигенов, NK-клеток «естественных, натуральных киллеров», уменьшает выработку IgE [6, 7, 9]. Схематично основные механизмы действия ОМ-85 обобщены на рис. 1.
ОМ-85 продемонстрировл эффективность в отношении различных форм ОРИ у детей. Терапия бактериальным лизатом снижала частоту [14], распространенность и/или продолжительность инфекций у детей с ОРИ в анамнезе по сравнению с плацебо [6, 7, 9] и по сравнению с пробиотической терапией [6]. Включение ОМ-85 в комплексную терапию острого бронхиолита у детей первых лет жизни позволило повысить эффективность терапии и сократить продолжительность болезни [15]. В исследовании детей с рецидивирующим тонзиллитом профилактика ОМ-85 улучшила исходы у большинства пациентов и, что немаловажно, сняла необходимость в хирургическом вмешательстве у значительной части пролеченных [16]. У детей с подострым синуситом профилактика ОМ-85 ускорила выздоровление и уменьшила количество инфекций, в то время как у детей с хроническим риносинуситом наблюдалось снижение симптоматики и снижение частоты приступов [17]. ОМ-85 также снижал частоту и распространенность инфекций у детей из закрытых коллективов. Также в этих исследованиях показано уменьшение необходимости в антибактериальной и симптоматической терапии, а также пропусков школы в связи с ОРИ. Важно отметить, что эффективность не зависела от совместного применения с антибактериальной терапией или вакциной против гриппа, при этом ОМ-85 давал дополнительную пользу с точки зрения невыходов на работу и распространенности инфекций в обоих случаях [17, 18].
Включение ОМ-85 в комплексную терапию респираторной инфекции детям с аллергией в анамнезе не только снижает частоту ОРВИ, но и приступы бронхообструкции на фоне заболевания [19]. У детей с бронхиальной астмой и частыми интеркуррентными острыми респираторными заболеваниями применение препарата способствовало клиническому улучшению в 68% наблюдений, сокращалась также заболеваемость ОРИ с явлениями бронхообструкции на 38%, количество тяжелых приступов удушья и годовая потребность ребенка в бронхолитической терапии. При этом наблюдалось увеличение уровня ИФН-γ, снижение общего IgЕ и циркулирующих иммунных комплексов в крови [19]. В настоящее время проводится новое поколение клинических исследований, позволяющих позиционировать неспецифический бактериальный лизат ОМ-85 в качестве потенциального средства, позволяющего контролировать бронхиальную астму, в том числе за счет снижения эпизодов ОРИ [6, 9].
ОМ-85 хорошо переносится и имеет частоту побочных явлений, сравнимую с таковой при применении плацебо в клинических испытаниях. Нежелательные явления в основном носят умеренный и преходящий характер, с управляемыми рисками. Этот профиль безопасности, по-видимому, является стабильным по своей природе и частоте в течение длительного использования [6, 7, 10, 13, 17].
ОМ-85 (Бронхо-мунал®) применяют как для лечения острого респираторного заболевания, так и с профилактической целью по 1 капсуле 1 раз в день детям с 6-месячного возраста. Профилактический курс — 10 дней в месяц в течение 3 месяцев. Начинать использование препаратов возможно как у здорового ребенка, так и во время очередного респираторного заболевания, продолжая курс после выздоровления (рис. 2).
В составе комплексной терапии острых инфекций дыхательных путей препарат применяют до исчезновения симптомов, но не менее 10 дней. Назначение препарата в остром периоде более эффективно в сочетании с этиотропными средствами. При проведении антибиотикотерапии Бронхо-мунал® следует принимать в сочетании с антибиотиками с начала лечения. Последующие 2 месяца возможно профилактическое применение препарата: курсами по 10 дней, интервал между курсами 20 дней. Эффект иммуномодуляторов системного действия (Бронхо-мунал®) сохраняется в течение 6 месяцев, что важно для определения интервала между курсами. У детей с частыми респираторными инфекциями показано проведение двух трехмесячных курсов по 10 дней каждый месяц [10].
Таким образом, применение бактериальных лизатов, в частности препарата Бронхо-мунал®, для лечения и профилактики острых респираторных заболеваний способствует снижению частоты респираторных инфекций, уменьшению длительности заболевания, снижению риска бактериальных осложнений и потребности в назначении антибиотиков, что обусловлено действием на системный и местный иммунитет и высокой иммуногенностью, в сочетании с хорошей переносимостью и низкой частотой нежелательных явлений.
Литература
- Toivonen L., Karppinen S., Schuez-Havupalo L., Teros-Jaakkola T., Vuononvirta J., Mertsola J., He Q., Waris M., Peltola V. Burden of recurrent respiratory tract infections in children: A prospective cohort study // Pediatr. Infect. Dis. J. 2016, 35, e362–e369. DOI: 10.1097/INF.0000000000001304.
- Simon A. K., Hollander G. A., McMichael A. Evolution of the immune system in humans from infancy to old age // Proc. Biol. Sci. 2015, 282, 20143085. DOI: 10.1098/rspb.2014.3085.
- Schaad U. B., Esposito S., Razi C. H. Diagnosis and management of recurrent respiratory tract infections in children: A practical guide // Arch. Pediatr. Infect. Dis. 2016, 4, 1–10.
- Principi N., Di Cara G., Bizzarri I., Isidori C., Borgia P., Mignini C. et al. Prevention of invasive pneumococcal disease: problems emerged after some years of the 13-valent pneumococcal conjugate vaccine use // Curr Infect Dis Rep. 2018; 20: 1a.
- Principi N., Esposito S. Protection of children against influenza: emerging problems // Hum Vaccin Immunother. 2018; 14: 750–757.
- Esposito S., Soto-Martinez M. E., Feleszko W., Jones M. H., Shen K. L., Schaad U. B. Nonspecific immunomodulators for recurrent respiratory tract infections, wheezing and asthma in children: A systematic review of mechanistic and clinical evidence // Curr. Opin. Allergy Clin. Immunol. 2018, 18, 198–209.
- Дронов И. А., Денисова А. Р. Бактериальный лизат ОМ-85: вопросы эффективности у детей и потенциальная роль в сдерживании роста антимикробной резистентности // Вопросы практической педиатрии. 2019; 14 (1): 76–83. DOI: 10.20953/1817–7646–2019–1–76–83.
- ПРИМА: педиатрические рекомендации по иммуномодулирующим препаратам в амбулаторной практике (консенсус). 2-е изд., перераб. и доп. М.: РГ-Пресс, 2017. 80 с.
- Kearney S. C., Dziekiewicz M., Feleszko W. Immunoregulatory and immunostimulatory responses of bacterial lysates in respiratory infections and asthma // Ann Allergy Asthma Immunol. 2015; 114: 364–369.
- Инструкция по применению лекарственного препарата для медицинского применения Бронхо-мунал®. Регистрационный номер: П N011632/01. https://www.sandoz.ru/products/broncho-munal#ui-id-3=0&ui-id-1=9.
- Yin J. et al. Broncho-Vaxom in pediatric recurrent respiratory tract infections: A systematic review and meta-analysis // International Immunopharmacology. 2018; 54: 198–209. https://doi.org/10.1016/j.intimp.2017.10.032.
- Dang A. T., Pasquali C., Ludigs K., Guarda G. OM-85 is an immunomodulator of interferon-b production and inflammasome activity // Sci Rep. 2017; 7: 43844.
- Roth M., Pasquali C., Stolz D., Tamm M. Broncho Vaxom (OM-85) modulates rhinovirus docking proteins on human airway epithelial cells via Erk1/2 mitogen activated protein kinase and cAMP // PLoS ONE. 2017; 12 (11): e0188010. https://doi.org/10.1371/journal.pone.0188010.
- Gu S., Wu C., Xie G. Efficacy of bacterial lysates in the adjuvant therapy for children with recurrent respiratory tract infections // Chin J Pract Pediatr. 2015; 30:207–210.
- Liu Y. W., Dong S. H., Zhan G. Y. et al. Analysis of the effect of bacterial lysate and the immunologic mechanism in treating infant bronchiolitis // Eur. Rev. Med. Pharmacol. Sci. 2017. Vol. 21, № 14, p. 3332–3336.
- Bitar M. A., Saade R. The role of OM-85 BV (Broncho-Vaxom) in preventing recurrent acute tonsillitis in children // Int J Pediatr Otorhinolaryngol. 2013; 77: 670–673.
- Triantafillou V., Workman A. D., Patel N. N. et al. Broncho-Vaxom (OM-85 BV) soluble components stimulate sinonasal innate immunity // Int Forum Allergy Rhinol. 2018; 00: 1–8.
- Esposito S., Marchisio P., Prada E. et al. Impact of a mixed bacterial lysate (OM-85 BV) on the immunogenicity, safety and tolerability of inactivated influenza vaccine in children with recurrent respiratory tract infection // Vaccine. 2014; 2: 2546–2552.
- Razi C. H., Harmanci K., Abaci A., Özdemir O., Hizli S., Renda R., Keskin F. The immunostimulant OM-85 BV prevents wheezing attacks in preschool children // J Allergy Clin Immunol. 2010, 126: 763–769.
- Косенко И. М. Иммуномодулирующая терапия заболеваний ротоглотки у детей // Детские инфекции. 2010. Т. 9. № 1.
Е. В. Фролкова, кандидат медицинских наук
ФГАОУ ВО Первый МГМУ им. И. М. Сеченова Минздрава России, Москва
1 Контактная информация: kolosovan@mail.ru
DOI: 10.26295/OS.2019.96.95.004
Обоснование использования бактериальных лизатов (ОМ-85) в лечении и профилактике респираторных инфекций у детей/ Н. Г. Колосова, Е. В. Фролкова
Для цитирования: Лечащий врач № 9/2019; Номера страниц в выпуске: 24-28
Теги: дыхательные пути, воспаление, дети, респираторные заболевания
Купить номер с этой статьей в pdf