Бронхиальная астма (БА) — это наиболее частое хроническое заболевание детского возраста и одна из основных причин детской смертности от хронических заболеваний. Обострение БА является частой причиной пропусков школы, поступления в отделение интенсивной терапии и госпитализации [1].
Для того чтобы выработать единый подход к диагностике и лечению БА, были созданы несколько важных международных рекомендаций: Национальная программа по обучению и профилактике бронхиальной астмы (NAEPP), Британское руководство по лечению астмы, Международный консенсус по астме у детей (ICON), Глобальная инициатива по лечению и профилактике бронхиальной астмы (GINA). GINA — это важный документ, определяющий дальнейшее направление диагностики, лечения и профилактики бронхиальной астмы, основанный на новейших достижениях в области медицины, фармакологии и молекулярной биологии. Многие национальные рекомендации, в том числе и рекомендации Союза педиатров России, практически полностью базируются на принципах Глобальной стратегии лечения и профилактики бронхиальной астмы.
Согласно новому определению, бронхиальная астма — это гетерогенное заболевание, которое характеризуется хроническим воспалением дыхательных путей и диагностируется по респираторным симптомам свистящего дыхания (визинга), одышки, стеснения в груди или кашля, вариабельных по длительности и интенсивности, в сочетании с обратимой обструкцией дыхательных путей. Диагностика БА должна основываться на анамнезе и характерной симптоматике, особенно это актуально для детей раннего возраста, а также на доказательстве обратимой обструкции дыхательных путей по тесту с бронходилататором или по другим тестам. Постановка тестов, подтверждающих диагноз БА, рекомендована до начала базисного лечения. Следует учесть, что на фоне базисной терапии, иногда достаточно длительной, не удается подтвердить обратимость и наличие скрытого бронхоспазма. Это не значит, что у больного нет БА. Если невозможно подтвердить диагноз БА с помощью теста с бронходилататором, то необходимо снова повторить этот тест позже или начать проводить пробное лечение для исключения или подтверждения диагноза БА. Назначение пробного базисного лечения может значительно облегчить диагностику и выбор дальнейшей тактики лечения.
Оценивая уровень контроля, БА подразделяют на хорошо контролируемую, частично контролируемую и плохо контролируемую. Критерии остались такие же, как в предыдущем издании GINA, — наличие дневных симптомов более чем 2 раза в неделю, ночные пробуждения из-за астмы, прием препаратов неотложной помощи более чем 2 раза в неделю и наличие любых нарушений деятельности вследствие БА. Однако оценка объема форсированного выдоха за первую секунду (ОФВ
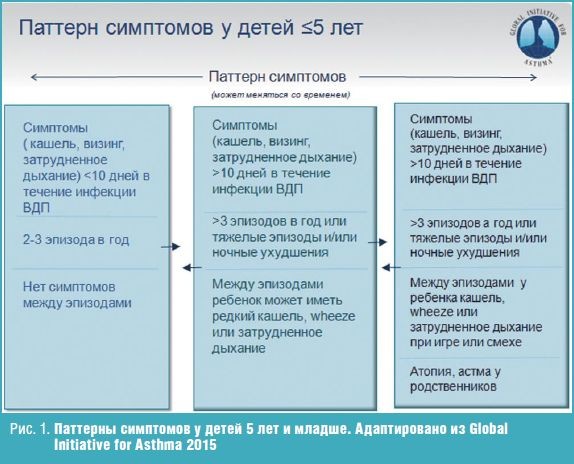
У многих пациентов БА начинается в раннем возрасте. В GINA-2015 акцентируется внимание на наличии у детей младше 5 лет трех паттернов свистящего дыхания (рис. 1). Первая группа детей — это дети с такими характерными симптомами, как кашель, затрудненное дыхание и визинг, которые длятся менее 10 дней в течение инфекции верхних дыхательных путей (ВДП), повторяются 2–3 раза в год, и данные симптомы отсутствуют между эпизодами затрудненного дыхания и/или визинга. Следующая группа включает пациентов, у которых длительность симптомов увеличена (> 10 дней в течение инфекции ВДП), частота эпизодов > 3 в год или тяжелые эпизоды и/или ночные ухудшения, между эпизодами ребенок может иметь редкий кашель, визинг или затрудненное дыхание. И третий паттерн — то же самое, как и в предыдущем случае, плюс отя��ощенная наследственность по атопии, или у ребенка уже есть проявления той или иной аллергической патологии. Характерные признаки БА у детей 5 лет и младше: кашель, визинг, затрудненное дыхание или одышка, снижение активности, положительный эффект от пробного лечения низкими дозами ингаляционными глюкокортикостероидами (иГКС) и бета-2-агонистами короткого действия (КДБА) (табл. 1).
Круг дифференциальной диагностики бронхиальной астмы у детей младшего возраста широк и требует тщательного сбора анамнеза и проведения дополнительных тестов. При наличии у ребенка младшего возраста кашля и визинга необходимо исключить рецидивирующие инфекции нижних дыхательных путей (НДП), бронхолегочную дисплазию, аномалии развития трахеи и бронхов, врожденные пороки сердца, гастроэзофагеальный рефлюкс, инородное тело, туберкулез, врожденные и наследственные заболевания, муковисцидоз, гипотиреоз, узелковый периартериит, объемные процессы в грудной клетке и целый ряд более редко встречающихся заболеваний (табл. 2).
Главная цель терапии больных бронхиальной астмой — это достижение контроля и управление бронхиальной астмой. Согласно схеме, приведенной в GINA-2015 для детей младше 5 лет, из терапии полностью исключены кромоны в связи с недостаточной эффективностью, но имеющие хороший профиль безопасности. Длительно действующие бета-2-агонисты (ДДБА) в комбинации с иГКС также исключены в связи с отсутствием в настоящее время достаточной доказательной базы по безопасности их использования в этой возрастной группе. На первой ступени следует использовать по требованию КДБА. На второй ступени — ежедневные низкие дозы иГКС или антагонистов лейкотриеновых рецепторов (АЛТР). Двигаясь step-up, на третьей ступени — двойная низкая доза иГКС или сочетание низких доз иГКС с АЛТР. И на четвертой ступени — увеличение дозы иГКС (рис. 2). В GINА-2014 года было введено такое понятие, как краткосрочная
Создание и широкое использование в первую очередь иГКС существенно повлияло на возможности достижения контроля течения астмы. иГКС, обладая мощным противовоспалительным действием, воздействуют на основные механизмы формирования БА. Но, несмотря на использование иГКС, у части больных все же не удается достигнуть контроля над течением заболевания. И данное обстоятельство диктует необходимость использовать в лечении БА препараты, относящиеся к другим фармакологическим группам. За последние 50 лет разрешены к использованию в лечении БА у детей только две новые группы препаратов: антилейкотриеновые препараты и анти-IgE-антитела.
В настоящее время в клинической практике широко используют высокие дозы иГКС через небулайзер в сочетании с небулированными формами КДБА при появлении обструкции на фоне респираторной вирусной инфекции. Помимо купирования бронхообструкции при вирус-индуцированном визинге предполагается получение и протективного эффекта иГКС для предотвращения последующих рецидивов визинга. Так, при рецидивирующих эпизодах острого визинга лечение высокими дозами иГКС (1600–2000 мкг/день по беклометазону, разделенной на 4 приема/день, 5–10 дней с начала вирусной респираторной инфекции или ухудшении астмы) ассоциировалось с некоторым улучшением клиники у новорожденных и маленьких детей [2–4]. По результатам других исследований данная тактика не привела к изменению эволюции формирования БА у детей из группы риска по аллергическим заболеваниям. Было проведено трехлетнее наблюдение за 301 новорожденным, получавшим будесонид 400 мкг/день или плацебо после первого эпизода визинга в течение 2 недель начиная с третьего дня каждого эпизода визинга. В результате не было получено различий в количестве бессимптомных дней или в необходимости назначения оральных кортикостероидов (ОКС) как в группе получавших иГКС, так и в группе плацебо [5].
В исследовании MIST изучали назначение иГКС при инфекции респираторного тракта у дошкольников с рецидивирующим визингом, риском развития БА и эпизодами визинга [6]. Сравнивался ежедневный прием низких доз будесонида в ингаляциях и эпизодический прием высоких доз будесонида в ингаляциях на ночь в течение 7 дней. Был получен одинаковый эффект при регулярном и эпизодическом приеме иГКС. Выбор схемы назначения иГКС (регулярный, интермиттирующий и режим по потребности) у детей с визингом в клинической практике до сих пор является предметом дискуссий.
Большинство исследований, оценивающих системные эффекты иГКС, брали за основу результаты, полученные у детей старше 5 лет. Международные согласительные документы утверждают, что у детей младшей возрастной группы, как и у старших детей, индивидуально подобранные дозы иГКС безопасны и потенциальный риск побочного действия обоснован их клинической эффективностью [7–9]. В целом низкие дозы иГКС не ассоциировались с любыми серьезными побочными системными эффектами в клинических исследованиях, поэтому эта терапия рассматривается как безопасная [3, 8–17]. Хотя существуют данные, указывающие на то, что высокие дозы ассоциировались с заметными системными эффектами (темповая задержка роста и влияние на гипоталамо-гипофизарно-надпочечниковую систему) даже в первый год терапии [3, 7–17]. Эти эффекты такие же, как и в исследованиях, проведенных у старших детей. Влияние на рост было накопительное при продолжении длительного лечения [18–20]. Дети, которые находились на лечении флутиказоном пропионатом в течение двух лет в возрасте двух или трех лет [7], догнали в росте своих сверстников через два года после прекращения терапии иГКС. Ретроспективный анализ показал, что у детей младше двух лет и при весе < 15 кг не был зафиксирован этот скачок в росте [21]. Согласно двум систематическим обзорам, опубликованным в кокрайновской библиотеке, дети с персистирующей БА, находящиеся на ежедневной терапии иГКС, растут на 0,5 см меньше в течение первого года лечения [22, 23]. Первый систематический обзор включал 25 исследований: 8471 ребенок с легкой и среднетяжелой БА, из которых 5128 были на лечении иГКС, а остальные дети получали плацебо. иГКС давали в низкой или средней дозе на протяжении от 3 месяцев до 4–6 лет. Средние показатели прибавок роста за год лечения были в среднем 6–9 см в группе контроля и на 0,5 см меньше в группе иГКС [22]. Второй систематической обзор также оценивал влияние низких или средних доз иГКС на рост у 728 детей с легкой и среднетяжелой персистирующей БА в течение года. В результате дети на низких дозах имели более высокую прибавку в росте на четверть сантиметра (5,74 в год, по сравнению с 5,94 см в год при терапии средними дозами) [23]. Еще один метаанализ, состоящий из 16 рандомизированных клинических исследований, также показал, что годовая терапия иГКС значительно снижает скорость роста у детей с различной степенью тяжести бронхиальной астмы [среднее различие –0,48 см/год (95% ДИ от –0,66 до –0,29)]. Окончательный рост у взрослого больного бронхиальной астмой был снижен в среднем на 1,20 см (95% ДИ от –1,90 см до –0,50 см) при лечении будесонидом по сравнению с плацебо [24].
Другая группа препаратов, широко использующаяся у детей, — это АЛТР, которые также имеют выраженный противовоспалительный эффект и высокий профиль безопасности. Лейкотриены — это важнейшие провоспалительные медиаторы, синтезируемые de novo клетками дыхательных путей (альвеолярными макрофагами и тучными клетками) и воспалительного инфильтрата (эозинофилами и нейтрофилами) при их активации. Цистеиниловые лейкотриены С4, D4, Е4 образуются из арахидоновой кислоты при участии 5-липоксигеназы и пептидаз. Они являются ключевыми медиаторами в патогенезе бронхиальной астмы: индуцируют продукцию слизи, развитие отека, эозинофилии и бронхоспазма.
Согласно рекомендациям Британского торакального общества (British Thoracic Society, BTS), АЛТР могут назначаться как альтернатива иГКС или в качестве добавочной терапии у тех детей, кто не полностью ответил на лечение иГКС [25]. Гайдлайн, опубликованный Национальным институтом здравоохранения (National Institute of Health, NIH), рекомендует назначение АЛТР для маленьких детей в качестве преодоления трудности использования ингаляционных устройств или когда присутствует низкий комплаенс [26].
Эффективность монтелукаста (оригинальный препарат Сингуляр) в качестве базового препарата при рецидивирующим вирус-индуцированном визинге у маленьких детей была подтверждена в нескольких крупных рандомизированных исследованиях. Было проведено проспективное, открытое, рандомизированное исследование 595 детей раннего возраста из группы высокого риска развития аллергических заболеваний. У всех детей был диагностирован визинг после РС-вирусной инфекции и назначен монтелукаст (Сингуляр) курсом в течение 12 недель. Эффективность монтелукаста оценивалась по шкале оценки клинических симптомов, функции легких, использованию КДБА и постановке диагноза инфантильной астмы. После 12 недель лечения получены значительные различия в оценке по шкале симптомов в отношении кашля, визинга, явления визинга на нагрузку, а также уменьшение числа госпитализаций и дней с использованием КДБА (р < 0,05). Диагноз бронхиальной астмы был поставлен в 9,6% (57 детей из 595). В результате авторы приходят к выводу, что монтелукаст клинически эффективен в лечении вирус-индуцированного визинга, улучшении функции легких и снижении риска инфантильной астмы [27].
Хорошо известен факт нарастания частоты обращений за оказанием экстренной помощи для детей с БА в осенне-зимний период в связи с увеличением случаев острых респираторных инфекций. Было проведено мультицентровое, рандомизированное двойное слепое плацебо-контролируемое исследование в течение 12 месяцев у 220 детей 2–14 лет с интермиттирующей БА. 113 детей получали плацебо, 107 получали монтелукаст (Сингуляр) в дозе 4 мг для детей 2–5 лет и 5 мг для 6–14 лет. Было важно, что лечение инициировалось родителями в начале каждой инфекции ВДП или симптомов астмы. Лечение продолжали минимум 7 дней или до тех пор, пока симптомы были компенсированы в течение 48 часов, но максимум 20 дней. В результате терапии монтелукастом симптомы БА были снижены на 14% и ночные пробуждения от БА на 8,6% (p = 0,043). Количество выданных справок школьникам уменьшилось на 37% и больничных листов по уходу за ребенком на 33% (p < 0,0001) [28].
Представляет интерес еще одно исследование выраженного противовоспалительного эффекта монтелукаста (Сингуляра) у маленьких детей. В плацебо-контролируемом исследовании с участием 42 детей с бронхиальной астмой в возрасте 2–5 лет монтелукаст был добавлен к базовой терапии на 45 дней в осенний период, и это привело к уменьшению числа дней обострения БА у мальчиков, но не у девочек [29].
Особенно важно учитывать возможность использования АЛТР для снижения стероидной нагрузки у детей с бронхиальной астмой. Было проведено рандомизированное, двойное плацебо-контролируемое исследование у 76 детей с астмой в возрасте 6–14 лет, с сенсибилизацией к клещам домашней пыли. Исследовали возможность снижения дозы иГКС, частоту обострений, функцию легких, АСТ-тест и изменение ОФВ
Еще одно исследование, оценивающее на протяжении 12 недель эффективность монтелукаста в качестве монотерапии или в комбинации с иГКС, подтвердило эффективность использования АЛТР у детей, больных астмой. Это мультицентровое, открытое, обсервационное исследование у детей (6,9 ± 3,4 года) с неконтролируемой астмой. Было обследовано 328 пациентов, из которых 76 (23,2%) были на монотерапии монтелукастом и 252 (76,8%) на комбинированной: иГКС + монтелукаст. Через 4 недели 61,3% и 52,9% пациентов с моно- и комбинированной терапией соответственно достигли контроля над астмой, и через 12 недель эта пропорция увеличилась до 75% и 70,9%. В группе детей с монотерапией по результатам ACQ-теста по контролю над астмой было отмечено улучшение симптомов (среднее ± SD 1,67 ± 0,69, 0,71 ± 0,70 и 0,50 ± 0,52 исходно, 4 и 12 недель соответственно; p < 0,001). В группе иГКС + монтелукаст средняя оценка ACQ-теста значительно улучшилась с 2,02 ± 0,83 исходно до 0,90 ± 0,86 в 4 недели и 0,64 ± 0,86 в 12 недель (p < 0,001). После 12 недель лечения монтелукастом в качестве добавочной терапии 22,6% пациентов снизили дозу иГКС. Одинаковые результаты были получены в группе школьников и дошкольников. Авторы исследования пришли к выводу, что монотерапия монтелукастом или в комбинации с иГКС является эффективной стратегией в достижении контроля над астмой у детей [31].
Учитывая существенно более высокую безопасность антилейкотриеновых препаратов по сравнению с иГКС, были проведены многочисленные исследования по сравнению эффективности этих двух групп лекарственных средств. В канадское исследование были включены 227 детей в возрасте от 2 до 17 лет с легкой или средней тяжести астмой, получавшие либо иГКС (в низкой или средней дозе 250 мкг/день по беклометазону или его эквиваленту), или АЛТР в виде монотерапии. Дети, которые получали АЛТР, были соотнесены 1:3 с детьми на иГКС по возрасту, полу, предыдущей истории обострений. Результаты оценивались по необходимости в приеме пероральных кортикостероидов, их дозировке и длительности приема, наличию обострений и госпитализации, использованию КДБА. В результате, в отличие от АЛТР, монотерапия иГКС незначительно снижает потребность в назначении ОКС или влияет на число обращений за неотложной помощью и ассоциировалась с более высоким уровнем госпитализаций и использованием КДБА. Эти, на первый взгляд, неожиданные результаты могут быть объяснены превалированием недостаточной продолжительности приема иГКС и низким комплаенсом в группе детей, получающих иГКС в виде монотерапии, чем в группе детей, получающих АЛТР [32].
Целью другого двойного слепого, мультицентрового, мультинационального исследования в 93 центрах по всему миру, включая 56 в США и 21 в странах Африки, Австралии, Европе, Северной и Южной Америке, было оценить эффективность монтелукаста у детей младшего возраста с персистирующей неконтролируемой бронхиальной астмой. Обследовано 689 детей в возрасте 2–5 лет, которые в течение 12 недель принимали монтелукаст в дозе 4 мг (461 пациент) или плацебо (228 пациентов). У всех детей была диагностирована персистирующая бронхиальная астма, требующая использование бета-2-агонистов. В результате через 12 недель терапия монтелукастом значительно улучшила уровень контроля над бронхиальной астмой по сравнению с плацебо в отношении наличия дневных и ночных симптомов, ежедневном использовании бета-2-агонистов, количестве бессимптомных дней, частоте обострений бронхиальной астмы, необходимости использования терапии по требованию, качестве жизни и уровне эозинофилов в периферической крови. Клинический эффект был виден уже с первого дня терапии монтелукастом. Не было отмечено значимых различий в частоте выявления клинических побочных эффектов, лабораторных находок или повышенных уровней трансаминаз в сыворотки крови [33].
Основные клинические ситуации, при которых назначается монтелукаст, суммированы в табл. 3. Они включают доказанные и дискутабельные положения, при которых до сих пор изучаются возможности назначения монтелукаста. Монтелукаст — это безопасный препарат с хорошим противовоспалительным эффектом в респираторных путях [34] и сильным бронхопротекторным эффектом [35]. Отличный профиль безопасности монтелукаста и возможность однократного приема через рот способствуют хорошему комплаенсу и отражают основные преимущества его использования у детей младшего возраста. Более того, монтелукаст является хорошей альтернативой иГКС у детей с плохим комплаенсом или у детей с побочными эффектами от длительной терапии стероидами.
Заключение
Антагонисты лейкотриеновых рецепторов являются эффективными противовоспалительными препаратами для лечения БА у детей с аллергической астмой, наличием вирус-индуцированного визинга и бронхоконстрикции, вызванной физической нагрузкой. Существенное значение данной группы препаратов в профилактике обострений бронхиальной астмы. Со времени первых клинических испытаний до сегодняшнего дня область применения этого класса лекарств постоянно расширяется. Будущие исследования в этой области должны включать в себя разработку критериев отбора пациентов для монотерапии монтелукастом или в виде комбинированной терапии, а также поиск биомаркеров для прогноза ответа на терапию.
Литература
- Masoli M., Fabian D., Holt S., Beasley R. The global burgen of asthma: executive summary of the GINA Dissemination Committee report // Allergy. 2004; 59: 469–478.
- Ducharme F. M., Lemire C., Noya F. J. et al. Preemptive use of high-dose fluticasone for virus-induced wheezing in young children // N Engl J Med. 2009; 360: 339–353.
- Connett G., Lenney W. Prevention of inviral induced asthma attacks using inhaled budesonide // Arch Dis Child. 1993; 68: 85–87.
- Wilson N. M., Silverman M. Treatment of acute, episodic asthma in preschool children using intermittenthigh dose inhled steroids t home // Arch Dis Child. 1990; 65: 470–410.
- Bisgaard H., Hermansen M. N., Loland L., Halkjaer L. B., Buchvald F. Intermittent inhaled corticosteroids in infants with episodic wheezing // N Engl J Med. 2006; 354: 1998–2005.
- Zeiger R. S., Mellon M., Chipps B. et al. Test for Respiratory and Asthma Control in Kids (TRACK): clinically meaningful changes in score // J Allergy Clin Immunol. 2011; 128: 983–988.
- Guilbert T. W., Morgan W. J., Zeiger R. S. et al. Long-term inhaled corticosteroids in preschool children at high risk for asthma // N Engl J Med. 2006; 354: 1985–1997.
- Baker J. W., Mellon M., Wald J., Welch M., Cruz-Rivera M., Walton-Bowen K. A multiple-dosing, placebo-controlled study of budesonide inhalation suspension given once or twice daily for treatment of persistent asthma in young children and infants // Pediatrics. 1999; 103: 414–421.
- Teper A. M., Colom A. J., Kofman C. D., maffey A. F., Vidaurreta S. M., Bergada I. Effects of inhaled fluticasone propionate in children less than 2 years old with recurrent wheeezinf // Pediatr Pulmonol. 2004; 37: 111–115.
- Nielsen K. G., Bisgaard H. Thee effect of inhaled budesonide on symptoms, lung function, and cold air and methacholine responsiviness in 2-to 5-year-old asthmatic children // Am J Respir Crit Care Med. 2000; 162: 1500–1506.
- Roorda R. J., Mezei G., Bisgaard H., Maden C. Response of preschool children with asthma symptoms to fluticasone propionate // J Allergy Clin Immunol. 2001; 108: 540–546.
- Bisgaard H., Gillies J., Gronewald M., Maden C. The effect of inhaled fluticasone propionate in the treatment of young asthmatic children: a dose comparison study // Am J Respir Crit Care Med. 1999; 160: 126–131.
- Chavasse R. J., Bastian-Lee Y., Richter H., Hilliard T., Seddon P. Persistent wheezing in infants with an atopic tendency responds to inhaled fluticasone // Arch Dis Child. 2001; 85: 143–148.
- Hofhuis W., van der Wiel E. C., Nieuwhof E. M. et al. Efficacy of fluticasone propionate on lung function and symptoms in wheezy infants // AM J Respir Crit Care Med. 2005; 171: 328–333.
- IIangovan P., Pedersen S., Godfrey S., Nikander K., Noviski N., Warner J. O. Treatment of severe steroid dependent preschool asthma with neubulised budesonide suspension // Arch Dis Child. 1993; 68: 356–359.
- Murray C. S., Woodcock A., Langley S. J., Morris J., Custovic A. Secondary prevention of asthma by the use of Inhaled Fluticasone propionate in Wheezy Infants (IFWIN): doublr-blind, randomized, control study // Lancet 2006; 368: 754–762.
- Pao C. S., McKenzie S. A. Randomized controlled trial of fluticasone in preschool children with intermittent wheeze // Am J Respir Crit Care Med. 2002; 166: 945–949.
- Pedersen S. Do inhaled corticosteroids inhibit growth in children? // Am J Respir Crit Care Med. 2001; 164: 521–535.
- Agertoft L., Pedersen S. Effect of long-term treatment with inhaled budesonide on adult height in children with asthma // N Engl J Med. 2000; 343: 1064–1069.
- Kelly H. W., Sternberg A. L., Lescher R. et al. Effect of inhaled glucocorticoids in childhood on adult height // N Engl J Med. 2012; 367: 904–912.
- Guilbert T. W., Mauger D. T., Allen D. B. et al. Growth of preschool children at high risk for asthma 2 years after discontinuation of fluticasone // J Allergy Clin Immunol. 2011; 128: 956-63.e1-7.
- Zhang L., Prietsch S. O. M., Ducharme F. M. Inhaled corticosteroids in children with persistent asthma: effects on growth // Cochrane Database Syst Rev. 2014; 7: CD009471. http://doi.wiley.com/10.1002/14651858.CD009471.pub2.
- Pruteanu A. I., Chauhan B. F., Zhang L., Prietsch S. O. M., Ducharme F. M. Inhaled corticosteroids in children with persistent asthma: dose response effects on growth // Cochrane Database Syst Rev. 2014; 7: CD009878. http://doi.wiley.com/10.1002/14651858.CD009878.pub2.1.
- Loke Y. K., Blanco P., Thavarajah M., Wilson A. M. Impact of Inhaled Corticosteroids on Growth in Children with Asthma: Systematic Review and Meta-Analysis // PLoS ONE. 2015; 10 (7): e0133428.doi: 10.1371/journal.pone.0133428.
- British Thoracic Society, Scottish Intercollegiate Guidelines Network: British Guideline on the management of asthma.
- National Heart, Lung, and Blood Institute, National Asthma Education and Prevention Program: Expert Panel Report 3. Guidelines for the Diagnosis and Management of Asthma. http://www.nhlbi.nih.gov. Last access on: 09 February 2012.
- Zou Y.-X. et al. Clinical efficacy of montelukast sodium in treating infantile wheezing // European Review for Medical and Pharmacological Sciences. 2014; 18: 775–780.
- Colin F. Robertson et al. Short-course Montelukast for intermittent asthma in children // Am J Respir Crit Care Med. 2007. Vol 175. p. 323–329.
- Johnson N. W, Mandhane P. J., Dai J. et al. Attenuation of the September epidemic of asthma exacerbations in children: a randomized, controlled trial of montelukast added to usual therapy // Pediatrics. 2007; 120: e702–712.
- Stelmach et al. Do children with stable asthma benefit from addition of montelukast to inhaled corticosteroids: Randomized, placebo controlled trial/Pulmonary Pharmacology & Therapeutics. 2015, 31, 42–48.
- Bérubé et al. Effectiveness of montelukast administered as monotherapy or in combination with inhaled corticosteroid in pediatric patients with uncontrolled asthma: a prospective cohort study // Allergy, Asthma & Clinical Immunology. 2014, 10: 21.
- Ducharme F. M., Gingras J., Allen-Ramey F. C., Maiese E. M., Noya F. J. D. // Current Medical Research & Opinion. 2012, Vol. 28, № 1, 111–119.
- Knorr B. et al. Montelukast, a Leukotriene Receptor Antagonist, for the Treatment of Persistent Asthma in Children Aged 2 to 5 Years // Pediatrics. 2001. Vol. 108. № 3.
- Straub D. A., Minocchieri S., Moeller A., Hamacher J., Wildhaber J. H. The effect of montelukast on exhaled nitric oxide and lung function in asthmatic children 2 to 5 years old // Chest. 2005, 127: 509–514.
- Bisgaard H., Nielsen K. G. Bronchoprotection with a leukotriene receptor antagonist in asthmatic preschool children // Am J Respir Crit Care Med. 2000, 162: 187–190.
- Montella et al. Update on leukotriene receptor antagonists in preschool children wheezing disordersItalian // Journal of Pediatrics. 2012, 38: 29.
Г. А. Новик1, доктор медицинских наук, профессор
Е. Г. Халева
ГБОУ ВПО СПбГПМУ МЗ РФ, Санкт-Петербург
1 Контактная информация: ga_novik@mail.ru
Купить номер с этой статьей в pdf