С конца ХХ века и по настоящее время в индустриально развитых странах, в том числе и в России, ведущей причиной смертности населения стали неинфекционные заболевания, доля которых составляет около 90%. Наиболее значимыми причинами смерти являются сердечно-сосудистые (ССЗ) и онкологические заболевания (ОЗ), а также внешние причины [1]. Свою роль в этом играет образ жизни человека, его индивидуальные привычки и генетическая предрасположенность, а также различные факторы внешней среды. По современным представлениям, если оценивать удельный вес этиологических факторов неинфекционной природы, приняв их совокупность за 100%, то ведущее значение имеет нездоровый образ жизни (49–53%). Вторыми по значимости являются генетически детерминированные этиологические факторы (18–22%). Факторы загрязненной окружающей среды представляются третьими по значимости (18–20%), и только четвертое место занимают медицинские этиологические факторы в виде несвоевременности/низкого качества медицинской помощи и проч. (8–10%) [1].
Можно утверждать, что значительная часть болезней современного общества (т. е. «болезней цивилизации») является почти прямым следствием экологической патологии. Экологическая патология (экопатология) (ЭП) — это общепатологические изменения в клетках органов и тканях под влиянием стимулов окружающей среды, измененной человеком [2]. Доказано, что влияние неблагоприятных факторов внешней и производственной среды приводит к более раннему и интенсивному развитию атеросклероза [3, 4], ишемической болезни сердца (ИБС) [5], с более неблагоприятными исходами [3, 5], неалкогольной жировой болезни печени (НАЖБП) [6, 7]. Интенсивное изучение роли ЭП как независимого фактора риска ССЗ отразилось в появлении термина «environmental cardiovascular disease» в зарубежной литературе конца ХХ — начала ХХI века, под которым понимают ССЗ, обусловленные факторами окружающей среды, а ряд исследователей предлагает выделить НАЖБП, ассоциированную с воздействием факторов внешней среды и ксенобиотиков, в отдельную нозологическую форму [8]. При этом необходимо отметить, что, несмотря на интенсивное изучение влияния внешней среды на развитие различных болезней, в доступной нам литературе зарубежными авторами ни разу не было предпринято ни одной попытки систематизировать имеющиеся знания в виде какой-либо классификации.
Изучение советскими и в последующем российскими учеными ЭП и ее влияния на организм человека началось гораздо раньше [2, 9], но публикации носят единичный характер и появляются раз в несколько лет [5, 9, 10]. Это не свидетельствует о неактуальности проблемы окружающей среды для населения России. Влияние ЭП можно продемонстрировать на популяционном уровне. Начиная с 90-х годов прошлого века развитие частоты сердечно-сосудистых заболеваний, в частности ИБС и связанных с ними исходов, неуклонно растет [1]. Наиболее отрицательная динамика в виде увеличения смертности и снижения средней ожидаемой продолжительности жизни наблюдается в наиболее промышленно развитых регионах с наибольшим потенциальным развитием ЭП [11].
Проблема ЭП в настоящее время достаточно малоизучена, данные о ней крайне разрозненны, предыдущие исследования в подавляющем большинстве основывались на изучении профессиональной патологии и эндемических заболеваний. Изучение ЭП в свете данных разделов медицины представляется нам искусственно зауженным, поскольку и профессиональные и эндемические заболевания представляют собой следствие экстремальных острых и/или хронических воздействий среды на организм человека и, следовательно, являются только частью огромной популяционной проблемы. В то же время большинство факторов урбанистической среды воздействуют на человеческий организм в относительно допустимых пределах, постепенно формируя донозологические состояния, которые приводят к ухудшению здоровья населения и увеличивают количество неблагоприятных исходов, несмотря на все более совершенную терапевтическую помощь.
В качестве примера нам бы хотелось привести следующую цепочку взаимодействий факторов окружающей среды и человеческого организма. Летучие органические вещества (ацетон и продукты кетонового ряда, бензол, формальдегид и проч.) и фталаты (компоненты различных пластмасс), являющиеся широко распространенной составляющей среды проживания, тесно связаны с развитием гиперлипидемии, атеросклероза, риском ССЗ и таких неблагоприятных исходов, как инфаркт миокарда [3–5]. В то же время повышение уровня летучих органических веществ в организме человека способствует развитию НАЖБП [16]. НАЖБП может приводить как к развитию неалкогольного стеатогепатита (НАСГ) и цирроза печени, так и к повышению риска ССЗ, сахарного диабета 2-го типа [17, 18]. Являясь частью метаболического синдрома, НАЖБП/НАСГ имеет в своем патогенезе целый ряд биохимических изменений, тесно связанных с нарушением способности гепатоцитов к метаболизму ксенобиотиков. Следовательно, перманентное воздействие вредных факторов постепенно приводит к нарушению функции печени, что становится отправной точкой для множественных метаболических нарушений и началом трансформации донозологических состояний в те или иные нозологические формы «болезней цивилизации».
Данная проблема лежит по большей части в терапевтической плоскости, поскольку подразумевает выделение групп риска, страдающих от экологических условий, для проведения превентивных воздействий по строго определенным лечебным схемам с позиций доказательной медицины. Подобная практика позволит воздействовать на патологические процессы в доклинические периоды болезни, когда выявляемость и обращаемость по поводу данных заболеваний в учреждения здравоохранения крайне низка. Проведение обоснованных превентивных комплексных программ приведет к снижению неблагоприятного воздействия на человеческий организм техногенных воздействий окружающей среды, к снижению смертности, связанной с «болезнями цивилизации», позволит продлить среднюю продолжительность жизни, что представляется важным как для каждого отдельного человека, так и для общества в целом.
В 1996 году Д. Д. Зербино была предложена одна из первых классификаций ЭП [2].
Экологическая патология: основные источники физических и химических стимулов (рабочая номенклатура по Д. Д. Зербино, 1996)
I. ЭП бытовая:
- в жилых помещениях (детергенты, лаки, краски, дезодоранты, парфюмерия, пластмассы);
- гаражи (бензин, масла, лаки, краски);
- в садах (пестициды, удобрения).
II. ЭП профессиональная.
III. ЭП парапрофессиональная.
IV. ЭП «урбанистического» генеза:
- окись углерода, тетраэтилсвинец, бензопирен, котельные.
V. ЭП радиационного генеза:
- испытание атомных и водородных бомб;
- аварии на АЭС;
- аварии приборов;
- зоны добычи урана.
VI. ЭП геохимическая:
- миграция природных элементов.
VII. ЭП «соседствующего» генеза:
- проживание рядом с заводами, химическими комбинатами, открытыми разработками.
VIII. ЭП, связанная с антропогенными изменениями климата:
- фотохимический смог;
- озоновые дыры.
IX. ЭП, обусловленная влиянием электромагнитных полей.
X. ЭП под влиянием ультрафиолетового и лазерного излучения.
Данная классификация имеет несомненную ценность, так как представляет собой попытку объединить и систематизировать факторы экзогенного воздействия на человеческую популяцию в едином понимании для клинической фундаментальной медицины и биологии. Однако данная номенклатура на сегодняшний день имеет целый ряд недостатков. Так, в отдельные разделы вынесены фотохимический смог, представляющий, по мнению автора, ЭП, связанную с изменениями климата, и ЭП урбанистического генеза, хотя фотохимический смог давно уже является частью урбанистических воздействий [13]. Озоновые дыры согласно данной классификации имеют самостоятельное воздействие, в то время как достоверно установлено, что воздействие озоновых дыр связано в первую очередь с усилением солнечного излучения в ультрафиолетовом спектре В (UVB) [20] и является практически прямым радиационным воздействием и, следовательно, должно относиться к ЭП, опосредованной воздействиями того или иного вида излучения. В представленной номенклатуре ЭП, обусловленная воздействием ультрафиолетового излучения, электромагнитных полей, и ЭП радиационного генеза представлены как совершенно разные явления, несмотря на общую их природу [14, 15]. Бытовая ЭП сведена к примерам того, какие помещения бывают в быту и что в них встречается. Таким образом, использование данной номенклатуры крайне затруднительно и маловероятно как для научной, так и для практической деятельности.
В литературе представлена еще одна классификация факторов экзогенного воздействия на человеческую популяцию, основанная на их делении в зависимости от источника поступления химических элементов и их соединений [2]:
1) группа химических болезней, возникающих под влиянием антропогенного загрязнения окружающей среды, — профессиональные, бытовые и урбанистические химические воздействия;
2) природные (геохимические) химические болезни;
3) болезни, не связанные с загрязнением окружающей среды, а носящие чисто индивидуальный характер (подразумевается собственное введение в организм веществ, являющихся ксенобиотическими), — курение, злоупотребление алкоголем, наркомании, токсикомании;
4) ятрогенные химические болезни (по большей части подразумевались так называемые «лекарственные болезни»).
Данная классификация является еще более условной, поскольку объединяет все заболевания в одну когорту, несмотря на то, что курение и злоупотребление алкоголем имеют отношение в первую очередь к отдельным лицам и преимущественно зависят от индивидуального поведения человека. В то время как ЭП представляет собой совокупность воздействий, по большей части не зависящих от поведения индивидуума. Кроме того, в ней не учитываются различные лучевые воздействия на организм человека, которым он подвергается в повседневной жизни и в тех или иных техногенных ситуациях. Представленная классификация не проясняет, какие воздействия считать бытовыми, а какие урбанистическими, что можно также отнести к ее недостаткам.
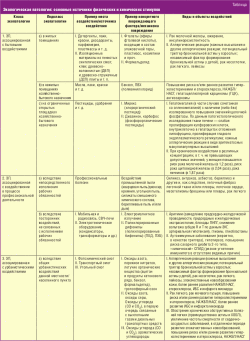
Занимаясь данной проблемой и оценив все разновидности воздействий на организм, мы посчитали возможным представить для обсуждения следующую классификацию ЭП (табл.).
Данная классификация объединяет ЭП по месту соприкосновения с организмом человека и по формам воздействия. Факторы разделены по интенсивности и опасности для здоровья. Таким образом закрывается двойственность трактовки острого и хронического воздействия, затрагивающих прогностическую ценность классификации на этапе предболезни. Термин «парапрофессиональная ЭП» преобразован в подкласс ЭП, ассоциированный с влиянием посторонних патологических факторов, не связанных с исполнением рабочих обязанностей (ЭП-2b).
Приводя примеры действия тех или иных факторов в соответствии с классом или подклассом ЭП, представленная классификация обобщает уже имеющиеся данные о причинно-следственной взаимосвязи внешних факторов и их последствий в виде тех или иных заболеваний. Результаты ЭП различимы как на этапе предболезни в виде неспецифических синдромов (гиперхолестеринемия, синдром «хронической усталости»), так и на ранних этапах заболеваний (атеросклероза, НАЖБП) еще до формирования стойких и необратимых изменений в организме человека.
Таким образом, системное и более подробное изучение ЭП и ее последствий позволит выделить целый ряд взаимосвязей между наиболее распространенными причинами заболеваний современности, внести определенные коррективы в понимание их течения, позволит осуществлять терапевтическое вмешательство на более ранних стадиях этих болезней, что, должно привести к лучшим результатам лечения, повышению качества жизни пациентов и увеличению ее продолжительности. На наш взгляд, прогресс в понимании и лечении «болезней цивилизации» достижим именно с помощью систематизации и четкого понимания природы воздействий на человеческий организм, чему, мы надеемся, должна способствовать представленная нами классификация.
Литература
- Шабунова А. А. Здоровье населения в России: состояние и динамика: монография. Вологда: ИСЭРТ РАН, 2010. 408 с.
- Зербино Д. Д. Экологическая патология и экологическая нозология: новое направление в медицине // Архив патологии. 1996. № 3. С. 10–15.
- Lind P. M. et al. Circulating levels of persistent organic pollutants (POPs) and carotid atherosclerosis in the elderly // Environ. Health Perspect. 2012. Vol. 120. P. 38–43.
- Olsén L. et al. Circulating levels of bisphenol A (BPA) and phthalates in an elderly population in Sweden, based on the Prospective Investigation of the Vasculature in Uppsala Seniors (PIVUS) // Ecotoxicol. Environ. Saf. 2012. Vol. 75. P. 242–248.
- Сергеев А. В. Стойкие органические загрязнители и атеросклероз. Достаточно ли имеющихся фактов, чтобы сделать однозначные выводы // Кардиология. 2010. № 4 (50). С. 50–54.
- Arciello M. et al. Environmental Pollution: A Tangible Risk for NAFLD Pathogenesis // Int. J. Mol. Sci. 2013. Vol. 14. P. 22052–22066.
- Kim J. W. et al. The Role of Air Pollutants in Initiating Liver Disease // Toxicol. Res. 2014. Vol. 30, № 2. P. 65–70.
- Wahlang B. et al. Toxicant-associated Steatohepatitis // Toxicol Pathol. 2013. Vol. 41, № 2. P. 343–360.
- Шпагина Л. А., Бобров С. В. Применение эссенциальных фосфолипидов у лиц, подвергающихся воздействию химических эколого-производственных факторов // Российский журнал гастроэнтерологии, гепатологии, колопроктологии. 2004. № 1 (14). С. 81–85.
- Аносова Е. В., Прощаев К. И. Роль ультразвуковых методов исследования при оценке биологического возраста человека в условиях ухудшающейся экологической ситуации и постоянного роста заболеваемости и смертности от сердечно-сосудистых заболеваний // Fundamental Research. 2011. № 7. С. 238–242.
- Кудрина В. Г., Дубинская Е. Л., Дубинский К. Л. Возможность статистического анализа в мониторинге демографических процессов // Росс. мед. вести. 2001. № 1 (Т. VI). С. 67–70.
- Бурневич Э. З., Краснова М. С. Неинвазивные серологические маркеры фиброза печени // Гепатологический форум. 2007. № 2. С. 18–22.
- Miller Jr., Tyler G. Living in the Environment: Principles, Connections and Solutions (12 th Edition). Belmont: The Thompson Corp., 2002. 423 p.
- IARC classifies radiofrequency electromagnetic fields as possibly carcinogenic to humans / WHO: Press release. 2011. P. 1–6.
- LaSalle D. L. Jr., Kripke M. L. et al. Reducing environmental cancer risk. What We Can Do Now: 2008–2009 Annual Report. National Cancer Institute, National Institutes of Health, 2010. 237 p.
- Rantakokko P. et al. Persistent organic pollutants and non-alcoholic fatty liver disease in morbidly obese patients: a cohort study // J. Environmental Health. 2015. Vol. 79, № 14. P. 1–11.
- Ekstedt M. et al. Long-term follow-up of patients with NAFLD and elevated liver enzymes // J. Hepatology. 2006. Vol. 44, № 4. P. 865–873.
- Lonardo A. et al. Cardiovascular and systemic risk in nonalcoholic fatty liver disease-atherosclerosis as a major player in the natural course of NAFLD // J. Curr Pharm Des. 2013. Vol. 19, № 29. P. 5177–5192.
В. В. Пьянников1, кандидат медицинских наук
Г. И. Нечаева, доктор медицинских наук, профессор
ФГБОУ ВО ОмГМУ МЗ РФ, Омск
1 Контактная информация: pyannikov@rambler.ru
Купить номер с этой статьей в pdf